-
大苏打溶液与氯气反应:Na2S2O3+4Cl2+5H2O=2NaCl+6HCl+2H2SO4 ,说法错误的是
A. 硫代硫酸钠溶液吸收氯气后,溶液的pH降低
B. 氧化产物、还原产物的物质的量之比为1∶1
C. 若0.5molNa2S2O3作还原剂,则转移4mol电子
D. 当Na2S2O3过量时,溶液能出现浑浊
高二化学单选题困难题查看答案及解析
-
硫代硫酸钠溶液与氯气能发生反应:Na2S2O3+4Cl2+5H2O=2NaCl+6HCl+2H2SO4。下列说法错误的是( )
A. 氧化产物、还原产物的物质的量之比为1∶1
B. 若0.5molNa2S2O3作还原剂;则转移4mol电子
C. 当Na2S2O3过量时,溶液能出现浑浊
D. 硫代硫酸钠溶液吸收氯气后,溶液的pH降低
高二化学单选题困难题查看答案及解析
-
纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的化学方程式为4Cl2+Na2S2O3+5H2O===2NaCl+2H2SO4+6HCl,有关该反应的说法正确的是( )
A.该反应中氧化剂是Cl2 B.该反应是复分解反应
C.反应中S元素的价态降低 D.该反应中H2O被氧化
高二化学选择题困难题查看答案及解析
-
下列离子方程式的书写正确的是( )
A. 向Na2S2O3溶液中通入足量氯气:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+
B. 向AlCl3溶液中加入足量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
C. 向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
D. 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+=I2+O2↑+2H2O
高二化学单选题中等难度题查看答案及解析
-
工业上常利用含硫废水生产海波Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。

烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (Ⅰ)
2H2S+SO2=3S+2H2O (Ⅱ)
S+Na2SO3=Na2S2O3 (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaOH溶液
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂(稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液)设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
已知Na2S2O3·5H2O遇酸易分解:S2O32-+2H+=S↓+SO2↑+H2O
(5)为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液20mL,充分反应后滤出硫,微热滤液使生成的SO2全部逸出。
测得有关实验数据如下(标准状况):
第一份
第二份
第三份
样品的质量/g
12.60
18.90
28.00
二氧化硫的体积/L
1.12
1.68
2.24
所用硫酸溶液中溶质的物质的量浓度为 。
高二化学实验题困难题查看答案及解析
-
工业上常利用含硫废水生产海波Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程.

烧瓶C中发生反应如下:
Na2S+H2O+SO2═Na2SO3+H2S (Ⅰ)
2H2S+SO2═3S+2H2O (Ⅱ)
S+Na2SO3
Na2S2O3 (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好.装置D的作用是 .装置E中为 溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 .
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 .
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂(稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液)设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: .已知Na2S2O3•5H2O遇酸易分【解析】
S2O32-+2H+═S↓+SO2↑+H2O(5)为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液20mL,充分反应后滤出硫,微热滤液使生成的SO2全部逸出.
测得有关实验数据如下(标准状况):
第一份
第二份
第三份
样品的质量/g
12.60
18.90
28.00
二氧化硫的体积/L
1.12
1.68
2.24
所用硫酸溶液中溶质的物质的量浓度为 .
高二化学实验题困难题查看答案及解析
-
Na2S2O3俗称大苏打(海波)是重要的化工原料。用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3。已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g。常温下,从溶液中析出的晶体是Na2S2O3·5H2O。
现实验室欲制取Na2S2O3·5H2O晶体(Na2S2O3·5H2O的分子量为248)步骤如下:
①称取12.6g Na2SO3于烧杯中,溶于80.0mL水。
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中。
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤。
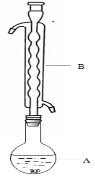
④滤液在经过 、 后析出Na2S2O3·5H2O晶体。
⑤进行减压过滤并干燥。
(1)仪器B的名称是________。其作用是___________。加入的硫粉用乙醇润湿的目的是 。
(2)步骤④应采取的操作是 、 。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是 。如果滤液中该杂质的含量不很低,其检测的方法是: 。
(4)为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L 的碘水,用 (填“酸式”或“碱式”)滴定管来滴定(2S2O32- + I2 = S4O62- + 2I-),滴定结果如下:
滴定次数
滴定前读数(mL)
滴定滴定后读数(mL)
第一次
0.30
31.12
第二次
0.36
31.56
第三次
1.10
31.88
则所得产品的纯度为 ,你认为影响纯度的主要原因是(不考虑操作引起误差) 。
高二化学实验题极难题查看答案及解析
-
大苏打(Na2S2O3·5H2O)、苏打、小苏打被称为“三苏”,它们在生
活、生产中用途广泛。
(1)工业上,将苏打和硫化钠以1:2的物质的量之比配成溶液,再通入SO2气体,可制得Na2S2O3,同时放出CO2。写出该反应的化学方程式 。硫化钠溶液在空气中久置,会生成淡黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的化学式 。
(2)Na2S2O3标准液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因 。
(3)工业上用大苏打溶液吸收工业废气中的氯气,其氧化产物为SO42-,写出离子方程式 。
(4)工业上常用苏打和盐酸除去锅炉中水垢中的硫酸钙。先用饱和苏打溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是 。(并用离子方程式表示)
(5)在密闭的容器中投入一定量的Na2O2和NaHCO3固体,在300℃下充分反应。若残留固体为纯净物,则起始时n(NaHCO3):n(Na2O2)满足的条件是 。
高二化学填空题简单题查看答案及解析
-
下列离子方程式正确的是( )
A. 向Na2S2O3溶液中通入足量氯气:S2O32-+ 2Cl2+3H2O=2SO32-+4Cl-+6H+
B. 等物质的量的FeBr2与Cl2反应为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
C. 等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH-+H+=Mg(OH)2↓+H2O
D. 等体积、等浓度的Ba(OH)2稀溶液与NaHSO4稀溶液混合:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
高二化学单选题中等难度题查看答案及解析
-
下列反应的离子方程式正确的是( )
A、硫酸钠稀溶液与三氧化硫反应:SO42-+SO3+H2O=2H++2SO42-
B、硫酸铝溶液和小苏打溶液混合:Al3++2HCO3-=3CO2+Al(OH)3
C、氯气和溴化钠反应:Cl2+2Br-=2Cl-+Br2
D、碳酸钡溶于醋酸:BaCO3+2CH3COOH=Ba2++2CH3COO-+H2O+CO2
高二化学选择题简单题查看答案及解析