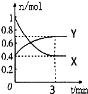-
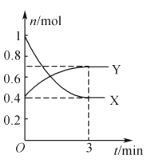
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
-
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.

(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
-
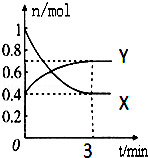
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4g)(无色),如图所示:
N2O4g)(无色),如图所示:
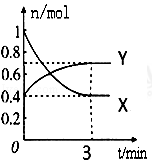
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
-
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
-
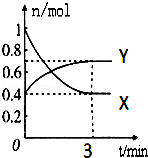
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:
2NO2(g)(红棕色) N2O4(g)(无色),如图所示.
N2O4(g)(无色),如图所示.
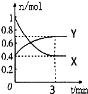
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
-
(8分)在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色) N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。
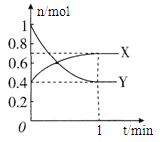
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(正) ,v(逆) 。(填“加快”或“减慢”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L·min),乙中v(N2O4)=0.2 mol/(L·s),则 中反应更快。
(4)在0到1 min中内用X表示该反应的速率是 ,该反应达限度时,Y的转化率 ,反应开始时与反应达平衡状态时的压强之比为 。
-
(题文)在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)⇌N2O4(g)(无色),如图所示.
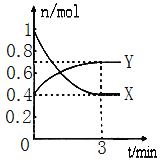
(1)曲线______(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若降低温度,则v(正)________, v(逆)________。(填“加快”或“减慢”或“不变”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得:
甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 _______ 中反应更快。
(4)在0到3min中内N2O4的反应速率为____________________ 。
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号)______________ ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X
-
一定温度下,在体积为0.5 L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2 (g)(红棕色)  N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
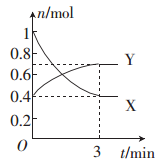
(1)曲线____(填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3 min内,用NO2表示的反应速率为____________。
(3)下列叙述能说明该反应已达到化学平衡状态的是________(填字母)。
a.容器内压强不再发生变化
b.NO2的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolN2O4的同时生成2nmol NO2
(4)反应达到平衡后,若降低温度,则v(正)______,v(逆)________。(填“增大”“减小”或“不变”)。
-
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
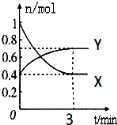
(1)曲线_____(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若降低温度,则υ(正)____,υ(逆)___。(填“加快”或“减慢”或“不变”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中υ(NO2)=0.3mol/(L•s),乙中υ(N2O4)=6mol/(L•min),则_____中反应更快。
(4)在0到3min中内N2O4的反应速率为____。
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号)_____。
A.υ(NO2)=2υ(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X
-
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:
2NO2(g)(红棕色) N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
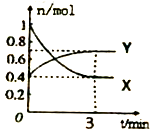
(1)曲线_______(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若降低温度,则v(正)______,v(逆)_____。(填“加快”或“减慢”或“不变”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.003mol/(L·s),乙中v(N2O4)=0.06mol/(L·min)则______中反应更快。
(4)在0到3min中内N2O4的反应速率为_______。
(5)达到反应限度时反应物的转化率为_____;此时混合气体的平均相对分子质量为_____。