乙烯气相直接水合反应制备乙醇C2H4(g)+H2O(g)⇌C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图(起始时,n(H2O)∶n(C2H4)=1∶1)。下列分析错误的是
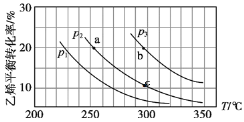
A.乙烯气相直接水合反应的∆H<0
B.图中压强的大小关系为:p1>p2>p3
C.图中a、b点对应的平衡常数相同
D.达到平衡状态a、c所需要的时间:a>c
高一化学多选题中等难度题
乙烯气相直接水合反应制备乙醇C2H4(g)+H2O(g)⇌C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图(起始时,n(H2O)∶n(C2H4)=1∶1)。下列分析错误的是

A.乙烯气相直接水合反应的∆H<0
B.图中压强的大小关系为:p1>p2>p3
C.图中a、b点对应的平衡常数相同
D.达到平衡状态a、c所需要的时间:a>c
高一化学多选题中等难度题
气相直接水合法制乙醇的方程式为:C2H4 (g)+H2O(g)=C2H5OH(g),其中乙烯的平衡转化率与温度、压强的关系如图[起始n(H2O)︰n(C2H4)=1︰1]。
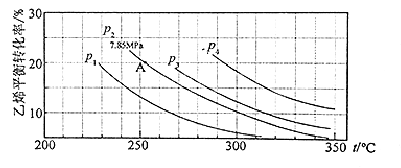
计算乙烯水合制乙醇反应在图中A点的平衡常数KP为(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
A.0.068 MPa-1 B.0.082 C.0.072 MPa-1 D.0.082 MPa-1
【答案】C
【解析】
由图可知,A点乙烯的平衡转化率为20%,设起始量n(H2O)=n(C2H4)=1mol,转化的乙烯为0.2mol,则: C2H4 (g)+H2O(g)=C2H5OH(g)
起始量(mol):1 1 0
转化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
压强之比等于物质的量之比,则p(C2H4)=p(H2O)=7.8MPa×(0.8mol÷1.8mol)=7.8MPa×4/9,p(C2H5OH)=7.8MPa×1/9,则Kp=p(C2H5OH)/[p(C2H4)×p(H2O)]=(7.8MPa×1/9)7.8MPa×4/9×7.8MPa×4/9 =0.072MPa-1,选项C正确。
考点:考查图像方法在化学平衡计算的应用的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】
X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y2是空气的主要成分之一。请回答:
(1)Q元素在周期表中的位置_______________________;
(2)这五种元素原子半径从大到小的顺序为_____________________________(填元素符号)。
(3)元素的非金属性Z____Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有 (填序号)
| A.Q的氢化物的水溶液放置在空气中会变浑浊 |
| B.Z与Q之间形成的化合物中元素的化合价 |
| C.Z和Q的单质的状态 |
| D.Z和Q在周期表中的位置 |
(4)X与Y可形成简单分子A,写出A的电子式_______________;实验室制备气体A的化学方程式 。
高一化学推断题困难题查看答案及解析
乙醇可由乙烯气相直接水合法或间接水合法生产,一些转化如图。

某些物质的有关数据如下表:
| 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | -114.1 | 78.3 | 易溶 |
| 乙醛 | -121 | 20.8 | 易溶 |
| 乙酸乙酯 | -83 | 77.0 | 难溶 |
回答以下问题:
(1)间接水合法中的转化③:乙烯与浓硫酸反应生成硫酸氢乙酯(CH3CH2—OSO3H)的有机反应类型是_____________,转化④的化学方程式是__________________;
(2)蘸有B的玻璃棒遇到氮的最简单氢化物气体会冒白烟,反应的化学方程式为________,转化⑤的化学方程式为______________________________;
(3)将一质量为w的铜丝灼烧变黑后,迅速插入乙醇中,变黑的铜丝恢复红色。
①使铜丝恢复红色的反应的化学方程式为________________________;
②若要证明铜丝起催化作用,还需要进行的操作是_______________;
(4)已知:CH3CHO + NaHSO3 → ↓(α-羟基乙磺酸钠),如上所得乙醛可用如下方式提纯:
↓(α-羟基乙磺酸钠),如上所得乙醛可用如下方式提纯:

①α-羟基乙磺酸钠的晶体类型为___________________。
②分离操作A的名称是________________;
③某同学设计分离操作B的装置(夹持和加热装置已略去)如图所示。冷凝管中的液体应从_____口进。(填“D”或“E”)
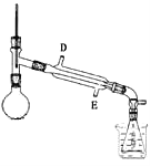
下列有关操作与装置的分析,正确的是_____。(填字母,多选反扣)
A.烧杯中应装冰水
B.冷凝管应通温水
C.图示装置可用于除去乙酸乙酯中混有的乙醇
高一化学综合题中等难度题查看答案及解析
乙烯直接水合法制乙醇因污染小而应用于工业合成,下列有关说法错误的是( )
A. 该反应属于加成反应
B. 乙烯能使酸性KMnO4溶液褪色
C. 乙烷中含有少量乙烯,可用H2除去
D. 等物质的量的乙烯与乙醇充分燃烧,耗氧量相同
高一化学单选题简单题查看答案及解析
实验室用浓硫酸和乙醇反应制备乙烯,若温度过高或加热时间过长,制得的乙烯中往往混有CO2、SO2、H2O (气体少量)。请回答下列问题:
(1)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2、SO2、H2O(g)和乙烯,按气流的方向,各装置的连接顺序是:___________________。
(已知:SO2不能使Br2的CC14 溶液褪色)
| ① | ② | ③ | ④ | ⑤ |
|
|
|
|
|
|
(2)能说明有SO2的现象是_______。能说明有CO2的现象是____________。
(3)装置②中所加的试剂是___________,简述确定装置②在整套装置中的位置的理由是____。
(4)装置①的B中的酸性高锰酸钾溶液发生的炉子方程式为:_________。
(5)工业上用乙烯和水制取乙醇,该反应的类型为______反应。写出HCOOH和CH3CH218OH在浓硫酸作用下发生的化学方程式:___________________。
高一化学实验题困难题查看答案及解析
I、关于工业转化图(见下图):
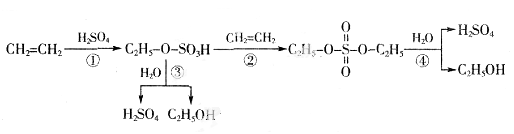
1、①反应类型: ④反应类型: 。
2、实验室制备乙烯的反应条件是 ;反应温度过低会产生副产物: (写结构简式);
II、现拟分离混有乙醇、乙酸和水的乙酸乙酯粗产品,下图是分离操作步骤的流程图,试填写图中试剂的化学式及分离方法
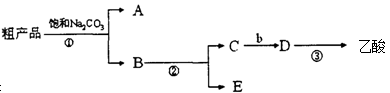
(1)试剂b是 ;
(2)分离方法①是: ;分离方法②是: ;
(3)A是: ;
高一化学填空题简单题查看答案及解析
实验室用浓硫酸和乙醇反应制备乙烯,若温度过高或加热时间过长,制得的乙稀往往混有CO2、SO2、H2O(气体少量)。请回答下列问题:
(1)试分析CO2和SO2是怎么样产生的? (用一句话说明)。
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),按气流的方向,各装置的连接顺序是: 。

(3)实验时若观察到:①中从左到右A瓶中品红溶液褪色,B瓶中高锰酸钾溶液颜色逐渐变浅,C瓶中品红溶液不褪色,则A瓶的作用是______,B瓶的作用是______,C瓶的作用是______。
(4)装置②中所加的试剂名称是______,它可以验证的气体是______,简述确定装置②在整套装置中的位置的理由是___ ___。
(5)装置③中所盛溶液的名称是______,它可以用来验证的气体是______。
高一化学实验题极难题查看答案及解析
某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是( )
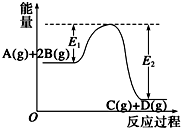
A.该反应为吸热反应
B.当反应达到平衡时,降低温度,A的转化率减小
C.升高温度,平衡常数K增大;压强增大,平衡向正反应方向移动
D.加入催化剂,反应速率增大,E1减小,E2减小,反应热不变
高一化学选择题中等难度题查看答案及解析
某可逆反应正向反应过程中能量变化如图所示,下列说法不正确的是 ( )
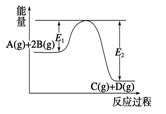
A.压强增大,平衡向正反应方向移动
B.当反应达到平衡时,降低温度,A的转化率增大
C.升高温度,平衡常数K减小;
D.加入催化剂,反应速率增大,E1减小,E2减小,反应热减小
高一化学选择题中等难度题查看答案及解析
(1)在实验室里制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计如图所示实验以确认上述混和气体中有C2H4和SO2。(乙烯的制取装置略)
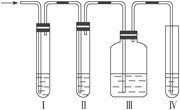
①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛入的试剂是:Ⅰ______、Ⅱ______、Ⅲ______、Ⅳ______。(将下列有关试剂的序号填入空格内)
A. 品红溶液 B. NaOH溶液 C. 浓H2SO4 D. 酸性KMnO4溶液
②能说明SO2气体存在的现象是____________________。
③使用装置Ⅲ的目的是____________________________。
④确定含有乙烯的现象是_________________________。
(2)取一支试管,向其中加入10mL溴水,再加入5mL正己烷(分子式为C6H14,结构简式为CH3CH2CH2CH2CH2CH3)。将此试管中的混合液在光照下振荡后静置,液体分为几乎都是无色的上、下两层。用玻璃棒蘸取浓氨水伸入试管内液面上方,有白烟出现。
① 请写出生成白烟的化学反应方程式:_____________________________。
② 该实验证明了这是一个__________。
A.取代反应 B.加成反应 C.氧化反应 D.水解反应
高一化学实验题中等难度题查看答案及解析
中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下:2CH4(g)⇌C2H4(g)+2H2(g) ΔH>0
| 化学键 | H—H | C—H | C=C | C—C |
| E(kJ/mol) | a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的ΔH=____________ (用含a、b、c、d的代数式表示)。
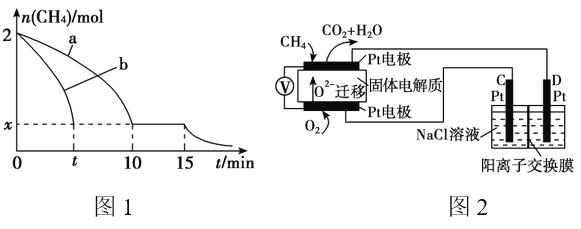
(2)T1温度时,向1 L的恒容反应器中充入2mol CH4 ,仅发生上述反应,反应过程中 0~15min CH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
①0~10min内CH4表示的反应速率为__________mol/(L·min)。
②若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是 ________ (填“a”或 “b”)。
③15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是_____________________________________(任答一条即可)。
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为______ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正____v逆(填“>”“=”或“<”),判断的理由是_________________ 。
(4)科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了 Y2O3与 ZrO2的固体,可在高温下传导O2-。
①C极的Pt为______ 极(填“阳”或“阴” )。
②该电池工作时负极反应方程式为_____________________。
③用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为112mL,则阴极区所得溶液在25℃时pH=_______ (假设电解前后NaCl溶液的体积均为500mL)。
高一化学综合题中等难度题查看答案及解析