-
已知反应:2H2O2=2H2O+O2↑,若其他条件不变,下列措施不能加快该反应速率的是
A. 升高温度 B. 加入少量MnO2
C. 加入浓度更高的H2O2溶液 D. 加水稀释H2O2溶液
高一化学单选题简单题查看答案及解析
-
某化学兴趣小组欲探究反应物浓度对化学反应速率的影响,在保持其他条件都相同的情况下,使四份质量分数不同的H2O2溶液发生分解反应:2H2O2=O2↑+2H2O,其中氧气生成速率最大的是
A. 5%H2O2溶液 B. 10%H2O2溶液 C. 20%H2O2溶液 D. 30%H2O2溶液
高一化学选择题简单题查看答案及解析
-
某化学兴趣小组欲探究反应物浓度对化学反应速率的影响,在保持其他条件相同时,使四份质量分数不同的H2O2溶液发生分解反应:2H2O2═O2↑+2H2O,其中氧气生成速率最大的是( )
A.5%的H2O2溶液
B.10%的H2O2溶液
C.20%的H2O2溶液
D.30%的H2O2溶液高一化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率
B.对于反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
C.将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生
D.100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
高一化学选择题中等难度题查看答案及解析
-
从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O
(1)为了加快该反应速率,不能采取的措施有________(填序号,下同)。
A.使用催化剂 B.适当提高氧气的浓度 C.扩大容器的体积 D.适当降低反应的温度
(2)该反应属于______反应(填“吸热”和“放热”)。
下图能正确表示该反应中能量变化的是________。
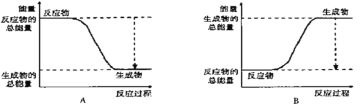
(3)氢氧燃料电池如图所示:
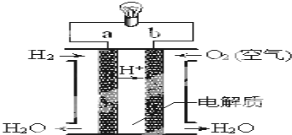
①a为________(填“正极”或“负极”),b电极发生_____反应(填“氧化”或“还原”);
②外电路中电子从b电极___,(填“流入”或“流出”),内电路中阳离子移向____极 (填”a”或”b”);
③写出该装置中正极上的电极反应式:___________________。
高一化学综合题简单题查看答案及解析
-
已知反应:2H2O2=2H2O+O2↑,若其它条件不变,下列措施不能加快该反应速率的是
A. 升高温度 B. 加水稀释H2O2溶液
C. 加入少量FeCl3溶液 D. 加入少量MnO2粉末
高一化学单选题中等难度题查看答案及解析
-
从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A.使用催化剂 B.适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)下图能正确表示该反应中能量变化的是________。

(3)从断键和成键的角度分析上述反应中能量的变化。
化学键
H—H
O=O
H—O
键能kJ/mol
436
496
463
请填写下表:
化学键
填“吸收热量”或“放出热量”
能量变化(kJ)
拆开化学键
2molH2化学键
________
________
1molO2化学键
形成化学键
4molH-O键
________
________
总能量变化
________
________
(4)氢氧燃料电池的总反应方程式为2H2 +O2=2H2O。其中,氢气在______极发生_______反应。电路中每转移0.2mol电子,标准状况下消耗H2的体积是______L。
高一化学综合题简单题查看答案及解析
-
反应条件与环境对化学反应会产生影响,下列说法错误的是( )
化学反应
影响因素
A
过氧化氢不稳定,向溶液中加入少量MnO2后分解速率明显加快
催化剂
B
Na与O2反应既能生成Na2O也能生成Na2O2
温度
C
20mL过氧化氢比10mL过氧化氢产生更多的O2
浓度
D
过氧化氢在酸、碱、中性条件下将高锰酸钾分别还原成Mn2+、MnO42-、MnO2
溶液的酸碱性
A.A B.B C.C D.D
高一化学单选题中等难度题查看答案及解析
-
对于反应2H2O2=2H2O+O2↑,能加快其反应速率的措施是
A. 减小压强 B. 降低温度
C. 加水稀释 D. 使用催化剂
高一化学选择题简单题查看答案及解析
-
影响化学反应速率的因素很多,下列措施不能加快化学反应速率的是
A. 降低温度 B. 升高温度 C. 使用催化剂 D. 增加反应物浓度
高一化学选择题简单题查看答案及解析