-
天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示,其中碳元素显﹣2价、氮元素显﹣2价),N2O4作氧化剂,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4 = 3N2↑+ 4H2O↑+ 2CO2↑,下列叙述错误的是
A. 燃烧反应放出的巨大能量,把火箭送入太空
B. 每生成1mol N2,该反应转移电子8mol
C. N2既是氧化产物也是还原产物,CO2是氧化产物
D. 此反应中R的分子式为C2H8N2
高二化学单选题中等难度题查看答案及解析
-
我国发射“神舟七号”载人飞船时,从火箭尾部喷出的气体呈红棕色,你认为该气体是( )
A.一氧化碳
B.一氧化氮
C.二氧化氮
D.二氧化碳高二化学选择题中等难度题查看答案及解析
-
2016年6月25日20时00分,我国新一代运载火箭“长征七号”在海南文昌航天发射场点火升空,首飞成功。“长征七号”运载火箭使用的是液氧煤油推进剂,下列说法不正确的是
A.工业上可利用空气冷冻成液体后再分离来获得液氧
B.煤油燃烧后的主要产物是水和二氧化碳,绿色环保
C.煤油属于纯净物.主要成分是烃
D.火箭装载的燃料越多,说明其动力越大
高二化学选择题中等难度题查看答案及解析
-
我国“神舟七号”载人飞船的火箭燃料主要是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4═3N2+4H2O+2CO2,下列叙述错误的是
A. 此反应是氧化还原反应
B. R的分子式为C2H8N2
C. 在反应中N2O4做还原剂
D. 生成3mol N2时电子转移数为16mol
高二化学选择题中等难度题查看答案及解析
-
2016年11月,我国首枚大型运载火箭“长征五号”成功发射。该火箭主发动机中所用的液氧(O2)属于
A. 单质 B. 氧化物 C. 化合物 D. 有机物
高二化学选择题中等难度题查看答案及解析
-
2005年10月12日我国用长征二号F型火箭成功发射了神舟“六号”载人飞船,并于10月17日圆满着陆。标志着我国载人航天又有新的突破。长征二号F型火箭用的燃料是液态的偏二甲基肼(C2H8N2),氧化剂是液态的N2O4,已知1.5 g火箭燃料偏二甲基肼完全燃烧生成氮气,二氧化碳和液态水放出热量50 kJ。下列说法不正确的是
A.燃料在火箭发动机中燃烧是将化学能主要转变为热能和机械能
B.偏二甲基肼在四氧化氮中的燃烧反应是放热反应
C.该反应中偏二甲基肼和四氧化氮总能量小于二氧化碳、氮气和水的总能量
D.燃烧时的总反应为:C2H8N2+2N2O4
2CO2+3N2+4H2O
高二化学选择题中等难度题查看答案及解析
-
偏二甲肼[(CH3)2N—NH2]与N2O4是常用的火箭推进剂,火箭发射时常出现红棕色气体,发生的化学反应如下:
① (CH3)2N—NH2(l) + 2N2O4(l) = 2CO2(g) + 3N2(g) + 4H2O(g) ∆H1<0
② N2O4(l)
2NO2(g) ∆H2 >0
下列说法不正确的是
A.反应①中,N2O4为氧化剂
B.反应①中,生成1mol CO2时,转移8 mol e-
C.由反应②推断:加压、降温是获得液态N2O4的条件
D.温度升高,反应①的化学反应速率减小、反应②的化学反应速率增大
高二化学单选题中等难度题查看答案及解析
-
2007年10月24日我国在西昌卫星发射中心用长征三号甲运载火箭将“嫦娥一号”卫星成功送入太空。“嫦娥一号”是我国自主研制的第一颗月球探测卫星,它的发射成功,标志着我国实施绕月探测工程迈出重要一步。
(1)火箭升空时,由于大气层的剧烈摩擦,产生高温,为了防止火箭温度过高,在火箭表面涂上一种特殊的涂料,该涂料的性质最可能的是( )
A.在高温下不熔化 B.在高温下可分解气化
C.在常温下就分解为气体 D.该涂料不可能发生分解
(2)肼(N2H4)是火箭发动机的燃料,它与N2O4反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g) ΔH=+8.7 kJ·mol-1,
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.0 kJ·mol-1,
则肼跟N2O4反应的热化学方程式为_______________。
(3)已知H2O(l)=H2O(g),△H=+44kJ/mol-1。则16g液态肼与足量的N2O4反应生成氮气和液态水时放出的热量是_______________kJ。
高二化学填空题中等难度题查看答案及解析
-
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用.
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体.已知室温下,0.1mol燃料完全燃烧释放出的能量为255kJ,请写出该反应的热化学方程式__ ;
(2)298K时,在2L的密闭容器中,发生可逆反应2NO2(g)
N2O4(g)△H=-a kJ•mol-1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
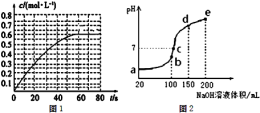
① 298k时,该反应的平衡常数为___________;②若反应在398K进行,某时刻测得n(NO2)=0.6mol,n(N2O4)=1.2mol,则此时V(正)_ _V(逆)(填“>”、“<”或“=”).

③在温度为T1、T
2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示。下列说法正确的是___________
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B=C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d、e五个点,①水的电离程度最大的是___________,②其溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值的是___________。
高二化学填空题困难题查看答案及解析
-
2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)(液态)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全反应生成氮气和1 mol气态水过程中的能量变化图。

(1)该反应属于________(填“吸热”或“放热”)反应。
(2)写出该火箭推进器中相关反应的热化学方程式:__________________。
(3)若该火箭推进器中H2O2有12 mol共价键发生断裂,则反应释放出的热量______kJ。
高二化学简答题中等难度题查看答案及解析