-
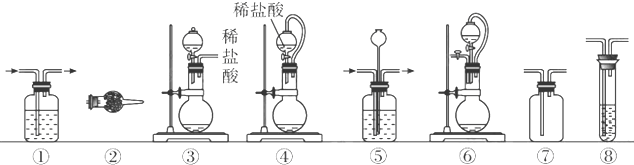
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):
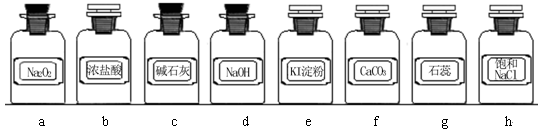
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液 f、CaCO3
g、石蕊试液 h、饱和NaCl溶液
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式______.
(2)下列装置组合最合理的是______(填序号,需考虑实验结束撤除装置时残留有害气体的处理).
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为:______.
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①______,
②______.
-
(12分)实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气。某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气。供选用的实验试剂及装置如下(部分导管、蒸馏水略):
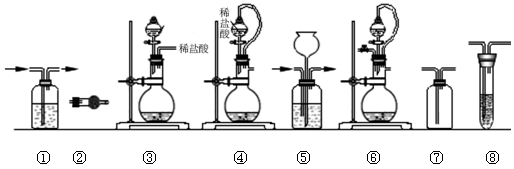
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式_________________________。
(2)下列装置组合最合理的是__________ (填序号,需考虑实验结束撤除装置时残留有害气体的处理)。
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③、⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④、⑥ | ⑤ | ⑧/g | ① |
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为:____________ 。
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ___________________________________,② ___________________________________。
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?___________(填“是”或“否”);理由是__________________________________________ 。
-
(15分)氯气的实验室制法是MnO2和浓盐酸在加热条件下反应,用KMnO4、KClO3氧化浓盐酸可快速制取氯气.根据上述反应原理,有人提出能否利用Na2O2的强氧化性氧化浓盐酸得到氯气呢.某课外小组在实验室进行了探索性实验,设计了如图装置:
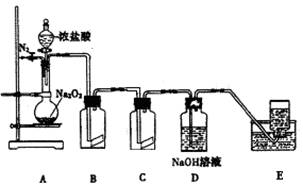
操作步骤及现在如下:
①组装好装置,检查装置的气密性,加入药品.
②缓慢通入一定量的N2后,将装置E连接好(导管未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体.
③一段时间后,将导管末端伸入集气瓶中收集气体.装置E中收集到能使带火星的木条复燃的无色气体.
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色.
回答下列问题:
⑴写出KClO3氧化浓盐酸制取Cl2的离子方程式________
⑵装置B中湿润的红色布条褪色,说明A中有 (填化学式)生成,装置C中为湿润的KI-淀粉试纸,能否仅通过试纸变蓝证明上述结论,请用离子方程式说明原因
⑶装置D的作用是
⑷写出生成O2的可能的反应方程式
⑸实验证明,Na2O2甚至能与干燥的HCl反应生成氯气,写出反应的化学方程式
综合上述实验,请分析实验室________ (填”能”或”否”)利用Na2O2与浓盐酸反应制备纯净的Cl2,理由是
-
KMnO4和MnO2都是重要化学物质,在实验室可以做氧化剂和催化剂,某学习小组对两种物质的制备和性质探究如下:
I.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:
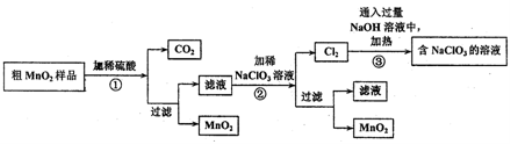
请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为____________。
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为_____________。
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的_________(填序号)。
a. NaCl b. NaClO c. NaClO4 d. NaOH
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器有:_____________,判断是否洗涤干净可选用的试剂是____________(填化学式)。
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为__________。
(6)工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该过程的阳极反应式为___________。
II.KMnO4的制备和性质:
(7)实验室由二氧化锰制备高锰酸钾可分二步进行:
第一步:MnO2与KOH共熔并通入氧气:2MnO2+4KOH+O2=2K2MnO4+2H2O
第二步:通入CO2,可使K2MnO4发生歧化反应生成KMnO4和MnO2。
第二步完成反应时,转化为KMnO4的K2MnO4占其全部的百分率约为_______(精确到0.1%)
(8)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应过程,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:

请将MnO4-氧化C2O42- 的离子方程式补充完整:
______MnO4-+C2O42-+_______=______Mn2++_____CO2↑+_______
请分析KMnO4溶液褪色时间变化的可能原因_____________________。
-
KMnO4和MnO2都是重要化学物质,在实验室可以做氧化剂和催化剂,某学习小组对两种物质的制备和性质探究如下:
I.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:
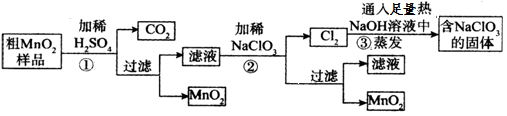
请回答下列问题:
(1)第②步操作中,NaClO3氧化MnSO4的离子方程式为_____________________。
(2)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器除玻璃棒外,还需要有:_________________,判断是否洗涤干净可选用的试剂是_____________(填化学式)。
(3)工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该过程的阳极反应式为____________。
II.KMnO4的性质与应用:该小组同学利用KMnO4溶液测定某物质的组成:
CuSO4溶液与K2C2O4溶液混合反应,产物之一是某种只含一种阴离子的蓝色钾盐水合物。通过下述实验确定该晶体的组成。
步骤a:称取0.6720 g样品,放入锥形瓶,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 ml水加热,用0.2000 mol·L-1KMnO4溶液滴定至终点,消耗8.00 mlKMnO4溶液。
步骤b:接着将溶液充分加热,使淡紫红色消失,溶液最终呈现蓝色。冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI。用0.2500 mol·L-1Na2S2O3标准溶液滴定至终点,消耗8.00 ml Na2S2O3溶液。已知涉及的部分反应的离子方程式为:I2+2S2O32-=2I+S4O62-
(4)已知室温下CuI的Ksp=1.27×10-12,欲使溶液中c(Cu )≤1.0×10-6mol·L-1,应保持溶液中c(I-)≥ mol·L-1。
(5)MnO4-在酸性条件下,加热能分解为O2,同时生成Mn2+。写出该反应的离子方程式为__________________________。若无此加热操作,则测定的Cu2+的含量将会 (填“偏高”、“偏低”或“不变”)。
(6)若用淀粉溶液做指示剂,则滴定终点观察到的现象为__________________。
(7)样品晶体的组成化学式为:_____________________。
-
(14分)某学校研究性学习小组利用实验室常用试剂,
探究硝酸的氧化性。请完成下面的空白:
(1)在具支试管底部滴入5滴浓硝酸,然后用硫化 亚铁与盐酸反应制备H2S气体,如图所示通入具支试管中,可以观察到在试管内形成黄烟,黄烟附着在试管内壁上,形成“黄霜”。
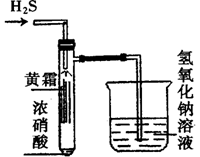
① 出上述制备H2S的离子方程式
______________________________________。
②在试管内壁上的“黄霜”的成分是_______________,该反应说明浓硝酸有氧化性外,实验现象还说明了浓硝酸具有________性。该实验中烧杯内的氢氧化钠溶液的作用是
__________________________________________________________________。
(2)卤族元素单质也具有氧化性,该小组设计了下面的实验探究碘单质与稀硝酸氧化性强弱比较:
①提出合理的假设
假设l:碘单质氧化性强于稀硝酸;假设2:碘单质氧化性弱于稀硝酸。
②设计实验方案,进行实验探究,请写出实验步骤和预期的现象与结论。限选实验试剂与仪器:稀硝酸、KI溶液、四氯化碳;试管、胶头滴管。
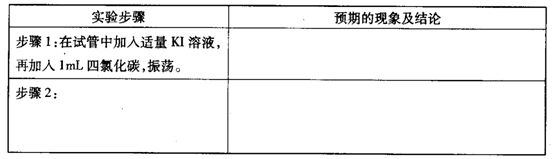
-
实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是( )
A.由题目信息知:KMnO4的氧化性比MnO2的强
B.制备氯气的整个实验过程中,只需要使用氧化剂与还原剂
C.用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体
D.用足量MnO2与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol
-
高锰酸钾是常用的氧化剂。某化学小组在实验室以软锰矿(主要成分是MnO2)为原料制备KMnO4,下图是实验室制备高锰酸钾的操作流程。
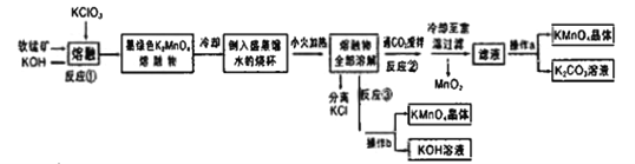
已知:
| 温度 | 溶解度/g |
| K2CO3 | KHCO3 | KMnO4 |
| 20℃ | 111 | 33.7 | 6.38 |
请回答:
(1)反应①的化学方程式为______。加热软锰矿、KClO3、和KOH固体时,除三脚架、玻璃棒、泥三角和铁坩埚外,还用到的仪器有_____,不采用瓷坩埚而选用铁坩埚的理由是________。
(2)反应②中氧化产物与还原产物的物质的量之比为________;上述流程中可以循环利用的物质是__________
(3)实验时,从滤液中得到KMnO4晶体的实验操作a为_____。若CO2过量会生成KHCO3导致得到的KMnO4产品的纯度降低其原因是_________
(4)反应③是模拟工业上采用惰性电极电解法制取高锰酸钾晶体,写出反应的化学方程式_____。
-
该学习小组通过查阅资料发现用KClO3和浓盐酸也可以制备氯气。为此该小组利用下图装置在实验室制取Cl2并探究其有关性质:
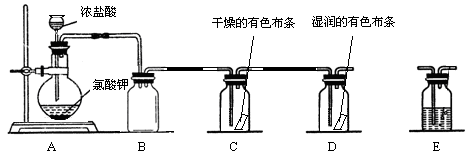
(1)装置A中存在一处错误,改正这处错误:________。
(2)写出装置A中发生反应的化学方程式:________。
(3)为了除去氯气中的氯化氢,需要在.A、B之间装置中添加装置E,装置E中所盛装的试剂为________。为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为________(选填序号)。
a A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入到集气瓶B中,可以观察到的现象是 ,能检验该反应产物中铁元素的价态的试剂________(选填序号,多选)。
a.氯水 b.蒸馏水和铁粉
c.蒸馏水和氢氧化钠溶液 d.蒸馏水和KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷?并给出了改进措施。该改进措施是:________。
-
实验室常用下列三个反应制备Cl2:①MnO2与浓盐酸反应制备氯气;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2 +8H2O; ③KClO3+6HCl(浓)=KCl+3Cl2 +3H2O如果分别用上述方法制得等量的Cl2,下列说法中正确的是 ( )
A.参加反应的HCl的物质的量相等
B.转移电子的总数相等
C.消耗氧化剂的物质的量相等
D.被氧化的氯离子数不相等










