-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请回答下列问题:
(1)实验室制取氯气的反应原理为:MnO2+4HCl(浓)  MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
①该反应中被还原的元素是________,还原剂是________。
②取一定量的浓盐酸使其与二氧化锰反应,产生的氯气在标准状况下的体积为33.6 L,则被氧化的HCl的物质的量为________,反应中转移电子数为________ 。
(2)某同学用下列装置制备并检验Cl2的性质。
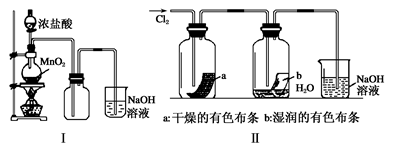
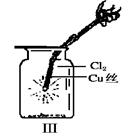
下列说法正确的是________
a.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
b.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
c.Ⅲ图中:生成蓝色的烟
(3)若氯气罐发生泄漏,当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是________。
a.NaOH b.NaCl c. KOH d. Na2CO3
(4)将SO2和Cl2分别通入装有品红溶液的两个试管中,两溶液的红色均褪去。加热后,有一支试管中的溶液又呈现红色,该试管通入的气体是________。
将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色。为检验两种气体在溶液中是否发生了氧化还原反应,应向所得溶液加入的试剂是________(填化学式)。经实验证明,SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是________。
-
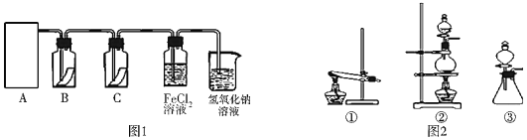
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。为探究氯气的性质,某同学设计了如图1所示的实验装置。
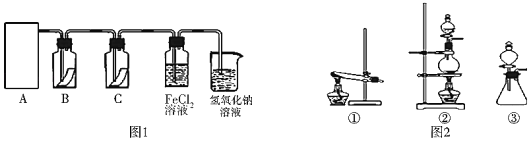
(1)实验中制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,该反应中还原剂是_____,还原产物是_____
MnCl2+Cl2↑+2H2O,该反应中还原剂是_____,还原产物是_____
(2)利用(1)中制气原理,从图2中选择合适的制气装置(A处):_____(填写序号)。
(3)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,理论上装置_____中的红色布条退色,但实验过程中该同学发现装置B、C中的布条均退色,其原因可能是_____,说明该装置存在明显的缺陷,请提出合理的改进方法_____
(4)为了验证氯气的氧化性,将氯气通入FeCl2溶液中,写出氯气与FeCl2溶液反应的离子方程式_____
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____(填化学式)。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中 是氧化剂,该反应中氧化产物与还原产物的物质量之比为 。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是: 。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液 mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式并用双线桥法表示出电子转移情况: 。
(5)现需490 mL 2.0 mol·L-1NaOH溶液:
①所需称量的氢氧化钠固体的质量是 。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、 。
③在配制溶液的过程中,下列操作可能造成结果偏高的是 。
| A.定容时俯视 |
| B.容量瓶不干燥,含有少量蒸馏水 |
| C.溶解所用烧杯未洗涤 |
| D.NaOH溶解后,未冷却即进行实验 |
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中____是氧化剂,该反应中氧化产物与还原产物的物质的量之比为____。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:______________________。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液____mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式______________。
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是____。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、______。
③在配制溶液的过程中,下列操作可能造成结果偏高的是____。
A.定容时俯视
B.容量瓶不干燥,含有少量蒸馏水
C.溶解所用烧杯未洗涤
D.NaOH溶解后,未冷却即进行实验
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中____是氧化剂,该反应中氧化产物与还原产物的物质的量之比为____。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:______________________。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液____mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式______________。
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是____。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、______。
③在配制溶液的过程中,下列操作可能造成结果偏高的是____。
A.定容时俯视
B.容量瓶不干燥,含有少量蒸馏水
C.溶解所用烧杯未洗涤
D.NaOH溶解后,未冷却即进行实验
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰外还可以利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需要加热。请你根据所学知识回答下列问题
(1)该反应中氧化产物与还原产物的物质的量之比为_____________________。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是________________________________。
(3)实验室配制好2.0mol/L NaOH溶液,需要这种溶液____________mL才能与4.48L氯气(标准状况)恰号完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式_________________________________。
(5)现需490mL 2.0mol/L NaOH溶液:
ⅰ所需称量的氢氧化钠固体的质量是__________________。
ⅱ上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、______________。
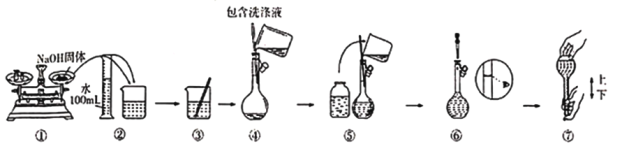
ⅲ某同学部分配制过程如图所示,你认为有错误的操作是_____________________;若按操作所示称量时,指针向左偏,则所配溶液浓度将____________________(填“偏高”“偏低”或“不变”)
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
(1)把氯气缓慢通入紫色石蕊溶液中,可以观察到的现象是 。
(2)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
①其反应原理为:(用离子方程式表示) 。
②实验室配制好4.0 mol·L-1的NaOH溶液,这种溶液________mL才能与2.24 L氯气(标准状况)恰好完全反应。
(3)配制250 mL 4.0 mol·L-1 NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量
b.称量氢氧化钠固体
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量蒸馏水溶解称量好的氢氧化钠固体,静置冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1 cm~2 cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切。
①用天平称量的所需氢氧化钠固体的质量是______g。
②上述步骤的正确操作顺序___________________。
(4)某化学实验小组的同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。


①实验室常选用制CO2的发生装置,用KMnO4和浓盐酸制Cl2;选用Cu和浓硫酸反应制取SO2时,应选用上图A、E两发生装置中 装置(填装置序号),反应的化学方程式为 。
②反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B: ,D: 。
(5)化学实验小组的同学还利用下图所示装置探究SO2和Cl2按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:a.控制气体通入速率;b. 。
②实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是 (用化学方程式表示)。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊溶液中,可以观察到的现象是_________;
(2)氯气与水反应生成次氯酸(HClO)具有杀菌作用,常用于自来水消毒。请写出氯气与水反应的化学方程式:___________,在该反应中氧化产物是_________,还原产物是____________。
(3)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。其反应原理为(用化学方程式表示):_________。
(4)某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用:
①该同学应称取NaOH固体__________ g;
②上述实验除了需要托盘天平、药匙、烧杯、玻璃棒、量筒等仪器外,还需要的仪器有_______。
③下列操作使配制的NaOH溶液浓度偏低的有__________。
A.将砝码放在左盘上,NaOH放在右盘上进行称量
B.定容的仰视刻度线
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡
(5)取上述配制的NaOH溶液______ L才能与0.224 L 氯气(标准状况下)恰好完全反应。
-
氯气是一种重要的化工原料,在工农 业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
Ⅰ.把氯气通入紫色石蕊溶液中,可以观察到的现象是:
请你解释其中的原因 。
Ⅱ.某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
(1)其反应原理为: (用化学方程式表示)
(2)实验室配制好4.0 mol·L-1的NaOH溶液,这种溶液 L才能与2.24 L氯气(标准状况)恰好完全反应。
(3)配制500 mL 4.0 mol·L-1 NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量。
b.称量氢氧化钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量蒸馏水溶解称量好的氢氧化钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1 cm~2 cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切。
①所需称量的氢氧化钠固体的质量是
②上述步骤的正确操作顺序是
③上述实验需要的仪器有
 ④某同学观察液面的情况如图所示,对所配溶液的物质的量浓度有何影响? (填“偏高”、“偏低”或“无影响”);
④某同学观察液面的情况如图所示,对所配溶液的物质的量浓度有何影响? (填“偏高”、“偏低”或“无影响”);
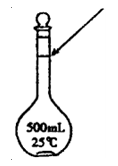
⑤在配制溶液的过程中,下列操作能造成结果偏低的是 。
A.容量瓶不干燥,含有少量蒸馏水
B.溶解所用烧杯未洗涤
C.NaOH溶解后,未冷却即进行实验
D.定容后摇匀,发现液面低于刻度线,然后又加水至刻度线。
-
(4分)氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
把氯气通入紫色石蕊溶液中,可以观察到的现象是: ;
请你解释其中的原因________
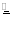 MnCl2+Cl2↑+2H2O,该反应中还原剂是______.
MnCl2+Cl2↑+2H2O,该反应中还原剂是______. 处
处 :______
:______ 填写序号
填写序号 。
。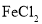 溶液中,写出氯气与
溶液中,写出氯气与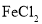 溶液反应的离子方程式______。
溶液反应的离子方程式______。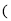 填化学式
填化学式 。
。





