-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g) + O2(g)  2SO3(g)
2SO3(g)  H=-197 kJ/mol。下列说法正确的是
H=-197 kJ/mol。下列说法正确的是
A.使用催化剂可以提高该反应的焓变
B.增大O2的浓度可以提高反应速率和SO2的转化率
C.反应450℃时的平衡常数小于500℃时的平衡常数
D.2 mol SO2(g) 和1 mol O2(g)所含的总能量小于2 mol SO3(g) 所含的总能量
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g) + O2(g) 2SO3(g)
2SO3(g) H=-197 kJ/mol。下列说法正确的是
H=-197 kJ/mol。下列说法正确的是
A.使用催化剂可以提高该反应的焓变
B.增大O2的浓度可以提高反应速率和SO2的转化率
C.反应450℃时的平衡常数小于500℃时的平衡常数
D.2 mol SO2(g) 和1 mol O2(g)所含的总能量小于2 mol SO3(g) 所含的总能量
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g) + O2(g) 
 2SO3(g),
2SO3(g), H=-197 kJ/mol。下列说法正确的是
H=-197 kJ/mol。下列说法正确的是
A.使用催化剂可以提高SO2的转化率
B.增大O2的浓度可以提高反应速率和SO2的转化率
C.反应450℃时的平衡常数小于500℃时的平衡常数
D.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
-
根据以下事实,回答下列问题
(1)工业接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)⇌2SO3(g)△H=-190kJ•mol-1该热化学反应方程式的意义是______.
(2)在25℃、101kPa下,1g甲醇[CH3OH(l)]燃烧生成CO2和液态水时放热.22.68kJ.则表示甲醇燃烧热的热化学方程式为______.
(3)已知25℃、l01kPa时下列反应的热化学方程式为:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H=-870.3kJ/mol
②C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
③H2(g)+ O2(g)=H2O(l)△H=-285.8kJ/mol,则C(s)与H2(g)、O2(g)反应生成CH3COOH(l)在该条件下的热化学方程式为______.
O2(g)=H2O(l)△H=-285.8kJ/mol,则C(s)与H2(g)、O2(g)反应生成CH3COOH(l)在该条件下的热化学方程式为______.
(4)由N2和H2合成1molNH3时可放出46.2kJ的热量.从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是______.
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)⇌△催化剂2SO3(g);△H=﹣190kJ•mol﹣1
(1)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.8g,则V(O2)= mol•L﹣1•min﹣1,计算此时化学平衡常数K1= .
(2)若温度不变,继续通入0.20mol SO2和0.10mol SO3,则平衡移动方向及原因是 ,达平衡后,化学平衡常数为K2,则K1、K2之间的关系为 (填“>”、“<”或“=”).
(3)有两只密闭容器A和B,A能保持恒容,B能保持恒压.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应.则(填>、=、<;左、右;增大、减小、不变).
①达到平衡所需要的时间:t(A) t(B)
②平衡时,SO2的转化率:a(A) a(B)
③达到平衡时,在两容器中分别通入等量的Ar气.B中的化学平衡向 反应方向移动,A中的化学反应速率 .
-
(1)接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:
2SO2(g)+O2(g)  2SO3(g) ΔH=-190Kj/mol
2SO3(g) ΔH=-190Kj/mol
①下列描述中能说明上述反应已达平衡的是____________。
a.  (O2)正=2
(O2)正=2 (SO3)逆 b.容器中气体的密度不随时间而变化
(SO3)逆 b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化 d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则 (O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
(O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol3) <_____mol。
(2)工业生成尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3 (g)+ CO2(g)  CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH_______0(填“>”、“<”或“=”)
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) =x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。
=x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。
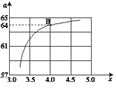
③右图中的B点对应的NH3的平衡转化率为___________。
-
(8分)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)  2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1
(1)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则v(O2)= mol·L-1·min-1
(2)下列条件的改变能加快其反应速率的是 (选填序号)
①升高温度 ②保持体积不变,只增加氧气的质量
③保持体积不变,充入Ne使体系压强增大 ④保持压强不变,充入Ne使容器的体积增大
(3)下列描述中能说明上述(1)反应已达平衡的是 (选填序号)
①v(O2)正=2v(SO3)逆 ②SO2、O2、SO3的浓度之比为2:1:2
③单位时间内生成2n molSO2的同时生成2n mol SO3 ④容器中气体的平均分子量不随时间而变化
⑤容器中气体的密度不随时间而变化 ⑥容器中气体压强不随时间而变化
(4)在相同条件下发生上述反应,若要得到380kJ热量,则加入各物质的物质的量可能是 。
A.4 mo1SO2和2mol O2 B.6mol SO2和6mo1 O2
C.4mol SO2和4 mo1 O2 D.6mo1 SO2和4 mo1 O2
-
接触法制硫酸工艺中,主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g) 
(1)上述反应的平衡常数表达式为___________。
(2)恒温恒容条件下,下列能说明此反应已达平衡的是______________。
a. v正(O2)=2v逆(SO3)
b. 容器中气体的密度不随时间而变化
c. 容器中气体的平均摩尔质量不随时间而变化
(3)下列有关该反应的叙述中,正确的是__________。
a. 升高温度可以增大活化分子百分数,加快反应速率
b. 使用催化剂提高二氧化硫的平衡转化率
c. 使用催化剂可以使反应物分子平均能量升高,加快反应速率
d. 缩小容器体积增大压强不能增大活化分子百分数,但可以加快反应速率
(4)一定温度下,在容积不变的密闭容器中充入4mol SO2和2mol O2,达平衡时SO2的体积分数为a%,其他条件不变时,若按下列四种配比作为起始物质,平衡后SO2的体积分数仍为a%的是___________。
a. 2mol SO3 b. 2mol SO2+1mol O2
c. 4mol SO3 d. 2.5mol SO2+1.25mol O2+1.5mol SO3
(5)SO2与H2O反应生成H2SO3,H2SO3电离方程式为____________;将H2SO3溶液加入酸性KMnO4溶液中,溶液紫色褪去,将下列离子方程式补充完整:
_________+_____MnO4-=______Mn2++_______________
-
(16分) 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g) ΔH=-190kJ·mol-1
2SO3(g) ΔH=-190kJ·mol-1
(1)该热化学反应方程式的意义是_______________________________________________
升高温度上述反应平衡常数____(填“变大”“变小”或“不变”)。
(2)下列描述中能说明上述反应已达平衡的是________。
a.v(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=__________mol·L-1·min-1;若继续通入0.20 mol SO2和0.10 mol O2,则平衡________________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol<n(SO3)<________mol。
-
(1) 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)  2SO3(g)
2SO3(g)  H = -190 kJ·mol-1
H = -190 kJ·mol-1
该热化学反应方程式的意义是____________________________________。
(2) 处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知: CO (g)+ O2 (g) = CO2 (g)
O2 (g) = CO2 (g)  H = -283.0 kJ·mol-1
H = -283.0 kJ·mol-1
S (g)+ O2 (g) = SO2 (g)  H = -296.0 kJ·mol-1
H = -296.0 kJ·mol-1
此反应的热化学方程式是__________________________________________________。
2SO3(g);△H=-190KJ·mol-1
