-
工业上利用某工厂的废渣(主要含CuO70%、MgFe2O420%,还含有少量FeO、NiO等氧化物)制取精铜和颜料铁红。流程如图所示。
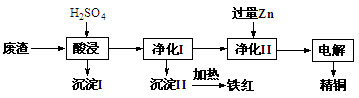
回答下列问题:
(1)净化Ⅰ操作分为两步:
第一步是将溶液中少量的Fe2+氧化;
第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下用H2O2氧化Fe2+反应的离子方程式: 。
②25 ℃时,pH=3的溶液中,c(Fe3+)=___________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ中第二步可选用CuO实现转化,用化学平衡移动原理说明其原因:
。
(2)用净化II所得的金属为电极进行电解得精铜,请写出阴极所发生的电极反应式:______________________________。
(3)为准确测定酸浸液中Fe2+的物质的量浓度以确定H2O2的用量,测定步骤如下:
①取出25.00mL酸浸液,配制成250.0mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,将0.2000mol/LKMnO4溶液装入
(填仪器名称),进行滴定,记录数据,重复滴定3次,平均消耗KMnO4溶液V mL。(反应离子方程式:5Fe2++MnO +10H+=5Fe3++Mn2++5H2O)
+10H+=5Fe3++Mn2++5H2O)
③计算酸浸液中Fe2+的物质的量浓度= mol/L (只列出算式,不做运算)。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示.回答下列问题:
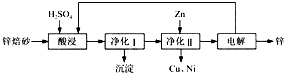
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为____________;
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀.
①写出酸性条件下H2O2与Fe 2+反应的离子方程式:____________;
②25℃时,pH=3的溶液中,c(Fe3+)= ____________mol•L-1(已知25℃,Ksp[Fe( OH)3]=4.0×10-38).
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____________;
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是____________;
(4)本流程中可以循环利用的物质除锌外还有____________。
-
某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu (NO3)2的部分工艺流程如图所示:

(1)Cu与稀硝酸反应的离子方程式为_______________________________________。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是______________,若保持反应温度为70℃,欲加快反应速率可采取的措施为______________________(写2种)。
(3)过滤后所得废渣的主要成分的化学式为________________。
(4)由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、_____、过滤、冰水洗涤、低温烘干。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO、SiO2等氧化物杂质)制取金属锌的流程如图所示。回答下列问题:
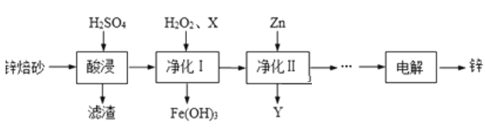
(1)ZnFe2O4中Fe的化合价为_________价,已知ZnFe2O4能溶于酸,则酸浸时ZnFe2O4反应的离子方程式为_________,酸浸后滤渣的成分主要是_________。
(2)酸浸时一般要将锌焙砂粉碎,其目的是提高酸浸效率,为达到这一目的,还可以采用的方法是_________(任答一条即可)
(3)净化Ⅰ中H2O2参与反应的离子方程式为_________,试剂X的作用是_________,
(4)净化Ⅱ中得到的Y是_________。
-
NiSO4 6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
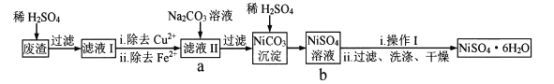
A.溶解废渣时不能用稀盐酸代替稀H2SO4 B.除去Cu2+可采用FeS
C.流程中a-b的目的是富集NiSO4 D.“操作I”为蒸发浓缩、冷却结晶
-
为了充分利用铜资源,某工厂拟用黄铜灰(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3、SiO2等)制取金属铜并得副产物锌盐,其生产流程如图:
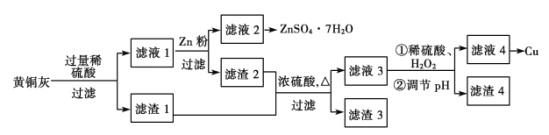
(1)滤渣1的主要成分为__。稀硫酸溶解黄铜灰过程中,可能发生多个氧化还原反应,其中没有Zn参加的反应的离子方程式是__。
(2)滤渣1及滤渣2用浓硫酸浸取可能产生的有毒气体是__(填化学式),实验室通常用__(填化学式)溶液吸收。
(3)从滤液2中获取硫酸锌晶体的方法是加热浓缩、__、过滤等。
(4)过滤操作所需玻璃仪器除玻璃棒外还有__。
(5)根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:__。
-
工业上利用硫酸废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)并回收(NH4)2SO4,具体生产流程如图所示:
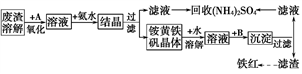
注:铵黄铁矾的化学式为(NH4)2Fe6(SO4)4(OH)12
回答下列问题:
(1)在废渣溶解操作中,加速废渣溶解的措施有________。
(2)物质A是一种氧化剂。
①工业上物质A最好选用________(填序号)。
A.空气 B.Cl2 C.MnO2 D.KMnO4
②简述工业上这样选择A的理由:__________________________________。
③写出A参与反应的离子方程式:__________________________________。
(3)往铵黄铁矾溶液(含Fe3+)中加入溶液B至pH为5时产生沉淀,请写出产生沉淀的离子方程式:__________________________________。
(4)回收所得的(NH4)2SO4晶体中可能含有的杂质是_______________________。
-
(9分) 硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
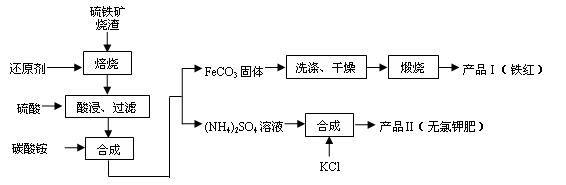
已知几种盐的溶解度随温度变化的曲线如下图所示:
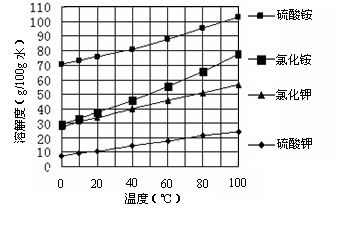
回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是________________。
(2)煅烧FeCO3生成产品I的化学反应方程式为________________________________。实验室进行煅烧操作所需仪器除了酒精灯、泥三角、三脚架、玻璃棒外,还有__________。
(3)产品Ⅱ的化学式为_______________,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是:________。
(4)检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,滴加过量Ba(NO3)2溶液,过滤后向滤液滴加硝酸酸化的AgNO3溶液。判断Ba(NO3)2已过量的方法是________。
-
工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3 ),具体生产流程如下:

试回答下列问题:
(1)滤液X中含有的金属阳离子是________(填离子符号)。
(2)步骤Ⅲ中可选用________试剂调节溶液的pH(填字母)。
A.稀硝酸 B.氨水 C.氢氧化钠溶液 D.高锰酸钾溶液
(3)过滤操作中除了玻璃棒、烧杯还需要的玻璃仪器是________。
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是________。
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为________。
-
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料-----铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为_____________________________;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有___________、玻璃棒和烧杯等;步骤Ⅳ中应选用______试剂调节溶液的pH(填字母编号)
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是________________;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是________________;
(5)步骤Ⅵ中发生反应的化学反应方程式为_____________________________;
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol•L-1.试判断所得的FeCO3中是否含有Fe(OH)2__________(填“是”或“否”),请通过简单计算说明理由__________________________(已知:Ksp[Fe(OH)2]=4.9×10-17)。

+10H+=5Fe3++Mn2++5H2O)









