-
钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。请回答下列问题:
(1)Co基态原子的外围电子排布式为 ;
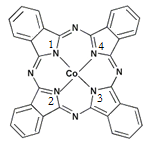
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
①酞菁钴中三种非金属原子的电负性由大到小的顺序为 ;
(用相应的元素符号作答);碳原子的杂化轨道类型为 ;
②与钴离子通过配位键结合的氮原子的编号是 ;
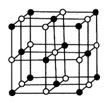
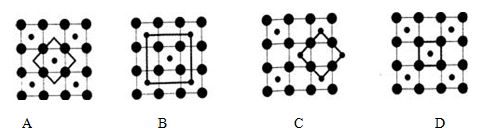
(3)Co的一种氧化物的晶胞如下图所示,在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是 。
-
钴是人体必需的微量元素,含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用,请回答下列问题:
(1)Co基态原子的电子排布式为_____。
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。
①酞菁钴中三种非金属原子的电负性有大到小的顺序为_________ (用相应的元素符号作答) ;碳原子的杂化轨道类型为__________;
②与钴离子通过配位键结合的氮原子的编号是_____________。

(3)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的氧原子有______个;已知在该钴的氧化物晶体中钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,则在该钴的氧化物晶体中原子的空间利用率为____(用含a、b的式子表示)。

(4)筑波材料科学国家实验室 一个科研小组发现了在5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图中,不能描述CoO2的化学组成的是_______。
 。
。
-
铜单质及其化合物在很多领域有重要的用途.
(一)如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如下:

 中的配体是_______________________ 。
中的配体是_______________________ 。
(2)氯化亚铜 的制备过程是:向
的制备过程是:向 溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀,反应的离子方程式为_______________________________________________________ 。
溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀,反应的离子方程式为_______________________________________________________ 。
(二)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.
(1)与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 _______________________  填元素符号
填元素符号 。
。
(2)往浓 溶液中加入过量较浓的
溶液中加入过量较浓的 直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的
直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的 并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色晶体是____________________(写化学式),实验中所加
并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色晶体是____________________(写化学式),实验中所加 的作用是________________________。
的作用是________________________。
(3) 晶体中呈正四面体的原子团是______ ,杂化轨道类型是
晶体中呈正四面体的原子团是______ ,杂化轨道类型是 杂化的原子是____________。
杂化的原子是____________。
-
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中,CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
⑴超细铜粉的某制备方法如下:
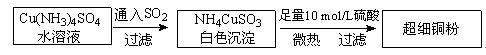
①[Cu(NH3)4]SO4中所含的化学键有________、________、________,
N、O、S三种元素的第一电离能大小顺序为:________>________>________。(填元素符号)
②NH4CuSO3中的金属阳离子的核外电子排布式为:________。
③ NH3分子中N原子的杂化方式为:________。
④与SO2互为等电子体的分子有________(写一种)。
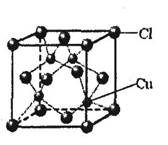
⑵氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通人一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀。
①CuCl的晶胞结构如下图所示,其中Cl原子的配位数为_________。
②CuCl的熔点比CuO的熔点________。(填“高”或“低”)
-
前四周期的元素及其化合物在生产、生活、化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式_________________,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有______种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是_______。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒_______________(分子或离子);
②硫氰酸分子中π键和σ键的个数之比为___________;
(4)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 ______ (填元素符号)
| 元素 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
②根据价层电子对互斥理论,预测ClO4-的空间构型为_______形,C1O2- 中Cl原子的杂化方式为_________。
③元素C、O、F、H的电负性由大到小的顺序为______________________。
-
Z、Y、X、W、V是原子序数依次增大的五种常见元素。X元素是地壳中含量最多的元素,Y、Z组成的气态化合物M的水溶液呈碱性,W的单质在X2中燃烧产物可使品红溶液褪色,V是一种历史悠久、应用广泛的金属元素。请回答:
(1)Y元素在周期表中的位置是 ;M的分子空间构型为 形,M是 分子(“极性”或“非极性”)
(2)写出X、Z两种元素组成的化合物Z2X2的结构式: 。
(3)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且反应属于氧化还原反应,请写出该反应的化学方程式 。
(4)X、Y、Z三种元素可组成一种强酸U,M与U反应生成一种盐K,写出K中含有的化学键类型 。
(5)若将V金属投入到盐酸溶液中,生成了浅绿色溶液N。N的酸性溶液与双氧水反应的离子方程式: 。
-
柔性电子产品因具有独特的柔性、延展性等优点在信息、医疗、能源等领域具有广泛应用前景。下图为中科院张新波课题组受中国传统书法艺术启发,直接将用毛笔书写后的纸张和锂箔作为电极材料组装成的锂空气电池。下列说法不正确的是( )
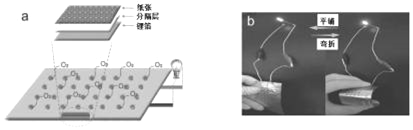
A. 纸张电极是该电池的正极
B. 锂箔电极发生的电极反应:Li﹣e-=Li+
C. 电池工作时,电子从锂箔电极经导线流向纸张电极,再从纸张电极经电解质溶液流向锂箔电极
D. 该电池具有轻型、柔性且可折叠的特点,有望应用于柔性电子器件
-
柔性电子产品因具有独特的柔性、延展性等优点在信息、医疗、能源等领域具有广泛应用前景。下图为中科院张新波课题组受中国传统书法艺术启发,直接将用毛笔书写后的纸张和锂箔作为电极材料组装成的锂空气电池。下列说法不正确的是( )
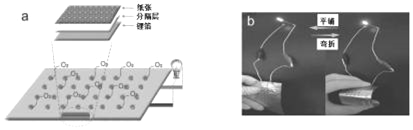
A. 纸张电极是该电池的正极
B. 锂箔电极发生的电极反应:Li﹣e-=Li+
C. 电池工作时,电子从锂箔电极经导线流向纸张电极,再从纸张电极经电解质溶液流向锂箔电极
D. 该电池具有轻型、柔性且可折叠的特点,有望应用于柔性电子器件
-
闪烁着银白色光泽的金属钛(22Ti)因具有密度小、强度大、无磁性等优良的机械性能,被广泛应用于军事、医学等领域,号称“崛起的第三金属”。已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是
A. 上述钛原子中,中子数不可能为22
B. 钛元素在周期表中处于第四周期
C. 钛的不同同位素在周期表中处于不同的位置
D. 钛元素是d区的过渡元素
-
闪烁着银白色光泽的金属钛(22Ti)因具有密度小、强度大、无磁性等优良的机械性能,被广泛应用于军事、医学等领域,号称“崛起的第三金属”。已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是
A. 上述钛原子中,中子数不可能为22
B. 钛元素在周期表中处于第四周期
C. 钛的不同同位素在周期表中处于不同的位置
D. 钛元素是d区的过渡元素





 。
。



