-
纯碱是重要的化工原料
(一)制备探究:如图是工业生产纯碱的主要流程示意图.
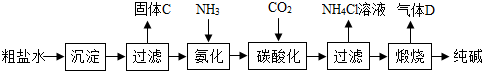
[查阅资料]
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式: 。
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是 ,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式 。
(3)“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热NH4Cl溶液,再加入熟石灰获得循环使用的物质是 ;
(4)煅烧制得纯碱的化学方程式是 。
(二)成分探究
[提出问题]纯碱样品中含有哪些杂质?
[猜想]
猜想一:可能含有NaHCO3; 猜想二:可能含有NaCl;猜想三:NaHCO3和NaCl
[实验探究]确定纯碱中是否含NaHCO3.实验装置和主要实验步骤如下:

①称量D、E装置总质量为200.0g,检查装置的气密性,将10.6 g纯碱试样放入锥形瓶中,按上图组装仪器,进行如下操作 ,后缓缓鼓入一段时间空气;
②按一定要求正确操作后,加入足量稀硫酸,待锥形瓶中不再产生气泡时,再次打开止水夹K1,从导管a处再次缓缓鼓入空气;
③一段时间后再次称量装置D、E的总质量为204.84g.
[实验讨论]
(5)步骤①中“如下操作”是指 ;
(6)装置B中一定发生的化学反应方程式为: ;
(7)装置B中生成CO2的质量为4.84g,通过计算说明纯碱中 含NaHCO3(填字母)。(写出计算过程)
A.一定 B.一定不 C.可能 D.无法确定
(8)另取10.6 g样品,加入a g 14.6%的盐酸恰好完全反应,再将所得溶液蒸干后得到固体的质量为W,当W的值满足 条件时,样品中含有NaCl。
-
纯碱是重要的化工原料
(一)制备探究:如图是工业生产纯碱的主要流程示意图.
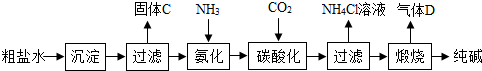
[查阅资料]
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式: 。
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是 ,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式 。
(3)“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热NH4Cl溶液,再加入熟石灰获得循环使用的物质是 ;
(4)煅烧制得纯碱的化学方程式是 。
(二)成分探究
[提出问题]纯碱样品中含有哪些杂质?
[猜想]
猜想一:可能含有NaHCO3; 猜想二:可能含有NaCl;猜想三:NaHCO3和NaCl
[实验探究]确定纯碱中是否含NaHCO3.实验装置和主要实验步骤如下:
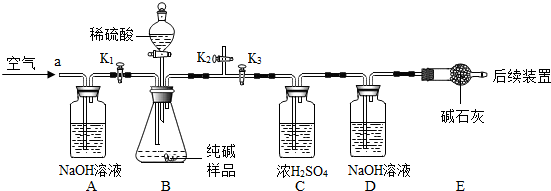
①称量D、E装置总质量为200.0g,检查装置的气密性,将10.6 g纯碱试样放入锥形瓶中,按上图组装仪器,进行如下操作 ,后缓缓鼓入一段时间空气;
②按一定要求正确操作后,加入足量稀硫酸,待锥形瓶中不再产生气泡时,再次打开止水夹K1,从导管a处再次缓缓鼓入空气;
③一段时间后再次称量装置D、E的总质量为204.84g.
[实验讨论]
(5)步骤①中“如下操作”是指 ;
(6)装置B中一定发生的化学反应方程式为: ;
(7)装置B中生成CO2的质量为4.84g,通过计算说明纯碱中 含NaHCO3(填字母)。(写出计算过程)
A.一定 B.一定不 C.可能 D.无法确定
(8)另取10.6 g样品,加入a g 14.6%的盐酸恰好完全反应,再将所得溶液蒸干后得到固体的质量为W,当W的值满足 条件时,样品中含有NaCl。
-
碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用,我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界技术的发展。
(查阅资料)①生产原料粗盐中含有少量可溶性杂质(MgCl2 和 CaC12)及不溶性杂质。
②氨气极易溶于水,二氧化碳能溶于水。
③生产原理:NaCl + NH3 + CO2+ H2O = NaHCO3↓+ NH4C1,分离得晶体 A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是 NH4Cl===NH3↑+HCl↑。
⑤部分生产流程如下图所示:

(问 题讨论)
(1)溶液 A 中的溶质为 ________,流程中加入适量盐酸的作用是 ________。
(2)反应(2)中为提高产率,所通入气体的顺序是 ________(填字母序号).
A.先通入 CO2 再通入 NH3 B.先通入 NH3 再通入 CO2
(3)上述生产流程中可循环使用的是 ________(填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(组成确定)
(1)称取一定质量的纯碱样品,多次充分加热,称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀 HNO3,再滴加 AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 ________(写化学式).
(含量测定) 同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下三组实验。甲组:取 12.0g 纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。将反应所得溶液小心蒸发,并将所得物质干燥、冷却至室温称得固体质量为 13.1g.样品中碳酸钠的质量分数为________。
乙组:取 12.0g 纯碱样品,利用下图所示装置,测出反应装置 C 增重了 4.1g(所加试剂均足量,每一步都反应完全).实验结束,发现乙组测定的质量分数偏小,其原因是_________。
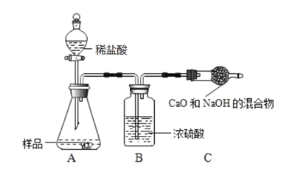
丙组:取 12.0g 的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀过滤、 洗涤、烘干称量固体质量,从而计算出碳酸钠的质量分数。组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是 ________。
-
我国制碱工业的先驱侯德榜发明了将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献,其生产工艺流程示意图如图:

(查阅资料)粗盐中含有CaCl2、MgCl2等可溶性杂质。
(1)粗盐水精制的过程中先加过量的NaOH溶液,发生反应的化学方程式是_____________;再加入过量的碳酸钠溶液,其目的是除尽__________(填名称)。
(2)煅烧后的产物X 是一种盐,写出其化学式:__________。
(3)Y是滤液中的主要成分,可作氮肥,但不能与碱性物质混合施用,原因是________________。
(4)该流程中可用于循环使用的物质有氨气和__________(填名称)。
-
我国制碱工业的先驱侯德榜发明了将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献,其生产工艺流程示意图如图:
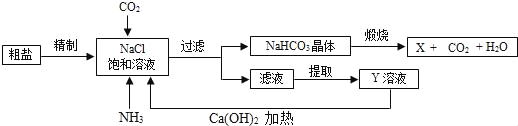
(查阅资料)粗盐中含有CaCl2、MgCl2等可溶性杂质。
(1)粗盐水精制的过程中先加过量的NaOH溶液,发生反应的化学方程式是_____________;再加入过量的碳酸钠溶液,其目的是除尽__________(填名称)。
(2)煅烧后的产物X 是一种盐,写出其化学式:__________。
(3)Y是滤液中的主要成分,可作氮肥,但不能与碱性物质混合施用,原因是________________。
(4)该流程中可用于循环使用的物质有氨气和__________(填名称)。
-
我国制碱工业的先驱侯德榜发明了将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献,其生产工艺流程示意图如图:
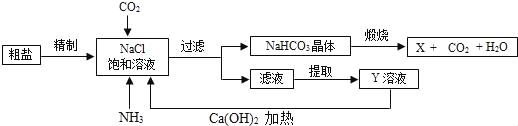
(查阅资料)粗盐中含有CaCl2、MgCl2等可溶性杂质。
(1)粗盐水精制的过程中先加过量的NaOH溶液,发生反应的化学方程式是_____________;再加入过量的碳酸钠溶液,其目的是除尽__________(填名称)。
(2)煅烧后的产物X 是一种盐,写出其化学式:__________。
(3)Y是滤液中的主要成分,可作氮肥,但不能与碱性物质混合施用,原因是________________。
(4)该流程中可用于循环使用的物质有氨气和__________(填名称)。
-
某校化学兴趣小组参观制碱厂后,获得以下信息井对相关问题进行研究。
【查阅资料】
①无水硫酸铜是白色固体,吸水变蓝。
②生产原料粗盐中含有少量可溶性杂质(MgCl2和CaC12)及不溶性杂质。
③生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4C1。分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是NH4Cl===NH3↑+HCl↑。
⑤部分生产流程如下图所示:
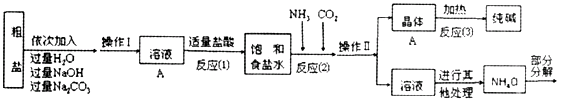
【问题讨论】
(1)①溶液A中的溶质有NaCl和__________、______________。
②操作Ⅱ的名称为___________。
③写出加入NaOH溶液所发生反应的化学方程式___________。
④流程中Na2CO3溶液的作用是除去粗盐中的___________。
(2)上述生产流程中可循环使用的是___________ (填序号)。
A.NH3 B. NaOH C. HCl D .CO2
【组成探究】
(3)①晶体A受热分解的化学方程式为 ________________________。
②设计实验检验纯碱样品中是否混有晶体A,请完成下表(从下列装置中选择):

| 选择的装置 | 实验现象 | 实验结论 |
| ________ | ________ | 样品不含晶体A |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。产生沉淀的方程式为_______________,由此确定纯碱样品含有杂质NaCl。
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
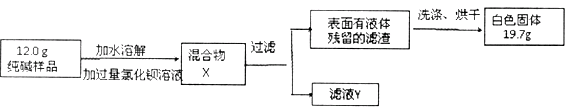
①氯化钡溶液过量的目的是___________________。
②判断滤渣是否洗干净,可向最后的洗出液中滴加________,然后观察现象判断。
A.氯化钡溶液 B.稀硫酸 C.稀盐酸 D.碳酸钾溶液
③根据实验数据,计算样品中碳酸钠的质量分数为__________。(精确到0. 1 % )
-
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
查阅资料:
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵.
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示
氯化铵分解的化学方程式是NH4Cl═NH3↑+HCl↑
<资料4>生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离的晶体A,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为______ Na2CO3+H2O+CO2↑.
-
(14分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。
【查阅资料】
①该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵。
②生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质。
③生产原理:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体A,并使其充分受热,即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为________。
④氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑。
⑤部分生产流程如下图所示:
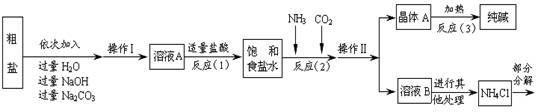
【问题讨论】
(1)溶液A中的溶质有NaCl和________、________,操作Ⅱ的名称为________。
(2)上述流程中NaOH溶液的作用是除去粗盐中的________。
(3)写出加入Na2CO3溶液所发生反应的化学方程式________。
(4)上述生产流程中可循环使用的是________(填序号)。
A.CO2 B.NH3 C.HCl D.NaOH
(5)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠:
【组成确定】
称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。
(6)由上述实验可确定纯碱样品含有杂质________(写化学式)。
【含量测定】
同学们为了测定该纯碱样品的纯度(假定只有(6)中的杂质),设计了如下实验:
(7)甲组实验:取10.0 g纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。充分加热蒸发所得物质并干燥、冷却至室温后称量,所得固体质量为10.9 g。计算样品中碳酸钠的质量分数为(写出计算过程,结果保留一位小数)。________
(8)乙组实验:取10.0 g纯碱样品,利用右图所示装置,测出反应后装置C增重了3.5g(所加试剂均足量)。实验结束后,发现乙组测定的碳酸钠质量分数偏小,其原因是________。
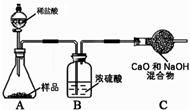
-
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵.
②生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
③生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离得晶体A,并使其充分受热,即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为______ Na2CO3+CO2↑+H2O














