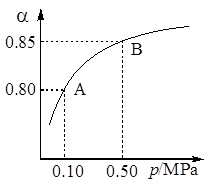-
二氧化硫是高中化学重点学习的三大气体之一,它是一种大气污染物,同时也是一种重要的化工原料。

(1)某化学兴趣小组采用图1所示装置制取并探究SO2气体的某些性质。
①下列实验方案能用图1所示装置制取所需SO2的是__________(填序号)„
A.铜与浓硫酸 B.固体硫在纯氧中燃烧
C.Na2SO3溶液与HNO3溶液 D.Na2SO3固体与浓硫酸
②验证c中生成SO2的实验方案:向试管d中加入_____后,打开活塞b,反应开始,待d中溶液________后,再______(填实验操作)d中的溶液,溶液________(填实验现象),则说明气体是SO2。
③图1所示装置存在一个明显的缺陷,请用文字说明改进方案:______________。
(2)在图1装置的d试管中加入BaCl2溶液,实验后发现d中有白色沉淀生成。为了探究沉淀的组成,该兴趣小组向d中加入过量稀盐酸,发现沉淀不溶解,你认为该沉淀物是____________,形成该沉淀的主要原因是__________________。为了进一步验证沉淀产生原因,该兴趣小组另取BaCl2溶液并加热煮沸。冷却后及时加入少量苯进行液封,然后再通入SO2,结果发现沉淀量减少,但仍有轻微浑浊产生,该兴趣小组改用图2制气装置再进行实验,结果发现d中没有出现浑浊。
下列气体可作为气体X的是________ (填序号,不定项选择)
A.CO2 B.NH3 C.O3 D.N2 E.NO2
⑶SO2通常作为保护剂添加到葡萄酒,有杀菌、抗氧化、改善风味和增酸的作用,但吸入过量的SO2对人体有害。我国国家标准规定葡萄酒中SO2的最大使用量为0.25g·L-1。图3(固定装置略)为该兴趣小组对葡萄酒中的SO2进行收集与含量测定的装置。
①冷凝管中水的进口为_________(填“e”或“f”)。
②g中加人300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与h中H2O2完全反应,反应的化学方程式为________________。
-
SO2是高中化学重点学习的三大气体之一,是常见的大气污染物之一,同时也是重要的工业原料,探究其制备方法和性质具有非常重要的意义,请回答下列问题。
Ⅰ.某研究小组将纯净的SO2气体通入0.5 mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-;假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
| 实 验 步 骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的10 mL 0.5 mol/L BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体。 | ______ | 假设一 成立 |
| 实验2:在盛有不含O2的10 mL 0.5mol/L Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体。 | ______ |
②设计实验一的目的是________________。
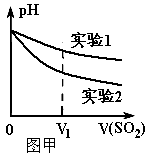
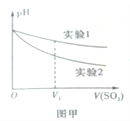
(2)为深入研究该反应,该小组还测得上述两个实验中溶 液的pH随通入SO2体积的变化曲线如图甲。实验2中溶液pH小于实验1的原因是(用离子方程式表示)___________________。
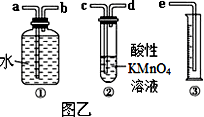
Ⅱ.我国规定空气中SO2含量不得超过0.02 mg/L。某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
(1)若原料气从左向右流,上述装置连接的顺序是:原料气→_______________(用字母和箭头表示)。当装置②中出现______现象时,立即停止通气。
(2)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是________。
A.NaOH溶液 B.溴水
C.氨水 D.BaCl2溶液
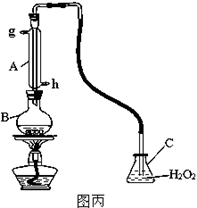
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定。
(1)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00ml,该葡萄酒中SO2含量为__________g/L。
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________。
-
SO2是高中化学重点学习大三大气体之一,是常见的大气污染物之一,同时有是重要的工业原料,探究其制备方法和性质具有非常重要的意义,请回答下列问题。
Ⅰ.某研究小组将纯净的SO2气体通入0.5mol/L的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一
①请在下表空白处填写相关实验现象。
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | ____ | 假设一成立 |
| 实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | ____ |
②设计实验1的目的是_________。
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲所示。实验2中溶液pH小于实验1的原因是(用离子方程式表示)_________。
Ⅱ.我国规定空气中SO2含量不得超过0.02mg/L。某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量(已知碘能氧化H2SO3,生成H2SO4)。

(1)若原料气从左向右流时,上述装置连接的顺序是:原料气→______ (用字母和箭头表示)。当装置②中出现_______现象时,立即停止通气。
(2)你认为下列试剂中,可以用来代替试管中的酸性KMnO4溶液的是________。(填字母代号)
A.NaOH溶液 B.溴水 C.氨水 D.BaCl2溶液
Ⅲ.中华人民共和国国家标准规定葡萄酒中SO2最大使用量为0.25g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行定性测定。
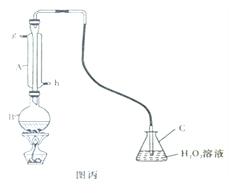
(1)B中加入250.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0900mol/L NaOH标准溶液进行滴定,滴定终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为_______g/L。
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施____。
-
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一。
(1) 新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,其吸收的化学反应方程式为________再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(只要求写一种)。
(2) 工业上生产硫酸时,将SO2氧化为SO3是关键一步。
① 某温度下,SO2(g)+1/2O2(g) SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时混合气体的总物质的量为8.0mol,该温度下平衡常数K=________。
SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时混合气体的总物质的量为8.0mol,该温度下平衡常数K=________。
② 一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g)达到平衡后改变下述条件,SO3的体积分数变大的是________
2SO3(g)达到平衡后改变下述条件,SO3的体积分数变大的是________
A、保持温度和容器压强不变,充入2mol SO3
B、保持温度和容器体积不变,充入2mol N2
C、保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2
D、升高温度
E、移动活塞压缩气体
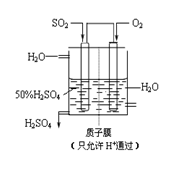
(3) 某人设想以如图所示装置用电化学原理生产硫酸,通入O2的一极的电极为________极; 写出通入SO2的电极的电极反应式:________。
-
二氧化硫为无色气体,有强烈刺激性气味,是大气主要污染物之一。某化学兴趣小组欲制备并探究SO2的某些性质。
【SO2的制备】用亚硫酸钠与较浓的硫酸反应制备SO2的装置图如下(夹持仪器省略):
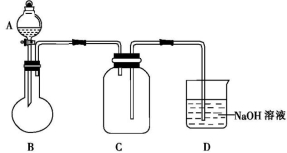
(1)图中的装置错误的是 ;B中发生反应的化学方程式为 ;D的作用是 。
【SO2的性质】探究SO2气体性质的装置如图所示:
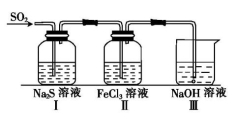
(2)装置Ⅰ中的现象是 ,说明SO2具有 (填“氧化”或“还原”)性。
写出装置Ⅰ中通入足量SO2的离子方程式 。
(3)在上述装置中通入过量的SO2,为了验证Ⅱ中发生了氧化还原反应,取Ⅱ中溶液分成两份,
并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案二:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的方案是 ,原因是 ,写出解释该原因的离子方程式 。
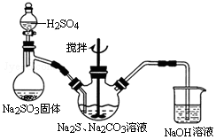
(4) SO2可以用来制备硫代硫酸钠,硫代硫酸钠可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.实验室可通过Na2S、Na2CO3和SO2共同反应来制取Na2S2O3。写出如图所示装置中三颈瓶中由反应制取Na2S2O3的化学方程式
-
(13分)二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一。
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中________能导致光化学烟雾的形成;
目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化。如:CO(g)+NO2(g) NO(g)+CO2(g) △H=-akJ·mol—1(a>0)2CO(g)+2NO2(g) N2(g)+2CO2(g) △H=-bkJ·mol—1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为mol,放出的热量为________kJ(用含有a和b的代数式表示)。
⑵新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(只要求写一种)。
(3)工业上生产硫酸时,将SO2氧化为SO3是关键一步。
①某温度下,SO2(g)+1/2O2(g) SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=________。
SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=________。
②一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是________
2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是________
A.保持温度和容器压强不变,充入2mol SO3
B.保持温度和容器体积不变,充入2mol N2
C.保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2
E.升高温度 F.移动活塞压缩气体
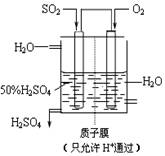
(4)某人设想以右上图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:________
________。
-
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中______能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.如:
CO(g)+NO2(g)═NO(g)+CO2(g)△H=-akJ•mol-1(a>0)
2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-bkJ•mol-1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为______mol,放出的热量为______kJ(用含有a和b的代数式表示).
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏.写出有关的化学反应方程式______.
(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g) 2SO3(g)△H=-196.kJ•mol-1
2SO3(g)△H=-196.kJ•mol-1
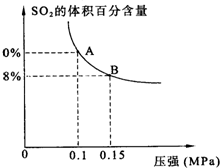
某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系______(填“吸收”或“释放”)能量.
②将5molSO2和7molO2通入10L密闭容器中,平衡时体系的总压强为0.1MPa.该反应在该温度下的平衡常数等于______.
-
为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了图1所示的实验装置。
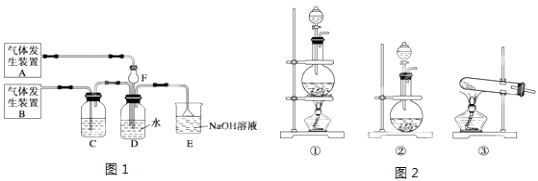
(1)该化学兴趣小组同学为制取Cl2和SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。请写出制取Cl2的离子方程式: 。
(2)在此实验中,F仪器的作用是:______________;发生装置B应选择图2三种装置中的___________(填序号)。
(3)D装置中主要反应的离子方程式为 。
(4)为验证通入D装置中过量的气体是Cl2还是SO2气体,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰酸钾溶液 ④品红溶液 ⑤溴水 ⑥稀硝酸
A.若Cl2过量:取适量D中溶液滴加至盛有试剂的试管内,发生的现象是: ;(试剂可以多选,请填试剂的序号,下同)。
B.若SO2过量:取适量D中溶液滴加至盛有试剂的试管内,发生的现象是: 。
-
一氧化碳、二氧化硫和氮的氧物是重要的化工原料,但也是大气的主要污染物,综合治理其污染是环境化学当前的重要研究内容之一.
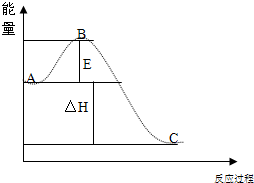
(1)硫酸生产中,SO2催化生成SO3:2SO2(g)+O2(g)═2SO3(g),反应过程的能量变化如图所示.
①图中A表示______.
②该反应通常用V2O5作催化剂,加V2O5对图中E的大小有何影响?______(填“增大”、“降低”、“没有”).
③在一定条件下,将0.100molSO2(g)和0.060molO2(g)放入容积为2L的密闭容器中,反应达到平衡时,测得c(SO3)=0.04mol/L.则该条件下反应的平衡常数K=______.
(2)一定条件下,氢气与一氧化碳按一定比例可生成洁净能源甲醇(CH3OH),则:
①n(H2):n(CO)=______.
②甲醇高效燃料电池是以CH3OH为燃料,O2为氧化剂,KOH为电解质组成.该电池放电时,负极反应式为:______.
(3)汽车尾气是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使CO和NO反应,生成可参与大气生态循环的无毒气体.
①写出一氧化碳与一氧化氮反应的化学方程式:______.
②用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△=-574kJ/mol
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△=-1160kJ/mol
若用标准状况下6.72LCH4还原NO2到N2,整个过程中转移电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ.
-
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3: 2SO2(g)+O2(g) 2SO3(g)。某温度下,SO2的平衡转化率( α)与体系总压强(p)的关系如图所示。根据图示回答下列问题:
2SO3(g)。某温度下,SO2的平衡转化率( α)与体系总压强(p)的关系如图所示。根据图示回答下列问题:
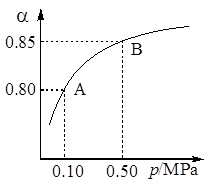
①将2.0 mol SO2和1.0 mol O2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。该反应的平衡常数等于____________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g);DH =-574 kJ/mol
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g);DH =-1160 kJ/mol
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为_____________(阿伏加德罗常数的值用NA表示),放出的热量为_________kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M = Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:

请写出MFe2Ox分解SO2的化学方程式______________________________________(可不配平)。