-
铁及其化合物在工农业生产和生活中有广泛应用.
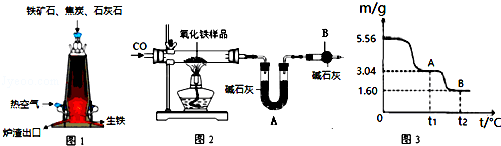
(1)图1为高炉炼铁示意图.从炉底流出的生铁属 (填“金属单质”或“合金”).
下列作用中①与铁矿石发生反应生成铁 ②燃烧供热 ③除去铁矿石中少量杂质(如SiO2)④生成CO,属于从炉顶加入焦炭的作用有 (填字母).
A.①② B.①③ C.②③ D.②④
(2)实验室可用图2装置模拟工业炼铁并测定样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不与CO反应)
【查阅资料】碱石灰能吸收二氧化碳和水蒸气
【问题讨论】装置B的作用是 ,从环保角度看该实验装置有一明显缺陷是: .
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量A装置增重4.4g.则 样品中氧化铁质量分数为 %.
【实验反思】当观察到反应管中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数 (填“偏大”,“偏小”,“无影响”)
(3)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),用于制备动物饲料硫酸亚铁的流程如下:
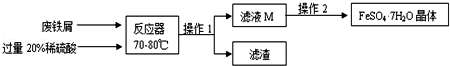
①反应器中发生的反应除了Fe2O3+3H2SO4=Fe2(SO4)3+3H2O和Fe+Fe2(SO4)3=3FeSO4外,还有 ;
②滤液M的溶质有 ,操作2为 ;
③FeSO4的溶解度和析出组成如下表.在操作2中,析出FeSO4•7H2O晶体的最高温度不超过 ℃.
| 温度t/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度S/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O |
| | | | | | | | | | |
(4)5.56g硫酸亚铁晶体(FeSO4•xH2O)隔绝空气受热分解时,生成金属氧化物和气体.固体产物的质量随温度变化的曲线如图3所示.
①0~t1℃,发生的变化是加热失去结晶水,x= ;
②t2℃时B点固体组成只有一种,化学式为 .
-
(17分)钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的
生铁的质量是多少?

Ⅱ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
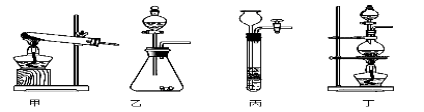
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑
后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现
固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:

根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| 玻璃管质量] | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 |
| 反应前 | 28.20 g | 33.00 g] | 300.0 g |
| 反应后 | 32.84 g | 300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
-
(2010•沈阳)钢铁是人类生产生活中应用最广泛的金属材料,下图是炼铁高炉的结构示意图,请回答下列与此有关的问题.
(1)根据矿石的主要成分分析,下列矿石中最适合炼铁的是______.
A、磁铁矿(主要成分Fe3O4)
B、黄铁矿(主要成分FeS2)
C、菱铁矿(主要成分FeCO3)
D、赤铜矿(主要成分Cu2O)
(2)请写出以赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式:______ 2Fe+3CO2
-
钢铁是人类生产生活中应用最广泛的金属材料。下图是炼铁高炉的结构示意图,请回答下列与此有关的问题;

(1)根据矿石的主要成分分析,下列矿石中最适合炼铁的是 ;
A.磁铁矿(主要成分Fe3O4) B.黄铁矿(主要成分FeS2)
C.菱铁矿(主要成分FeCO3) D.赤铜矿(主要成分Cu2O)
(2)请写出以赤铁矿(主要成分为Fe2O3)为原料炼铁的化学方程式: ;
(3)在炼铁原料中使用焦炭的目的是 (答一点);
-
钢铁是人类生产生活中应用最广泛的金属材料,下图是炼铁高炉的结构示意图,请回答下列与此有关的问题.
(1)根据矿石的主要成分分析,下列矿石中最适合炼铁的是______.
A、磁铁矿(主要成分Fe3O4)
B、黄铁矿(主要成分FeS2)
C、菱铁矿(主要成分FeCO3)
D、赤铜矿(主要成分Cu2O)
(2)请写出以赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式:______ 2Fe+3CO2
-
金属在生产和生活中应用广泛.
(1)每年因金属锈蚀造成很大浪费,铁生锈的条件是________;废钢铁可回收重新冶炼,高炉炼铁中一氧化碳还原氧化铁的化学方程式为________.
(2)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:
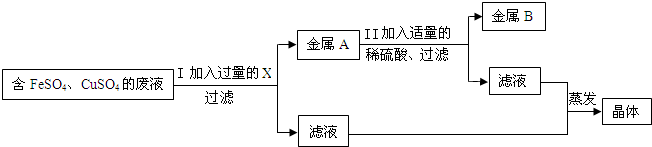
①写出Ⅰ中有关反应的化学方程式________.
②小红、小强同学在步骤Ⅰ中X能否改用锌的问题上产生了分歧.请你也参与他们的讨论,表明观点,并说明理由.________.
-
(2009•西城区一模)金属材料在生产、生活中应用广泛.
(1)下列铁制品中,利用金属导热性的是(填序号).

(2)联合钢铁工业的基本生产流程示意图如:
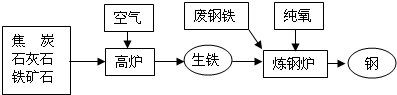
石灰石、生铁和钢均属于(填“纯净物”或“混合物”).生铁和钢的主要区别是.写出以赤铁矿(主要成分是氧化铁)为原料,用一氧化碳冶炼生铁的化学方程式为.
(3)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用氢气和氯化亚铁发生置换反应,生成“纳米铁”,反应的化学方程式为.
(4)氯化铁能腐蚀铜(2FeCl3+Cu=2FeCl2+CuCl2),工业上常用此原理生产印刷线路板.
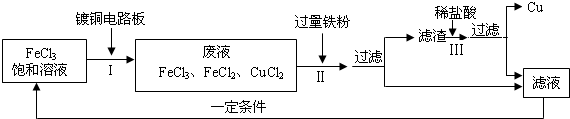
步骤Ⅱ中发生了两个反应:2FeCl3+Fe=3FeCl2和;滤渣的成分有.
-
金属单质及其合金是应用最广泛和最重要的工程材料.铁是应用最广泛的金属,炼铁原理的化学方程式为________.
实际应用中使用的生铁和________是含碳量不同的铁的两种合金.
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:___________________________;
(2)实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
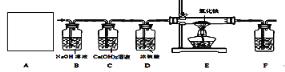
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的_________(填装置编号);
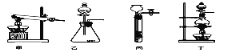
(2)图中装置C、D的作用分别是 ____________、_______________;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的_____________(填试剂名称),反应的化学方程式为 ______________________;
(4)该装置设计有一个明显缺陷,你认为是______________________________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:

根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;②_________ ③ ____________。
(6)定量分析 用电子天平称量得部分数据如下:
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 |
| 反应前 | 28.20 g | 33.00 g | 300.0 g |
| 反应后 | 32.84 g | 300.4 g |
根据上述数据,纯净的Fe2O3固体质量为_____________g,请选择有效的数据,推断出反应后黑色固体的成分(写出计算过程)__________________________。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:__________________________。
-
铁是生产生活中使用最广泛的一种金属,铁矿石冶炼成铁是一个复杂的过程。下图为高炉炼铁的示意图。
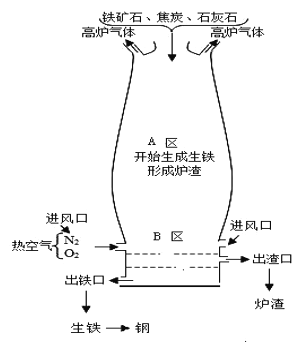
(1)根据图示写出在A区内生成铁的化学反应方程式____________。
(2)铁粉、活性炭、蛭石、无机盐和水等按一定的比例可制成暖宝宝。暖宝宝能够发热,主要是细微铁粉的功劳,利用铁生锈的原理,在工作过程中实现了由化学能转化为_____________能。
(3)生铁百炼而成钢。不锈钢由于其特殊的金属性能,制成的器皿美观耐用,因此不锈钢餐具广泛进入家庭。以下是关于不锈钢餐具使用的一些观点,你认同的是____________。
a.不锈钢餐具既不易碎又使用方便
b.不锈钢餐具不容易滋生细菌,但盛放热菜会烫手
c.不锈钢餐具可长时间盛放盐、酱油、醋、汤等













