-
(12分)非金属元素H、C、N、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛,完成下列各题。
(1)①O2-的核外电子排布式为 ,CS2的晶体类型为 晶体,其C的轨道杂化方式为 ;
②CH3OH在常温下为液态,沸点高于乙烷的主要原因是 ;
(2)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 | 
|
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用 。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于
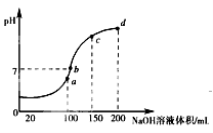
(3)室温时,向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
-
卤族元素是典型的非金属元素,其单质及其化合物具有广泛的用途。已知:KMnO4与浓盐酸常温下反应可生成氯气。根据所学化学知识及所给信息,回答下列有关问题:
(1)下列可以用来判断氯、溴、碘元素非金属性强弱的是 (填序号)。
①HCl、HBr、HI的热稳定性逐渐减弱;
②AgCl、AgBr、AgI的颜色逐渐加深;
③ HCl、HBr、HI的酸性依次减弱;
④ Cl2、Br2、I2的颜色逐渐加深;
⑤ Cl2、Br2、I2和H2反应条件由光照(或点燃)→ 一定温度→ 持续加热;条件由易到难;
⑥Cl2、Br2、I2的氧化性逐渐减弱。
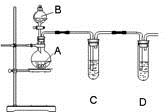
(2)某化学探究小组选用右图所示的装置和下列所给的试剂来证明非金属性:Cl>I,请你按照他们的设计思路完成该实验。
可供选择的试剂有:①浓盐酸,②硝酸银溶液,③KMnO4,④稀盐酸,⑤淀粉碘化钾溶液, ⑥MnO2, ⑦NaOH溶液;⑧浓硫酸
烧瓶A中应盛放的药品是 (填序号),试管C中应盛放的药品是 (填序号),则装置D的作用是 。观察到 现象,即可证明非金属性Cl>I。
(3)一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示。
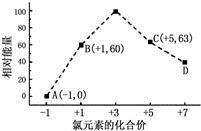
①D是 (填离子符号)。
②B→A+C反应的离子方程式为 ;生成1molC时, KJ的热(填吸收或放出以及具体数值)
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___________,氧化性最弱的简单阳离子是(填离子符号)___________。
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
①工业制镁时,电解MgCl2而不电解MgO的原因是______________;
②制铝时,电解Al2O3而不电解AlCl3的原因是_________________;
③写出电解Al2O3反应方程式 。
-
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是( )
a.HCl、HBr、HI水溶液的酸性
b.Cl2、Br2、I2的熔点
c.HCl、HBr、HI的热稳定性
d.Cl2、Br2、I2的氧化性
(3)工业上,通过如下转化可制得KCl03晶体:

②Ⅱ反应过程能析出KCIO3晶体而无其他晶体析出的原因是
(4)一定条件下,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。
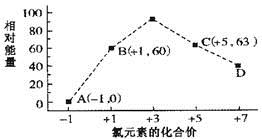
①D是_________(填离子符号)。
②B→A+c反应的热化学方程式为___________(用离子符号表示)。
-
第IIA族元素在地壳内蕴藏较丰富,其单质和化合物用途广泛。回答下列问题:
(1)基态Ca原子M能层有_______个运动状态不同的电子,Mn和Ca属于同一周期,且核外最外层电子构型相同,但金属Mn的熔沸点等都比金属Ca高,原因______。
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是_________,中心原子的杂化方式为_______。
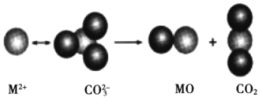
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3__________(填“高于”或“低于”)SrCO3,原因是_______。从成键轨道看,CO2分子内的化学键类型有________。
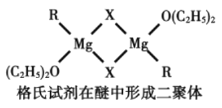
(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键__________。
-
铜是重要的过渡元素,其单质及化合物具有广泛用途。回答下列问题:
(1)铜元素基态原子的价电子排布式________________________________。
(2)铜能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。
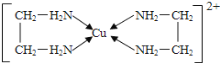
①Cu2+与乙二胺所形成的配离子中含有的化学键是_________________。
a.配位键 b.离子键 c. 键 d.
键 d. 键
键
②乙二胺分子中氮原子的杂化轨道类型为________________________,C、N、H三种元素的电负性由大到小顺序是________________________________。
③乙二胺和三甲胺[N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是_______________。
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是_____________________________。(请结合原子的性质进行回答)
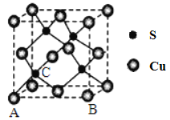
(4)Cu和S形成某种晶体的晶胞如图所示。
①该晶体的化学式为____________________
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为____________________。
③已知该晶体的密度为d g·cm-3,Cu2+和S2-的半径分别为a pm和b pm,阿伏加德罗常数值为NA。列式表示该晶体中原子的空间利用率______________。
-
砷 是第四周期ⅤA族元素,可以形成
是第四周期ⅤA族元素,可以形成 、
、 、
、 、
、 等 化合物,有着广泛的用途
等 化合物,有着广泛的用途 回答下列问题:
回答下列问题:
(1)写出砷的原子序数______________
(2)工业上常将含砷废渣 主要成分为
主要成分为 制成浆状,通入
制成浆状,通入 氧化,生成
氧化,生成 和单质硫
和单质硫 写出发生反应的化学方程式 _____________________________________________
写出发生反应的化学方程式 _____________________________________________  该反应需要在加压下进行,原因是 _______________________________________
该反应需要在加压下进行,原因是 _______________________________________
(3)已知: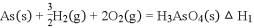

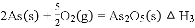
则反应 的
的 ________________________
________________________
(4) 时,将
时,将 、
、
 和20mL NaOH溶液混合,发生反应:
和20mL NaOH溶液混合,发生反应: 溶液中
溶液中 与反应时间
与反应时间 的关系如图所示.
的关系如图所示.
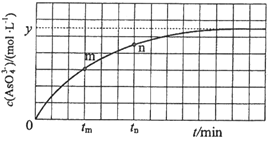
①下列可判断反应达到平衡的是 ______  填标号
填标号 .
.
 溶液的pH不再变化
溶液的pH不再变化 

 不再变化
不再变化 

② 时,
时, ______
______ 填“大于”“小于”或“等于”
填“大于”“小于”或“等于”
③ 时,
时, ______
______ 时
时 填“大于”“小于”或“等于”
填“大于”“小于”或“等于” ,理由是 ____________________
,理由是 ____________________
④若平衡时溶液的 ,则该反应的平衡常数K为 ______________
,则该反应的平衡常数K为 ______________
-
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1) 分子的晶体中,在晶胞的顶点和面心均含有一个
分子的晶体中,在晶胞的顶点和面心均含有一个 分子,则一个
分子,则一个 晶胞的质量为_______。
晶胞的质量为_______。
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是_____(填字母)。
a.晶体的熔点:干冰>冰
b.晶体中的空间利用率:干冰>冰
c.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的是______(填字母)。
a.金刚石中碳原子的杂化类型为 杂化,石墨中碳原子的杂化类型为
杂化,石墨中碳原子的杂化类型为 杂化
杂化
b.晶体中共价键的键长:金刚石中 <石墨中
<石墨中
C.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
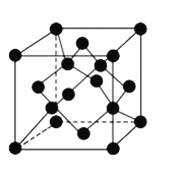
(4)金刚石晶胞结构如下图,立方 结构与金刚石相似,在
结构与金刚石相似,在 晶体中,
晶体中, 原子周围最近的
原子周围最近的 原子所构成的立体图形为_______,
原子所构成的立体图形为_______, 原子与
原子与 原子之间共价键与配位键的数目比为_______,一个晶胞中
原子之间共价键与配位键的数目比为_______,一个晶胞中 原子数目为___________。
原子数目为___________。
(5)已知 单质的晶体密度为
单质的晶体密度为 ,
, 的相对原子质量为
的相对原子质量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则
,则 的原子半径为_________。
的原子半径为_________。
-
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
(1)C60分子能与F2发生加成反应,其加成产物为______,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______
-
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
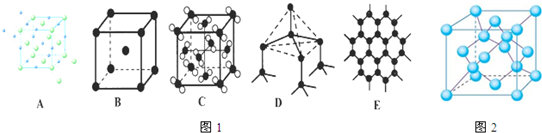
(1)如图1分别代表了五种常见的晶体,分别是:A______,B______,C______,D______,E______.(填名称或化学式)
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳的两种常见单质,下列叙述正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨 d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
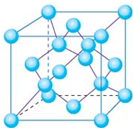
(4)金刚石晶胞结构如图2,一个晶胞中的C原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______









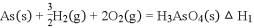
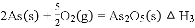
 溶液中
溶液中


