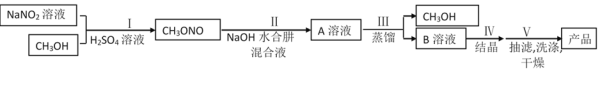-
水合肼(N2H4·H2O) 是一种强还原剂,沸点118.5℃,熔点-40℃,常温下为无色透明的油状液体,属于二元弱碱,在空气中可吸收CO2而产生烟雾。水合肼的制备装置如图。
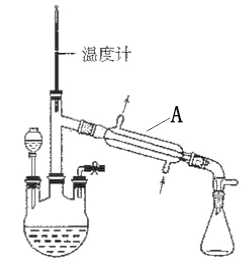
(1)装置A的名称为________________。向三颈烧瓶中加入溶液之前,应先从右侧导管中通入氮气,目的是______________________。
(2)水合肼可用含NaOH 的NaClO溶液氧化尿素[CO(NH2)2]溶液制得,反应的化学方程式为__________________。
(3)制备水合肼时,分液漏斗应盛装________(填标号)。理由是___________。
a.NaOH 和NaClO 混合溶液 b.CO(NH2)2 溶液
(4)弱酸性条件下水合肼可处理电镀废水,将Cr2O72-还原为Cr(OH)3沉淀而除去,水合肼被氧化为N2,该反应的离子方程式为_____________。常温下Ksp[Cr(OH)3]= 10-32,且当溶液中离子浓度小于10-5mol/L时可视作沉淀完全。则Cr3+沉淀完全时,溶液的pH=________。
(5)有同学认为该实验收集装置有缺陷。请你写出改进措施:______________。
-
N2H4·H2O(水合肼)极毒且不稳定,100℃以上易分解失水,常用作还原剂和除氧剂(通常生成N2和H2O),其熔点为-40℃,沸点118.5℃。现以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O和无水Na2SO3,其主要流程如下:
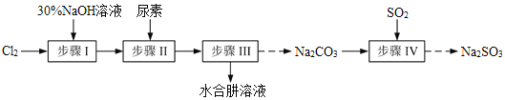
已知:Cl2(g)+2OH-(aq)=ClO-(aq)+Cl-(aq)+H2O(aq) △H<0
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒、烧杯外,还需要_____________(填标号)。
A.容量瓶 B.胶头滴管 C.玻璃棒 D.锥形瓶
(2)步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液充分反应生成NaClO3和NaCl。实验中为控制反应温度除了用冰水浴、充分搅拌外,还需采取的措施是_______________________。
(3)步骤Ⅱ合成N2H4·H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________(填字母);
a.尿素溶液 b.NaClO碱性溶液 c.尿素溶液或NaClO溶液任选其一
理由是____________________________________。
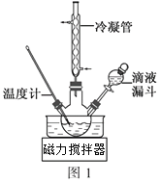
(4)步骤Ⅲ中分离出N2H4·H2O应该采用的方法最合理是____________________。
(5)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、HSO3-、SO32-随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示)。
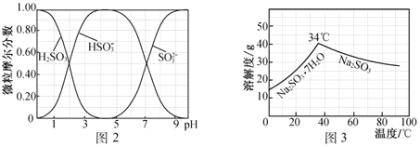
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的方法是______________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:_________________________________,用少量无水乙醇洗涤,干燥,密封包装。
(6)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
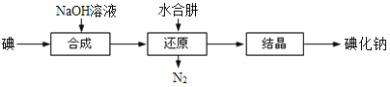
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是_______________________。
-
水合肼(N2H4·H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+2NH3===N2H4·H2O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
甲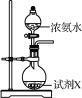 乙
乙 丙
丙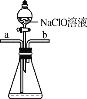 丁
丁
A. 装置甲中试剂X可以选择生石灰 B. 装置乙作为反应过程的安全瓶
C. 装置丙制备水合肼时氨气从b口进入 D. 装置丁可用于吸收多余的尾气
-
水合肼(N2H4·H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+2NH3===N2H4·H2O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
甲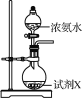 乙
乙 丙
丙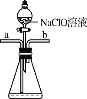 丁
丁
A. 装置甲中试剂X可以选择生石灰 B. 装置乙作为反应过程的安全瓶
C. 装置丙制备水合肼时氨气从b口进入 D. 装置丁可用于吸收多余的尾气
-
水合肼(N2H4·H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+2NH3===N2H4·H2O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
甲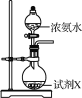 乙
乙 丙
丙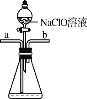 丁
丁
A. 装置甲中试剂X可以选择生石灰 B. 装置乙作为反应过程的安全瓶
C. 装置丙制备水合肼时氨气从b口进入 D. 装置丁可用于吸收多余的尾气
-
水合肼是一种重要的精细化工原料,纯品为无色透明的油状液体,在高温下分解成N2、NH3和H2.水合肼具有还原性,能与碘反应:N2H4+2I2═N2+4HI.在农药、医药及有机合成中有广泛用途.用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→N2H4•H2O+NaCl+Na2CO3
实验步骤:
步骤1.向30%的NaOH溶液中通入Cl2,保持温度在30℃以下,至溶液显浅黄绿色停止通Cl2.静置,检测NaClO的浓度后,倾出上层清液,配制所需浓度的NaClO和NaOH的混合溶液.
步骤2.称取一定质量尿素配成溶液,置于冰水浴.将一定体积步骤1配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,继续搅拌0.5h.
步骤3.将步骤2所得溶液,转移到三口烧瓶(见图甲)并加入5gKMnO4作催化剂,边搅拌边急速升温,在108℃回流5min.
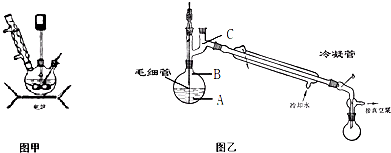
(1)步骤1中检测NaClO浓度的目的是______.步骤2中冰水浴的作用是______.
(2)粗产品倒入图乙的烧瓶中进行减压蒸馏.减压蒸馏的原理是______.在烧瓶中插入一根毛细管,通过蒸馏即可得到纯品.在减压蒸馏过程中毛细管的作用是______,温度计水银球放置的位置是______(填写图中A、B、C).
(3)测定水合肼的质量分数可采用下列步骤:
a.准确称取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液.
b.移取10.00mL于锥形瓶中,加入20mL水,摇匀.
c.用0.1000mol•L-1碘的标准溶液滴定至溶液出现微黄色且0.5min内不消失,记录消耗溶液的体积.
d.进一步操作与数据处理
①使用容量瓶前要先检漏并洗净,检漏的操作方法是______.
②滴定时,碘的标准溶液盛放在______滴定管中(填“酸式”或“碱式”);称取1.250g试样时所用的仪器是______.
③若本次滴定消耗碘的标准溶液为18.00mL,则产品中N2H4•H2O的质量分数为______.
④为获得更精确的滴定结果,步骤d中进一步的操作是______.
-
工业水合肼法制备叠氮化钠的工艺流程如图所示:
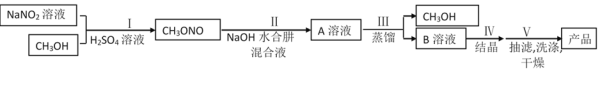
一、合成水合肼
己知: (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。
合成 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
(1)写出 的结构式____________,
的结构式____________, 的电子式____________
的电子式____________
(2)①写出制取 的离子方程式___________________________
的离子方程式___________________________
②实验中通过滴液漏斗滴加的溶液是_________理由是_______________图1使用冷凝管的目的是____________________________________
③从反应后的混合溶分离出 ,应该采用的分离方法最合理的是________。
,应该采用的分离方法最合理的是________。
二、合成叠氮化钠( )晶体
)晶体
已知:相关物质的物理性质如下表
| 熔点℃ | 沸点℃ | 溶解性 |
| 
| -97 | 67.1 | 与水互溶 |
| 水合肼( ) ) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| 亚硝酸甲酯( ) ) | -17 | -12 | 溶于乙醇、乙醚 |
| NaN3 | | | 与水互溶,不溶于乙醚、微溶于乙醇 |
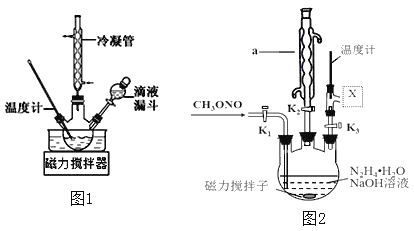
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是________________。(写出1点即可)
②图中 处连接的最合适装置应为下图中的__________。
处连接的最合适装置应为下图中的__________。
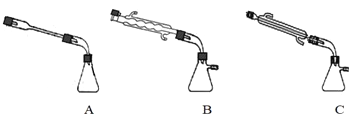
③步骤Ⅱ中制备叠氮化钠的操作是________(填序号)步骤Ⅲ中溶液 进行蒸馏的合理操作顺序是_______。(填序号)
进行蒸馏的合理操作顺序是_______。(填序号)
①打开 ,关闭
,关闭 ②打开
②打开 ③加热 ④关闭
③加热 ④关闭
(4)步骤Ⅳ对溶液 加热蒸发至溶液体积的
加热蒸发至溶液体积的 ,
, 结晶析出。步骤Ⅴ可以用________洗涤晶体。
结晶析出。步骤Ⅴ可以用________洗涤晶体。
A.水 B.乙醚 C.乙醇水溶液 D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
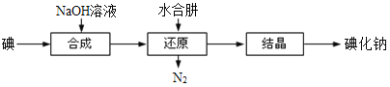
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是______________________________________。
-
水合肼(N2H4·H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:
CO(NH2)2+2NaOH+NaC1O==N2H4·H2O+Na2CO3+NaCl。
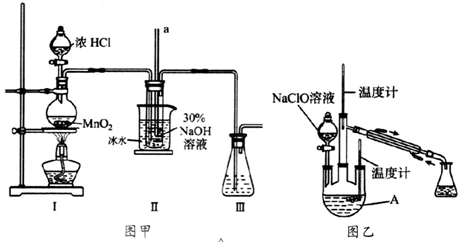
实验1:制备NaClO溶液。(已知:3NaClO 2NaCl+NaClO3)
2NaCl+NaClO3)
(1)图甲装置I中烧瓶内发生反应的化学方程式为_______________________。
(2)用NaOH固体配制溶质质量分数为30%NaOH溶液时,所需玻璃仪器除量筒外还有________________。(填标号)
a.烧杯 b.容量瓶 c.玻璃棒 d.烧瓶
(3)图甲装置Ⅱ中用冰水浴控制温度的目的是_________________。
实验2:制取水合肼。
(4)图乙中若分液漏斗滴液速度过快,部分N2H4·H2O会参与A中反应并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式:________________________。充分反应后,蒸馏A中溶液即可得到水合肼的粗产品。
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15 mol·L-1的碘的标准溶液滴定。(已知:N2H4·H2O+2I2==N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在________(填“酸式”或“碱式”)滴定管。
②下列能导致馏分中水合肼的含量测定结果偏高的是_________。(填标号)
a.锥形瓶清洗干净后未干燥
b.滴定前,滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后俯视
d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为_______________________。
-
水合肼(N2H4·H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂,利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=Na2CO3+ N2H4·H2O +NaCl
实验一:制备NaClO溶液。(实验装置如右图所示)
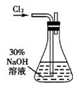
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是 。
(3)设计实验方案:用中和滴定原理测定反应后锥形瓶中剩余NaOH的浓度(实验提供的试剂:H2O2溶液、FeCl2溶液、0.10 mol·L-1盐酸、酚酞试液): 。
实验二:制取水合肼。(实验装置如右图所示)
(4)控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。分液漏斗中的溶液是 (填标号)。A.CO (NH2) 2溶液 B.NaOH和NaClO混合溶液原因是: (用化学方程式表示)。
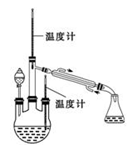
实验三:测定馏分中肼含量。
(5)称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.10mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4·H2O + 2I2 = N2↑+ 4HI + H2O)
①滴定时,碘的标准溶液盛放在 (填“酸式”或“碱式”)滴定管中;本实验滴定终点的现象为 。
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 。
-
水合肼(N2H4·H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaC1O=Na2CO3+N2H4·H2O+NaCl
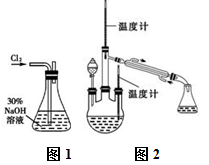
实验一:制备NaClO溶液。(实验装置如图1所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有______(填标号)。
A.玻璃棒 B.烧杯 C.烧瓶 D.容量瓶 E.胶头滴管
(2)锥形瓶中发生反应的离子方程式是___________________。
实验二:制取水合肼。(实验装置如图2所示)
(3)①仪器A的名称为_______________。
②反应过程中需控制反应温度,同时将分液漏斗中溶液缓慢滴入A中,如果滴速过快则会导致产品产率降低,同时产生大量氮气,写出该过程的化学反应方程式:__________,故分液漏斗中的溶液是______(填标号)。
A.CO(NH2)2溶液 B.NaOH和NaClO
③充分反应后,加热蒸馏A内的溶液,收集108~114℃馏分,即可得到水合肼的粗产品。
实验三:测定馏分中肼含量。
(4)称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2〜3滴淀粉溶液,用0.10mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在______(填"酸式”或“碱式”)滴定管中,本实验滴定终点的现象为____________________。
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4·H2O)的质重分数为__________。





 乙
乙 丁
丁 乙
乙 丁
丁 乙
乙 丁
丁