-
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
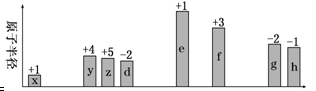
根据判断出的元素回答问题:
(1)f在周期表中的位置是 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):__________________;比较g 、h的最高价氧化物对应水化物的酸性强弱:____________________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:____________________。
(4)已知1mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:_____________________________________________________。
-
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是_____________。
(2)上述元素形成的简单阴、阳离子中,离子半径最大的是(用化学式表示,下同)________;在e、f、g、h四种元素的最高价氧化物对应的水化物中的酸性最强的是__________。
(3)d、e能形成原子个数比为1:1的化合物,该化合物的电子式为_______,0.10 mol该化合物与足量水反应时转移的电子数为____________。
(4)气体分子(yz)2的电子式为____________,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是_____________________________。
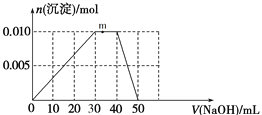
(5)上述元素可组成盐R: zx4f(gd4)2,向盛有10 mL1 mol/L R溶液的烧杯中滴加1 mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:

①在m段发生反应的离子方程式为______________________。
②若在10mLlmol/L R溶液中改加20 mLl.2 mol/L Ba(OH)2溶液,充分反应后,溶液中产生的沉淀的物质的量为__________。
-
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
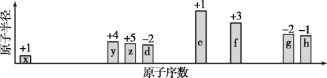
根据判断出的元素回答问题:
(1)h在周期表中的位置是________。
(2)比较d、f离子半径大小(用化学式表示,下同):____>____。比较g、h的最高价氧化物对应水化物的酸性强弱:____>____。
-
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)y在元素周期表中的位置是_______。z、d、e、f四种元素的简单离子中,半径最小的是______(填离子符号)。
(2)g和h氢化物的稳定性由大到小的顺序:_______(用化学式表示)。
(3)元素e和g的同族元素中半径最小元素组成的化合物B中离子半径较大的是______(填离子符号)。
(4)下列可作为比较f和Na随金属性强弱的依据是____。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱(或酸)性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)有人建议将氢元素排在元素周期表的IVA族,请你从化合价的角度给出一个理由_______。
-
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
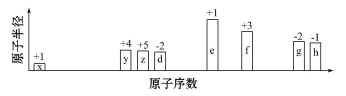
根据判断出的元素回答问题:
(1)g在周期表中的位置是________。
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:________>________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:________。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:________。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有 10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
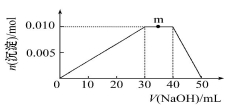
①写出m点反应的离子方程式:________。
②若在R溶液中改加20 mL 1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________mol。
-
随原子序数的递增,八种短周期元素(用字母x表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
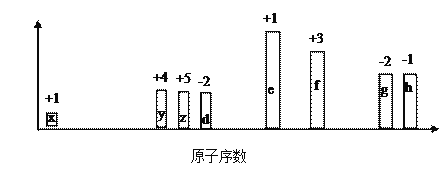
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同)________________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:__________。
(4)已知1mol e 的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:__________________。
-
随原子序数的递增,八种短周期元素(用字母x表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。根据判断出的元素回答问题:
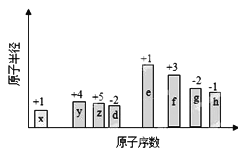
(1)y在元素周期表的位置是_____。
(2)比较g、h的气态氢化物的还原性强弱是:_____>_____。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式_____。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol∙L‐1R溶液的烧杯中滴加1mol∙L‐1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
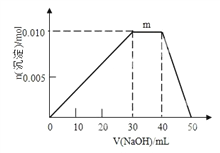
①写出m点反应的离子方程式_____。
②若R溶液改加20mL1.2 mol∙L‐1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为______mol。
-
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
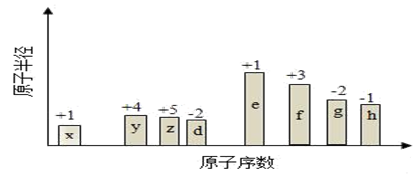
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)写出x与z形成四原子共价化合物的电子式__________。
(4)物质A是一种比水轻的油状液体,仅由x、y两种元素组成,y元素与x元素的质量比为12:1,A的相对分子质量为78.A与浓硫酸与浓硝酸在50-60℃反应的化学反应方程式______,反应类型______.
-
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
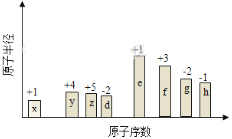
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的大小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
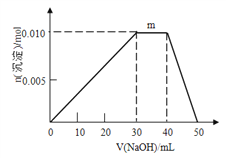
①写出m点反应的离子方程式_____________________________。
②若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
-
随原子序数递增,八种短周期元素(用字母 x 等表示),原子半径的相对大小、最高正价或最低负价的变化如下图所示:
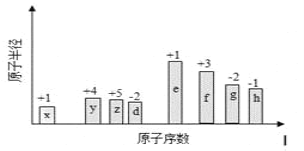
根据判断出的元素回答问题:
(1)g 在周期表中的位置是__________.
(2)d、e、h 的简单离子半径由大到小顺序:_____________(用离子符号表示).
(3)有关 y、z、d 三种元素的说法正确的是__________(填序号).
①最高正价:d>z>y ②简单气态氢化物的稳定性:d>z>y
③非金属性:d>z>y ④单质活泼性:y>z>d
(4)根据g 和h 两种元素填空:
①最高正价氧化物对应水化物的酸性由强到弱的顺序是____________.(用化学式表示)
②g2h2 分子中原子都满足 8 电子结构,试写出其电子式____________.
(5)①试写出x、d、e 形成化合物的水溶液与单质f 反应的化学方程式________________.
②已知化合物A、B 均由 x、d、e、g 四种元素组成,试写出A 和B 反应的离子方程式________________。