-

某班级兴趣小组计划对金属与酸反应的情况进实验探究.
实验目的:探究酸的浓度对金属反应速度的影响;酸的浓度对生成氢气的量的影响.
实验原理:锌与稀硫酸反应生成氢气
实验仪器:氢气的制取和收集装置、托盘天平、量筒、秒表.
实验试剂:锌粒,5%的稀硫酸,10%的稀硫酸.
实验步骤:
实验一:称量:用托盘天平称取锌粒1.3g,放入干燥管内;用量筒量取500mL5%稀硫酸(足量),倒入500mL烧杯.
如图所示连接仪器,收集氢气,记录反应时间和产生氢气的体积(如下表).
实验二:量取500mL10%的稀硫酸,重复上述实验,记录反应时间和生成氢气的体积(如下表).
| 实验编号 | 锌的质量 | 足量稀硫酸的浓度 | 时间 | 生成氢气的体积 |
| 实验一 | 1.3g | 5% | 169分钟 | 448mL |
| 实验二 | 1.3g | 10% | 66分钟 | 448mL |
结论:
①同种金属在浓度较大的稀硫酸(或盐酸)中反应的速度______.
②______.
-
金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
(提出问题)锌与硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与稀硫酸的浓度有关;b.可能与锌的形状有关。
(设计并实验)小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 稀硫酸的浓度(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
(1)锌与稀硫酸反应的化学方程式为_____。
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是_____。
(3)利用如图装置进行实验时,为了较准确的测量氢气的体积,在读取量气管中液面读数的过程中,应注意_____(填字母编号)。
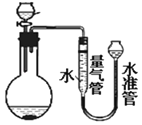
A.读数时视线与凹液面最低处相平。
B.保持水准管静止,待水准管中液面不再上升时再读数。
C.读数前应上下移动水准管,待两管液面相平再读数。
通过上述实验,你得出的结论是硫酸的质量分数越大,反应速率越快。锌与硫酸的接触面积越大,反应速率越快
(4)发生装置中留有氢气,是否会影响实验最终结果_____(填“是”或“否”)。
(5)下表是小组同学第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第4分钟 | 第3分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 9.6mL | 11.9mL | 7.6mL | 6.0mL |
解释第二分钟以后变化的原因_____。
-
为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
| 图象 | 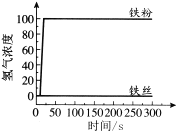
| 
| 
|
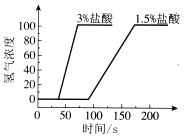
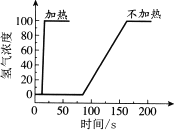
| 实验 | 等质量的铁丝、铁粉分别与相同浓度的盐酸反应 | 等质量的铁粉分别与不同浓度的盐酸(3%和1.5%)反应 | 不同温度下, 等质量的铁粉与相同浓度的足 量稀盐酸反应 |
A.由图1可知铁粉反应更快
B.由图1可得结论:盐酸不能与铁丝反应
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
-
某学习小组的同学为探究实验室制取氢气的方案,分别用等质量的金属A、B跟质量相同、浓度相同稀硫酸反应,反应生成氢气的质量与时间的关系如图(已知金属A、B在生成物中均显+2价,A的相对原子质量大于B)。
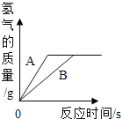
分析图像得到的下列结论中,其中不合理的是
A. 金属的活动性A>B
B. 生成氢气的质量A=B
C. 两份硫酸均反应完,B一定有剩余
D. A、B均反应完,硫酸有剩余
-
某化学兴趣小组设计了如下实验来探究影响锌与稀硫酸反应速率的因素(实验过程中杂质不能与稀硫酸反应),实验数据记录如下表:
| 实验编号 | 试剂 | 产生50mL氢气 的时间/s |
| 不同纯度的锌 | 稀硫酸的浓度 | 稀硫酸的用量/ mL |
| a | 纯锌 | 30% | 30 | 52 |
| b | 含杂质的锌 | 30% | 30 | 47 |
| c | 纯锌 | 20% | 30 | 68 |
| d | 纯锌 | 30% | 40 | 50 |
(1)实验_____和实验______(填实验编号)的实验目的是为了研究硫酸浓度对反应速率的影响。
(2)对比实验a和实验b,可以得到的实验结论是____________________。
(3)计算9.8g纯硫酸与足量的锌完全反应,可制得氢气是_________克?请你帮他们完善计算过程:
①______________②____________________

-
(2009•济宁)某兴趣小组为探究活泼金属与酸反应的规律,将质量相等的甲、乙两种金属分别放入到质量分数相同的足量稀盐酸中,经实验测定并绘制出生成氢气的质量与反应时间的关系(见右图).分析图象得到的以下结论中,一定正确的是( )
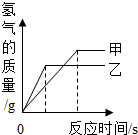
| A.金属甲比金属乙活泼 |
| B.金属甲比金属乙的相对原子质量大 |
| C.金属乙比金属甲的反应速率大 |
| D.金属乙比金属甲的化合价高 |
-
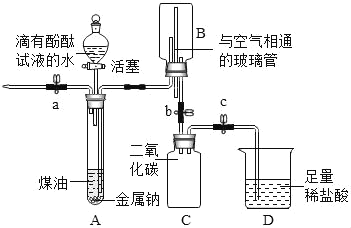
已知:煤油不与金属钠反应;煤油密度比水小且不溶于水;金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气。化学兴趣小组同学设计了如图所示装置进行实验探究,有关实验操作及现象记录如下:
| 
步骤 | 操 作 | 现 象 |
| Ⅰ | 先打开a,再打开分液漏斗活塞。 待大试管A中充满液体后,立即 关闭a及分液漏斗活塞 | A中液体分层,油层在上;钠熔成银白色小球, 在液体的界面处剧烈反应,产生大量气泡; 下层溶液呈红色,并逐渐进入B中 |
| Ⅱ | 打开b,待B中部分溶液进入C 中时关闭b,并打开a排气减压 | C中溶液仍呈红色 |
| Ⅲ | 打开止水夹c | D中溶液进入C中,产生气泡,溶液变为无色 |
下列关于该实验的说法:
①步骤Ⅰ、Ⅱ中红色溶液呈碱性,步骤Ⅲ中 无色溶液呈中性
②本实验证明了二氧化碳能与氢氧化钠起反应
③装置D中若改用氯化钙溶液也能实现实验探究的目的
④步骤Ⅲ中,C装置内发生的化学反应是1个
⑤装置B中与空气相通的玻璃管的作用是维持内外气压平衡,使液体顺利地进出
以上说法中正确的是( )
A. ①②③ B. ②③⑤ C. ①④⑤ D. ②④⑤
-
为了探究金属与酸的反应,某兴趣小组进行了以下实验:
(1)A小组研究影响金属与酸反应剧烈程度的因素,如图时20℃时相同质量的铁粉、铁片、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。

由此分析,归纳出影响金属与酸反应速率的因素有:金属的种类、_____和_____。
(2)金属铬(Cr)越来越受到人们的关注,B小组对Cr、Al、Cu的金属活动性顺序进行了探究,过程如下:
(提出假设)对三种金属的活动性顺序提出假设
a.Al>Cr>Cu b.Cr>Al>Cu c._____
(设计实验)同温下,取大小相同的金属薄片,分别投入到等体积、等浓度的足量稀盐酸中,观察现象,记录如下:
| 金属 | Cr | Al | Cu |
| 现象 | 反应缓慢,金属逐渐溶解 | 反应激烈,金属迅速溶解 | 无明显现象 |
(实验条件)实验前,打磨三种金属发生的是_____(填“物理”或“化学”)变化;上述实验使用等浓度的盐酸溶液的理由是_____。
(得出结论)原假设中正确的是_____(填假设中a、b或c),写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式_____。
-
为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
| 图象 | 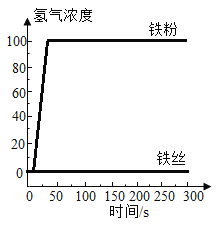 图1 图1
| 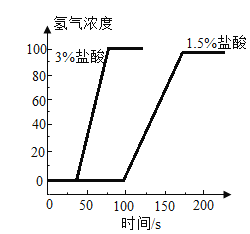 图2 图2
|  图3 图3
|
| 实验 | 等质量的铁丝、铁粉分别与相同浓度的盐酸反应 | 等质量的铁粉分别与不同浓度的盐酸(3%和15%)反应 | 不同温度下,等质量的铁粉与相同浓度的足量稀盐酸反应 |
A.由图1可知:盐酸不能与铁丝反应
B.由图1可得结论:铁粉反应更快
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
-
(09济宁)某兴趣小组为探究活泼金属与酸反应的规律,将质量相等的甲、乙两种金属分别放入到质量分数相同的足量稀盐酸中,经实验测定并绘制出生成氢气的质量与反应时间的关系(见下图)。分析图像得到的以下结论中, 一定正确的是:( )

A.金属甲比金属乙活泼
B.金属甲比金属乙的相对原子质量大
C.金属乙比金属甲的反应速率大
D.金属乙比金属甲的化合价高










 图1
图1 图2
图2 图3
图3