-
以反应5H2C2O4+2MnO4-+6H +===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
①
0.10
2.0
0.01
4.0
25
②
0.20
2.0
0.01
4.0
25
③
0.20
2.0
0.01
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO 4溶液的褪色时间为40 s,则这段时间内平均反应速率v(KMnO4)=2.5×10 -4 mol·L -1·s -1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
高二化学单选题困难题查看答案及解析
-
以反应5H2C2O4+2MnO4-+6H +===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
①
0.10
2.0
0.01
4.0
25
②
0.20
2.0
0.01
4.0
25
③
0.20
2.0
0.01
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO 4溶液的褪色时间为40 s,则这段时间内平均反应速率v(KMnO4)=2.5×10 -4 mol·L -1·s -1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
高二化学单选题困难题查看答案及解析
-
以反应5H2C2O4+2MnO4-+6H +===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO 4溶液的褪色时间为40 s,则这段时间内平均反应速率υ(KMnO4)=2.5×10 -4 mol·L -1·s -1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
高二化学选择题困难题查看答案及解析
-
以反应5H2C2O4+2MnO4-+6H +===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO 4溶液的褪色时间为40 s,则这段时间内平均反应速率υ(KMnO4)=2.5×10 -4 mol·L -1·s -1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
高二化学单选题困难题查看答案及解析
-
以反应5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KmnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法不正确的是( )
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol/L
体积/mL
浓度/mol/L
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
A.实验①、②、③所加的H2C2O4溶液均要过量
B.实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
C.实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影响
D.实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速率v(KMnO4)=2.5×10-4 mol·L-1·s-1
高二化学单选题困难题查看答案及解析
-
以反应5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KmnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/mol·L-1
体积/mL
浓度/mol·L-l
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速率v(KMnO4)=2.5×10-4 mol·L-1·s-1
C. 实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影响
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
高二化学选择题中等难度题查看答案及解析
-
以反应5H2C2O4 + 2MnO4- + 6H+ = 10CO2↑ + 2Mn2+ + 8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号
H2C2O4溶液
酸性KMnO4
温度/oC
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速v(KMnO4)= 2.5×10 -4 mol·L-1·s-1
C. 实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影响
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn2+对反应起催化作用
高二化学单选题中等难度题查看答案及解析
-
甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4- + 5H2C2O4+ 6H+=2Mn2+ +10CO2+8H2O)
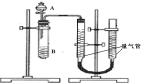
甲组:利用右图装置,通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。(实验中所用KMnO4溶液均已加入H2SO4)
序号
A溶液
B溶液
①
2ml 0.2mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液
②
2ml 0.1mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液
③
2ml 0.2mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液和少量MnSO4
(1)该实验的目的是探究 对化学反应速率的影响。
(2)分液漏斗中A溶液应该 加入(填“一次性”或“逐滴滴加”)
(3)实验结束后,读数前为了使两个量气管的压强相等,避免产生压强差,影响测定结果,需要进行的操作是 。
乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率
为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号
1
2
3
4
水/ml
10
5
0
X
0.5 mol/L H2C2O4/ml
5
10
10
5
0.2 mol/L KMnO4/ml
5
5
10
10
时间/s
40
20
10
---
(4)X=
A.5 B.10 C.15 D.20
4号实验中始终没有观察到溶液褪色,你认为可能的原因是 。
高二化学实验题中等难度题查看答案及解析
-
甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2+8H2O)
甲组:利用如图装置,通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.(实验中所用KMnO4溶液均已加入H2SO4)

序号
A溶液
B溶液
①
2ml 0.2mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液
②
2ml 0.1mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液
③
2ml 0.2mol/LH2C2O4溶液
4ml 0.01mol/LKMnO4溶液和少量MnSO4
(1)该实验的目的是探究________________对化学反应速率的影响.
(2)分液漏斗中A溶液应该_____________加入(填“一次性”或“逐滴滴加”)
(3)实验结束后,读数前为了使两个量气管的压强相等,避免产生压强差,影响测定结果,需要进行的操作是____________________.
乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号
1
2
3
4
水/ml
10
5
0
X
0.5mol/L H2C2O4/ml
5
10
10
5
0.2mol/L KMnO4/ml
5
5
10
10
时间/s
40
20
10
﹣﹣﹣
(4)X=____________
A.5 B.10 C.15 D.20
4号实验中始终没有观察到溶液褪色,你认为可能的原因是____________
高二化学实验题困难题查看答案及解析
-
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

实验序号
A溶液
B溶液
①
20 mL 0.1 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
②
20 mL 0.2 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
(1)该实验探究的是________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是________>________(填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=_______mol·L-1。(假设混合溶液体积为50 mL)
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定________来比较化学反应速率。
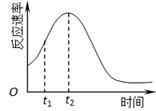
(4)小组同学发现反应速率总是如下图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②________。
高二化学实验题中等难度题查看答案及解析