-
A、B、C、D为短周期元素,且原子序数依次增大。已知A原子的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子。下列说法正确的是
A.非金属性:A>B
B.四种元素中,C处于元素周期表中最左、下方,故原子半径最大
C.元素B和C只能形成一种化合物
D.A、C、D的最高价氧化物对应的水化物中没有两性氢氧化物
高二化学选择题中等难度题查看答案及解析
-
A、B、C、D为短周期元素,且原子序数依次增大。已知A原子的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子。下列说法正确的是
A.非金属性:A>B
B.四种元素中,C处于元素周期表中最左、下方,故原子半径最大
C.元素B和C只能形成一种化合物
D.A、C、D的最高价氧化物对应的水化物中没有两性氢氧化物
高二化学选择题简单题查看答案及解析
-
原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29。
用元素符号或化学式回答下列问题:
(1)Y在周期表中的位置为__________________。
(2)已知YZ2+与XO2互为等电子体,则1mol YZ2+中含有π键数目为___________。
(3)X、Z与氢元素可形成化合物XH2Z,XH2Z分子中X的杂化方式为_________________。
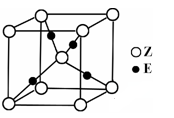
(4)E原子的核外电子排布式为__________;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该价态的化学式为____________。
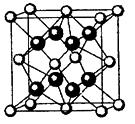
(5)氧元素和钠元素能够形成化合物F,其晶胞结构如图所示(立方体晶胞),晶体的密度为ρg··cm-3,列式计算晶胞的边长为a=______________cm(要求列代数式)。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D为四种短周期主族元素,且原子序数依次增大。已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子。下列说法正确的是
A.原子半径:C>A
B.气态氢化物的稳定性:A>B
C.最高价氧化物对应水化物的碱性:C < D
D.D元素形成的氧化物和氢氧化物能溶于酸,但不能溶于C元素形成的氢氧化物
高二化学选择题简单题查看答案及解析
-
A、B、C、D为四种短周期主族元素,且原子序数依次增大.已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子.下列说法正确的是( )
A.最高价氧化物对应水化物的碱性:C<D
B.气态氢化物的稳定性:A>B
C.四种元素能够在同一周期
D.原子半径:C>A高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、W为四种短周期主族元素,且原子序数依次增大.已知X的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最外层电子数是W原子最外层电子数的2倍,Z原子最外层只有一个电子.下列说法正确的是( )
A.最高价氧化物对于水化物的碱性:Z<W
B.原子半径:Z>X
C.气态氢化物的稳定性:X>Y
D.Y与Z能形成共价化合物高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、W为短周期元素,且原子序数依次增大。已知X原子的最外层电子数是其内层电子数的3倍,Y原子最外层只有一个电子,Z是地壳中含量最高的金属元素,W与X属于同一主族。下列说法正确的是( )
A. 金属性:Z>Y
B. 元素X和Y只能形成一种化合物
C. 原子半径:W>Z>Y>X
D. Y、Z、W的最高价氧化物对应的水化物均能相互反应
高二化学选择题困难题查看答案及解析
-
(12分)X、Y、Z、W、N五种元素中,X原子核外的M层中只有两个成对电子,Y原子的外围电子排布式为nsnnpn+1,Z是地壳内含量(质量分数)最高的元素,W的核电荷数是X与Z的核电荷数之和,N在元素周期表的各元素中电负性最大。
(1)Z元素基态原子的电子排布图为________
(2)W的元素符号是________,在周期表中的位置是________,其基态原子的电子排布式为________,在形成化合物时它的最高化合价为
(3)Y的氢化物的VSEPR模型是________,属于________分子(填极性或非极性),
(4)X的氢化物的沸点________Z的氢化物的沸点(填大于、小于或等于)
原因是
(5)用氢键表示式写出N的氢化物溶液中存在的所有氢键
________
高二化学填空题简单题查看答案及解析
-
(10分)X、Y、Z、W、N五种元素中,X原子核外的M层中只有两个成对电子,Y原子的外围电子排布式为nsnnpn+1,Z是地壳内含量(质量分数)最高的元素,W的核电荷数是X与Z的核电荷数之和,N在元素周期表的各元素中电负性最大。
(1)Z元素基态原子的电子排布图为________。
(2)W的元素符号是________,在周期表中的位置是________,在形成化合物时它的最高化合价为________。
(3)Y的氢化物的VSEPR模型是________,属于________分子(填极性或非极性),
(4)X的氢化物的沸点________Z的氢化物的沸点(填高于、低于或等于)
原因是________。
(5)用氢键表示式写出N的氢化物分子间存在的氢键________。
高二化学填空题中等难度题查看答案及解析
-
已知:A、B、C、D、E、F六种元素核电荷数依次增大,属元素周期表中前四周期的元素。其中A原子核外有三个未成对电子;B和E可形成离子化合物B2E,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序为________(用元素符号表示)。
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是________。
⑶F原子的核外电子排布式是____________,F的高价离子与A的简单氢化物形成的配离子的化学式为________。
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为________(黑色球表示F原子)。
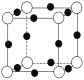
⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为________。
高二化学综合题简单题查看答案及解析