-
肼(N2H4)是氮和氢形成的一种化合物,易溶于水.工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如下:

十水合碳酸钠制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O.
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有________(选填编号).
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测Cl2与NaOH溶液发生反应的化学方程式:________.
从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:________.
(3)在实验室中,欲从母液中分离出十水合碳酸钠晶体.可采用的操作依次为________(选填编号).
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等.请写出肼除氧时发生反应的化学方程式:________.
-
(7分)肼(N2H4)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如下:
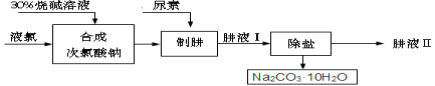
制肼过程的反应为:CO(NH2)2(尿素) + NaClO + 2NaOH = N2H4 + Na2CO3 + NaCl + H2↑
(1)实验室若配制30%烧碱溶液,所需玻璃仪器除玻璃棒外,还有 (选填编号)。
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2 + H2O = HCl + HClO(次氯酸),请推测Cl2与NaOH溶液发生反应的化学方程式: 。 从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71 : 。
(3)在实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为蒸发浓缩、 、洗涤。
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式: 。
-
肼(N2H4)是氮元素和氢元素形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品碳酸钠晶体,其工艺流程如下:
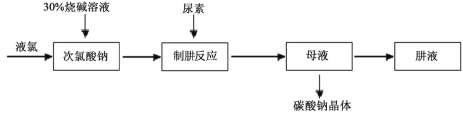
(1)实验过程中,制肼的化学反应方程式为:CO(NH2)2 + NaClO + 2NaOH═N2H4 + Na2CO3 + H2O + _____(填化学式);
(2)实验室配制 30%烧碱溶液,所需的玻璃仪器有_____(填序号);
A 漏斗 B 烧杯 C 烧瓶 D 量筒 E 玻璃棒
(3)在实验室中,从不饱和的碳酸钠母液的溶液中分离出碳酸钠晶体,可以采用的操作 依次为_____(填序号)和过滤;过滤时,若液面高于滤纸边缘,会导致得到的碳酸钠晶体质量_______(填“偏高”或“偏低”)。
A 蒸馏 B 蒸发 C 灼烧 D 过滤 E 冷却结晶
-
肼(NH)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如下:
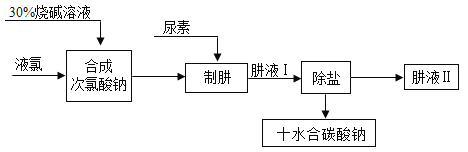
制肼过程的反应为:

(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有_____(填标号)。
A 漏斗 B 烧杯 C 烧瓶 D 量筒
(2)已知: 。请推测Cl2与NaOH溶液发生反应的化学方程式:_____;从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_____。
。请推测Cl2与NaOH溶液发生反应的化学方程式:_____;从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_____。
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为_____(填标号)。
A 蒸馏 B 蒸发 C 灼烧 D 过滤 E冷却结晶
(4)肼具有很好的还原性,且还原产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式_____。
-
肼(N2H4)是氮和氢形成的化合物,易溶于水。工业上利用尿素法生产肼,同时得副产品十水碳酸钠,工艺流程如下:
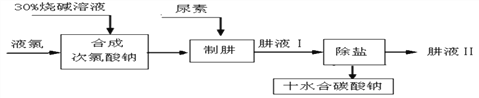
(资料)①尿素的化学式为CO(NH2)2; ②Cl2+H2O==HCl+HClO;
③制肼过程的反应为CO(NH2)2+NaClO+2NaOH==N2H4+Na2CO3+NaCl+H2O;
下列说法不正确的是
A. 尿素不能与熟石灰、草木灰等碱性物质混合使用,会生成氨气,造成肥效流失
B. Cl2与NaOH溶液发生反应的化学方程式为Cl2+2NaOH==NaCl+NaClO+H2O
C. 从母液中分离出十水合碳酸钠晶体,可采用蒸发浓缩、冷却结晶、过滤、洗涤干燥等步骤
D. 从后续反应过程来看,若要使原料利用率最佳,合成次氯酸钠时投入的液氯与烧碱的质量之比为71 :80
-
肼(N2H4)是氮和氢形成的化合物,易溶于水。工业上利用尿素法生产肼,同时得副产品十水碳酸钠,工艺流程如下:

(资料)①尿素的化学式为CO(NH2)2; ②Cl2+H2O==HCl+HClO;
③制肼过程的反应为CO(NH2)2+NaClO+2NaOH==N2H4+Na2CO3+NaCl+H2O;
下列说法不正确的是
A. 尿素不能与熟石灰、草木灰等碱性物质混合使用,会生成氨气,造成肥效流失
B. Cl2与NaOH溶液发生反应的化学方程式为Cl2+2NaOH==NaCl+NaClO+H2O
C. 从母液中分离出十水合碳酸钠晶体,可采用蒸发浓缩、冷却结晶、过滤、洗涤干燥等步骤
D. 从后续反应过程来看,若要使原料利用率最佳,合成次氯酸钠时投入的液氯与烧碱的质量之比为71 :80
-
碳酸镁水合物是制备镁产品的中间体。
【制取MgCO3·3H2O】工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO3·3H2O的方法如下:
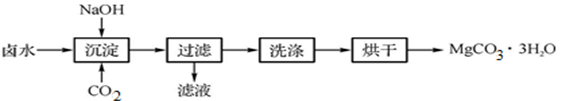
图1 获取MgCO3·3H2O的工艺流程
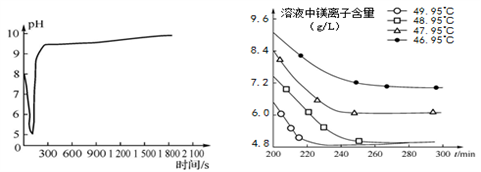
图2 沉淀过程的pH变化 图3 不同温度下溶液中镁离子含量随时间的变化
(1)沉淀过程的化学方程式为:
MgCl2+CO2+2NaOH+2H2O MgCO3·3H2O↓+2_________。
MgCO3·3H2O↓+2_________。
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为_______(填字母)。
a. 向卤水中滴加NaOH溶液,同时通入CO2
b. 向NaOH溶液中滴加卤水,同时通入CO2
c. 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
d. 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如表所示。
不同反应温度下的水合碳酸镁
| 温度(℃) | 产物 |
| 46.95 | MgCO3·3H2O |
| 47.95 | MgCO3·3H2O |
| 48.95 | MgCO3·3H2O |
| 49.95 | Mg5(OH)2(CO3)4·4H2O |
则沉淀过程选择的温度为_________,理由是_________。
【测定MgCO3·3H2O的纯度】
利用下图所示装置(图中夹持仪器略去)进行实验,以确定MgCO3·3H2O的纯度。
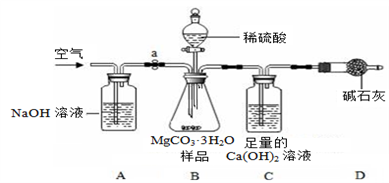
依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有_________。
(2)C中反应生成CaCO3的化学方程式为___________;D中碱石灰的作用为___________。
(3)下列各项措施中,不能提高测定准确度的是___________(填标号)。
a.在加入硫酸之前,应排净装置内的CO2气体
b.为了缩短实验时间,快速滴加硫酸
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在C装置左侧导管末端增添多孔球泡
(4)实验中准确称取15.0 g样品三份,进行三次测定,测得中生成CaCO3沉淀的平均质量为10.0 g。请计算样品中MgCO3·3H2O的纯度(写出计算过程)。 ______________________
(5)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有___________。
(6)若获取MgCO3·3H2O的样品中含有少量Mg5(OH)2(CO3)4·4H2O,则产品中镁元素的质量分数_______(填“偏大”“不变”或“偏小”,下同),样品中MgCO3·3H2O的纯度_______。
-
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(1)“降温”的目的是析出副产品“A晶体”,A的化学式是________.
(2)“操作Ⅰ”中的操作是________,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有________.
(3)“盐水精制Ⅰ”是除去盐水中的少量氯化镁,反应的化学方程式是________.
(4)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式 是________.
-
工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下:
①
②
③
④
下列说法不正确的是( )
A.反应①②④均有元素化合价发生变化
B.反应①④不属于四种基本反应类型中的任何一种
C.反应②③属于化合反应
D.四个反应的产物都有氧化物
-
食品添加剂碳酸钙为极细白色粉末,该产品可作面粉处理剂、膨松剂、稳定剂和食品工业用加工助剂.某实验探究小组利用石灰石为原料,设计了如下两个流程得到碳酸钙粉末.
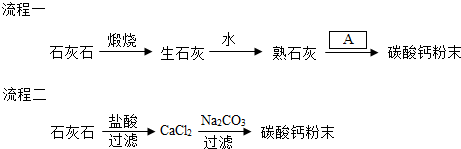
①生石灰的化学式是________,流程一中加入的“A”可以是CO2,这样做的优点是________;
②写出石灰石与盐酸发生的主要化学方程式________;写出以上流程中属于化合反应的化学方程式________;
③若石灰石中所含碳酸钙的纯度为90%,取用100g该石灰石则所含碳酸钙的物质的量为多少摩尔?用盐酸溶解上述石灰石,理论上所用盐酸含HCl的物质的量至少为多少摩尔?
请列式计算,写出计算过程:计算碳酸钙物质的量________计算HCl的物质的量
④“流程一”中生石灰加一定量的水得到熟石灰乳,而不是得到澄清石灰水,这样做的理由是________;
为判断熟石灰是否完全转化,实验的方法可以是取反应过程中少量样品进行如下实验:
| 实验药品及操作 | 实验现象 | 结论 |
| ________ | ________ | 熟石灰已完全转化 |
⑤“流程二”中有两次过滤,第一次过滤的目的是________,
过滤后发现滤液仍有一些浑浊,而过滤器经检查发现完好,此时应该进行的操作是________.
⑥若要得到食品级碳酸钙,上述两个流程中,应该倾向利用________(填“流程一”“流程二”)进行生产.










