-
Ⅰ.(1)研究钢铁的防腐蚀措施意义重大。利用如图所示装置可以模拟铁的电化学防护,其中Y为NaCl。
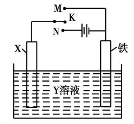
为减缓铁的腐蚀:
①若X为碳棒,开关K应置于 (填字母)处,此时X极发生的电极反应式为 。
②若X为锌,开关K置于M处,则此时铁极发生的电极反应式为 。
(2)在城市中地下常埋有纵横交错的管道和输电线路,地上还铺有铁轨,当有电流泄漏入潮湿的土壤中,并与金属管道形成回路时,就会引起后者的腐蚀。为表示其原理,某班级的学生绘制了下列装置图(假设电极材料均为铁,电解质溶液均为NaCl溶液)。

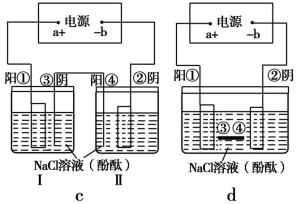
你认为其中能合理模拟金属管道的腐蚀原理的是 ;c(Ⅱ)的总反应方程式是 ;若图d 中接通电源,则平放的铁丝左侧附近产生的现象是 ;请你为防止地下金属管道腐蚀提供一种策略 。
Ⅱ.1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | 
| Cl− |
| 物质的量浓度/(mol/L) | 2 | 1 | 4 | x |
用惰性电极电解该溶液。当电路中有5 mol 电子通过时,溶液的pH= (忽略电解时溶液体积的变化及电极产物可能存在的溶解现象)。
-
利用如图装置可以模拟铁的电化学防护。下列叙述正确的是 ( )。
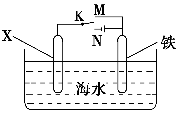
A.铁被腐蚀过程实质是金属铁发生了还原反应
B.若X为锌片,开关K置于M处,可减缓铁的腐蚀
C.若X为碳棒,开关K置于M处,可减缓铁的腐蚀
D.当K置于N处时,可减缓铁的腐蚀
-
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)利用如图装置,可以模拟铁的电化学防护。
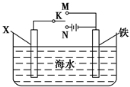
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为__________________。
(2)以下为铝材表面处理的一种方法:
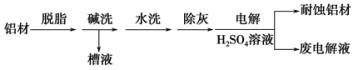
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_________________。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________________。
(3)镀铜可防止铁制品腐蚀,电镀时阳极材料为________________,用铜而不用石墨作阳极的原因是______________________。
-
利用如图所示装置,可以模拟铁的电化学防护。下列说法错误的是( )
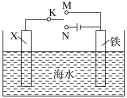
A.若X是锌棒,将K与M连接,此方法是牺牲阳极的阴极保护法,使铁不易受腐蚀
B.若X是碳棒,将K与N连接,可减缓铁的腐蚀
C.若X是碳棒,将K与M连接,碳棒的电极反应式是2H++2e-=H2↑
D.若X是锌棒,将K与N连接,锌棒的电极反应式是Zn-2e-=Zn2+
-
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是
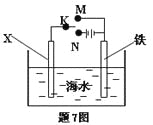
A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀
B.若X为锌棒,开关K置于M处,铁极发生氧化反应
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀
D.若X为碳棒,开关K置于N处,X极发生氧化反应
-
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是
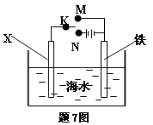
A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀
B.若X为锌棒,开关K置于M处,铁极发生氧化反应
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀
D.若X为碳棒,开关K置于N处,X极发生氧化反应
-
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是
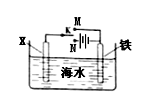
A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀
B.若X为锌棒,开关K置于M处,铁极发生氧化反应
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀
D.若X为碳棒,开关K置于N处,X极发生氧化反应
-
用如图装置研究电化学原理,下列分析中错误的是

| 选项 | 连接 | 电极材料 | 分析 |
| a | b |
| A | K1K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
| B | K1K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
| C | K1K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
| D | K1K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
A. A B. B C. C D. D
-
用如图装置研究电化学原理,下列分析中错误的是
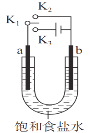
| 选项 | 连接 | 电极材料 | 分析 |
| a | b |
| A | K1K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
| B | K1K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
| C | K1K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
| D | K1K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
A. A B. B C. C D. D
-
用右图装置研究电化学原理,下列分析中错误的是
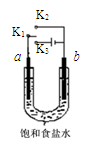
| 选项 | 连接 | 电极材料 | 分析 |
| a | b |
| A | K1 K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
| B | K1 K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
| C | K1 K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
| D | K1 K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
| | | | |












