-
NH3经一系列反应可以得到HNO3,如下图所示。

(1)已知反应N2(g)+3H2(g)  2NH3(g) △H,在恒压密闭容器中达到平衡状态。
2NH3(g) △H,在恒压密闭容器中达到平衡状态。
①根据表中所列键能数据,可得△H=_________kJ·mol–1。(用含a、b、c的式子表示)
| 化学键 | H-H | N-H | N≡N |
| 键能/ kJ·mol-1 | a | b | c |
②往上述平衡体系中充入氩气,此时v (N2)正 ________(填“增大”、“减小”或“不变”)
(2)某温度下,密闭容器发生反应N2O4(g) 2NO2(g),相互转化时的量变关系如图所示。请回答:
2NO2(g),相互转化时的量变关系如图所示。请回答:
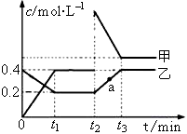
①代表乙的物质是_______(填“N2O4”或“NO2”)
②反应进行到t2时刻,改变的条件可能是_______________
③已知:N2(g)+O2(g) 2NO(g) △H=+180.5 kJ·mol–1
2NO(g) △H=+180.5 kJ·mol–1
CO(g)+1/2O2(g) CO2(g) △H=-283 kJ·mol–1
CO2(g) △H=-283 kJ·mol–1
治理汽车尾气过程中,将NO和CO转化成CO2和N2的反应的热化学方程式为_____________
(3)电解NO制备 NH4NO3的工作原理如图所示,总反应为:8NO+7H2O 3NH4NO3+2HNO3
3NH4NO3+2HNO3

 ① NH4NO3溶液中离子浓度由大到小顺序为_____________________
① NH4NO3溶液中离子浓度由大到小顺序为_____________________
② X极的电极反应为____________________
③ 为使电解过程中阳极产生的NO3–与阴极产生的NH4+全部转化为NH4NO3,需补充的物质A为________(填化学式)
-
在一密闭容器中进行如下反应:3H2(气)+N2(气) 2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3 的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3 的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
A.H2 为 0.6mol/L、N2 为 0. 2mol/L B.NH3 为 0.25mol/L
2mol/L B.NH3 为 0.25mol/L
C.N2、NH3 均为 0.15mol/L D.NH3 为 0.4mol/L
-
在密闭容器中,保持一定温度进行如下反应N2(g)+ 3H2(g) 2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=________。
(2)平衡常数K值越大,表明建立平衡时________(填字母序号)。
A.N2的转化率越高 B.NH3的产量越大
C.正反应进行得越彻底 D.化学反应速度越快
(3)a与b的关系是:a________b(填>、<、=)
(4)填写下表空格:
| 状态 条件 | 起始时物质的物质的量(mol) | 平衡时NH3的物质的量 (mol) |
| 编号 | X(N2) | Y(H2) | Z(NH3) |
| 恒容 | ① | 1 | 3 | 0 | b |
| ② | 0 | 0 | | b |
| ③ | | 2.25 | | b |
-
向容积相同的甲、乙密闭容器中投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol ):
):
| 反应物投入量 | NH3的浓度 (mol·L ) ) | 反应的 能量变化 | 体系压强 (Pa) | 反应物 转化率 |
| 甲 | 1mol N2、3mol H2 | c1 | 放出a kJ | p1 | α1 |
| 乙 | 2mol NH3 | c2 | 吸收b kJ | p2 | α2 |
下列说法正确的是( )
A.c1 = c2 B.a + b = 1 C.p1>p2 D.α1 +α2>1
-
已知合成氨反应的浓度数据如下:
| N2 + 3H2  2NH3 2NH3 |
| 起始浓度mol/L | 1.0 | 3.0 | 0 |
| 2秒末浓度mol/L | 0.6 | 1.8 | 0.8 |
| | | |
当用氨气浓度的增加来表示该化学反应速率时,其速率为 ( ).
A.0.2 mol/(L·s) B.0.4 mol/(L·s) C.0.6 mol/(L·s) D.0.8 mol/(L·s)
-
液氨气化后,分解产生的氢气可作为氢氧燃料电池的燃料。氨气分解反应的热化学方程式如下:
2NH3(g)  N2 (g) + 3H2(g) H = + a kJ·mol-1
N2 (g) + 3H2(g) H = + a kJ·mol-1
请回答下列问题:
(1)已知:2H2 (g) + O2 (g) =2H2O(l) H = - b kJ·mol-1
NH3 (g)  NH3(l) H = - c kJ·mol-1
NH3(l) H = - c kJ·mol-1
则4NH3(l) + 3O2 (g) = 2N2 (g) + 6H2O(l) 的H = kJ·mol-1。
(2)水能发生电离:2H2O(l)  H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式 。
H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式 。
(3)实验室用Pt电极对液氨进行电解可以得到H2和N2 ,若电解过程中阳极收集得到4.48L气体(标况),则转移的电子的数目是 ,标准状况下阴极得到的气体的质量为 g。
-
在一个容积为3L的密闭容器里进行如下反应N2(g)+ 3H2(g) 2NH3(g) ,反应开始时n(N2)=1.5mol, n(H2)=4.4mol, 2min末n(H2) =3.5mol。则:
2NH3(g) ,反应开始时n(N2)=1.5mol, n(H2)=4.4mol, 2min末n(H2) =3.5mol。则:
(1)用NH3的浓度变化来表示该反应的速率为 ;
(2)2min末时N2的浓度为 ;
(3)氮气的转化率为 。
-
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2 + 3H2  2NH3(正反应是放热反应)。下列有关说法正确的是( )
2NH3(正反应是放热反应)。下列有关说法正确的是( )
A.降低温度可以加快反应速率
B.达到化学反应限度时,生成2mol NH3
C.向容器中再加入N2可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
-
合成氨反应:N2(g) + 3H2(g)  2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
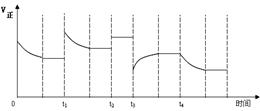
下列说法正确的是
A.t1时增大了压强
B.t2时同倍数增加N2、H2的物质的量
C.t3时降低了温度
D.t4时增大了c(NH3)
-
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2  2NH3(正反应是放热反应)。下列有关说法正确的是
2NH3(正反应是放热反应)。下列有关说法正确的是
A.降低温度可以加快反应速率
B.达到化学反应限度时,生成2mol NH3
C.向容器中再加入N2可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量

2NH3(g) △H,在恒压密闭容器中达到平衡状态。
2NO2(g),相互转化时的量变关系如图所示。请回答:

2NO(g) △H=+180.5 kJ·mol–1
CO2(g) △H=-283 kJ·mol–1
3NH4NO3+2HNO3

① NH4NO3溶液中离子浓度由大到小顺序为_____________________
