-
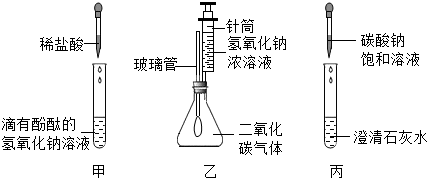
在学习碱的化学性质时,某兴趣小组进行了如图所示的实验.
Ⅰ.实验记录:
①在甲实验过程中,用温度计测量溶液温度,随着稀盐酸的不断滴入,溶液温度逐渐升高,你认为溶液温度升高的原因是________,该反应的化学方程式是________;
②乙实验中滴加氢氧化钠溶液后,可观察到的现象是________;
③丙实验中观察到试管内有白色沉淀产生;
Ⅱ.废液成分探究:
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和________;
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想:
猜想1:是碳酸钠; 猜想2:是氢氧化钠; 猜想3:是氢氧化钠和碳酸钠;
你的猜想是:是________(写一种猜想).
【实验设计】用氯化钙溶液来验证上述猜想.
查阅资料获悉氯化钙溶液呈中性,并设计如下实验.请将实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | 没有白色沉淀,溶液呈红色 | 猜想2正确 |
| ________ | 猜想1正确 |
| ________ | 猜想3正确 |
③要验证你的猜想,所需要的试剂和预计的现象是________.
【反思拓展】分析化学反应后所得物质成分时,除考虑生成物外还需考虑________.
-
(2011•息县一模)某兴趣小组在学习碱的化学性质时,进行了如图所示的实验.
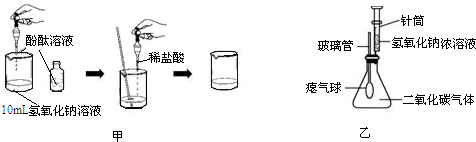
(1)在甲实验过程中,插入一支温度计来测量溶液的温度时,随着稀盐酸的不断滴入,溶液的温度逐渐升高,你认为溶液温度升高的原因是______;写出该反应的化学方程式______.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是______;反应的化学方程式______.
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个干净的废液缸中,看到有气泡出现,最终废液呈红色,由此产生疑问.
提出问题:废液中含有哪些物质?
交流讨论:①一定含有的物质:指示剂、水和______.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小兰认为:只有碳酸钠(提示:碳酸钠水溶液PH>7);小亮认为:只有氢氧化钠.你认为还可能是______.
实验设计:小斌想用氯化钙溶液来验证小兰、小亮和你的猜想.查阅资料获悉氯化钙
溶液呈中性,并设计如下实验.请你将小斌的实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上
层清液于试管中,
加入过量氯化钙
溶液,静置. | ①没有白色沉淀,溶液呈红色. | ______的猜想正确. |
②有白色沉淀,溶液由红色变
为无色 | ______的猜想正确. |
| ③______ | 你的猜想正确. |
(4)在甲实验中,如果消耗质量分数为7.3%的稀盐酸20.0g时,此时溶液的颜色恰好由红色变为无色,试计算氢氧化钠溶液中溶质的质量分数.(提示:氢氧化钠溶液的密度为1g/ml)
-
某兴趣小组在学习碱的化学性质时,进行了如图所示的实验。
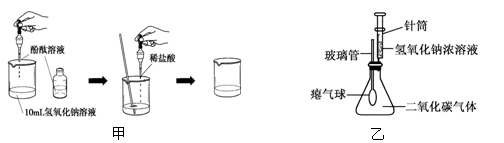
(1) 在甲实验过程中,插入一支温度计来测量溶液的温度时,随着稀盐酸的不断滴入,
溶液的温度逐渐升高,你认为溶液温度升高的原因是________;
写出该反应的化学方程式________。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是________;
反应的化学方程式________。
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个干净的废液缸中,看到有
气泡出现,最终废液呈红色,由此产生疑问。
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:指示剂、水和________。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小兰认为:只有碳酸钠(提示:碳酸钠水溶液PH﹥7);小亮认为:只有氢氧化钠。
你认为还可能是________。
【实验设计】小斌想用氯化钙溶液来验证小兰、小亮和你的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小斌的实验设计补充完整。
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上 层清液于试管中, 加入过量氯化钙 溶液,静置。 | ①没有白色沉淀,溶液呈红色。 | ________的猜想正确。 |
| ②有白色沉淀,溶液由红色变 为无色 | ________的猜想正确。 |
| ③ | 你的猜想正确。 |
(4)在甲实验中,如果消耗质量分数为7.3%的稀盐酸20.0g时,此时溶液的颜色恰好
由红色变为无色,试计算氢氧化钠溶液中溶质的质量分数。(提示:氢氧化钠溶液的密度为1g/ml)
-
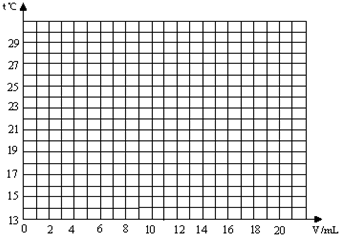
某化学兴趣小组对“氢氧化钠与稀盐酸反应中溶液温度升高的现象”进行了实验探究.在一定体积10%的氢氧化钠溶液中滴加10%的盐酸,并对反应中溶液的温度与加入盐酸的体积变化记录如下:
| 加入盐酸体积V(mL) | | 2 | 6 | 10 | 16 | 20 |
| 测得溶液温度t℃ | 14.0 | 15.2 | 22.0 | 28.2 | 24.7 | 22.9 |
请回答下列问题:
(1)写出氢氧化钠与稀盐酸反应的化学方程式______.
(2)在如图中,绘出溶液的温度与加入盐酸的体积之间的变化关系曲线.
(3)根据实验可得出结论是______.
(4)根据曲线讨论溶液温度变化的原因.加入盐酸的量在2-10mL之间时:______;加入盐酸的量在lO-20mL之间时:______.
-
某校化学兴趣小组对“大理石与稀盐酸反应快慢与温度的关系”进行了探究。
[实验探究]在不同温度下测量收集等体积CO2所需的时间及溶液温度变化(盐酸浓度18%、大理石颗粒大小均匀、质量相同),如下表:
| 温度/°C | 需要的时间/s | 温度变化/°C |
| 15 | 145 | +1 |
| 20 | 105 | +1 |
| 25 | 73 | +3 |
| 30 | 51 | +3 |
| 35 | 30 | +4 |
(1)写出大理石和稀盐酸反应的化学方程式_____________________。
(2)根据上表分析,大理石和稀盐酸反应过程中伴随着________________________(填“吸热”或“放热”现象)。
(3)在实验中控制的变量有_____________________________(填写一种即可)。
[实验结论]
(4)实验结果_______________________(填“可靠”或“不可靠”),理由是______________________。
[评价与反思]
(5)根据上表数据分析,你认为实验中温度计的灵敏度__________(填“高”或“不高”),其原因是______。
(6)除了温度,大理石和稀盐酸反应的快慢还可能受哪些因素的影响?请设计方案验证:
[影响因素]______________________。
[实验方案]______________________。
-
某研究性学习小组的同学对酸和碱之间的反应进行了如下探究:
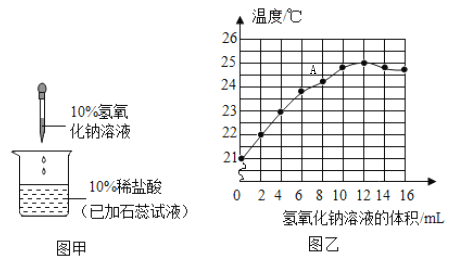
实验1:证明酸和碱发生了反应.
在图甲中,判断氢氧化钠溶液和稀盐酸恰好完全反应的实验现象是______.
实验2:测量酸和碱反应过程中温度的变化情况.
(1)往一定量的稀盐酸中逐滴滴加氢氧化钠溶液,烧杯中溶液温度变化如图乙所示.请判断A点时溶液的酸碱性为______性.
(2)若改为将等量稀盐酸往氢氧化钠固体中滴加,反应过程中最高温度远高于图乙中的最高值.请做出合理解释______.
-
学习中和反应时,老师和同学们展开了如下探究:
【探究一】:探究实验过程中的能量变化
用胶头滴管将10%的稀盐酸逐滴加入盛有NaOH溶液的烧杯中,并用温度计测量温度变化.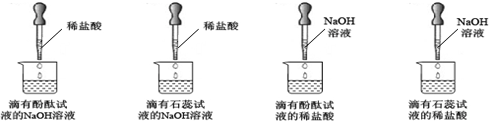
小军发现:随着稀盐酸的不断滴入,溶液的温度先升高后降低.对此合理的解释是______
______;
【探究二】:探究反应发生及反应终点问题
实验中,除了温度有变化外,没有任何现象能证明反应是否发生及反应是否已至终点,小雯同学在老师的帮助下,进行了下图所示的探究实验(滴加试剂时同时搅拌).
①通过实验现象,小雯排除了实验B,你认为她的理由是______;
②实验C中溶液的颜色最终变成了红色,但也被排除,原因是______;
③实验时,老师告诉小雯:相对于实验A,实验D也有不足.通过下面的资料,你认为理由是______;
【资料卡片】:
紫色石蕊试液和无色酚酞试液在不同酸碱性溶液中的变色情况
| 紫色石蕊试液 | pH<5.0:红色 | 5.0<pH<8.0:紫色 | pH>8.0:蓝色 |
| 无色酚酞试液 | pH<8.2:无色 | 8.2<pH<10.0:红色 | pH>10.0:无色 |
④小杰认为:将NaOH溶液和稀盐酸混合后的溶液蒸干,若得到白色固体,则说明反应生成NaCl,从而确认反应已发生,你认为这种观点是否正确,并说出理由?______.
【探究三】:探究实验过程中的意外情况
(1)为了提高实验的趣味性,老师演示了如下图所示的连贯实验,回答下列问题: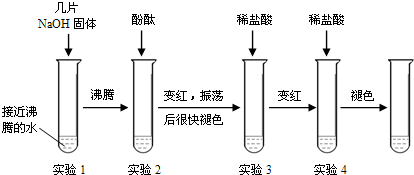
①实验1所得溶液沸腾时的温度______100℃(填“>”、“<”或“=”);
②实验后溶液一定显碱性的试管有______支,实验3后溶液中NaOH质量分数______(填“>”、“<”或“=”)实验2后溶液中NaOH质量分数;
③通过上述探究,你对酚酞试液在碱性溶液中的颜色变化有何新的认识?______;
(2)小岳在他的实验过程中意外发现有气泡出现,你认为原因是______.
【探究四】:从部分变质的NaOH样品中回收较为纯净的NaOH
小江同学查阅了不同温度下NaOH的溶解度(见资料卡片),并按如下步骤进行了实验(其中Ⅰ、Ⅱ、Ⅲ为实验操作):
【资料卡片】:
| 温度/°C | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 64 | 85 | 138 | 203 | 285 | 376 |
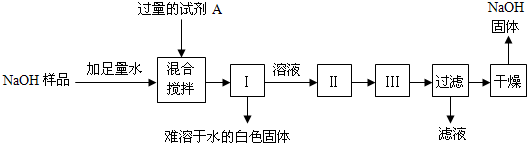
①试剂A是______(填化学式)溶液;
②操作名称:Ⅰ______、Ⅱ______、Ⅲ______;
③为获得纯度较高的NaOH固体,小江同学应在干燥前将其用______进行淋洗.
【探究五】:测定NaOH样品中NaOH的质量分数
小海取13.5g部分变质的NaOH固体样品加适量的水配成溶液,向其中加入足量质量分数为7.3%的稀盐酸,使其充分反应,生成二氧化碳2.2g(假设生成的CO2被完全吸收).
求:①样品中NaOH的质量分数(精确到小数点后一位);
②在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸质量的关系图(不要求精确);解题过程:______;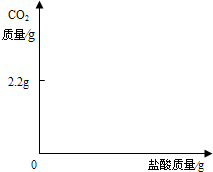
【反思】:经过讨论,大家一致认为小海方法有误,求出的NaOH的质量分数比实际值大,造成错误最有可能的原因是什么?______;
【拓展提高】:欲使实验结果准确可靠,你对小海的实验会做怎样的改进?______.
-
下面是某小组同学学习氢氧化钠和稀盐酸反应时的实录:
在盛有氢氧化钠溶液的烧杯中,插入一支温度计测量溶液的温度,用胶头滴管吸取10%的稀盐酸逐滴加入到氢氧化钠溶液中.
(1)探究实验中的能量变化:
在实验过程中,用温度计测量溶液的温度,结果发现:随着稀盐酸的不断滴入,溶液的温度逐渐升高.由此你可以得到的结论是______;
(2)探究反应终点问题:用什么方法证明氢氧化钠和盐酸恰好完全反应?他们提出下列两种方法:
方法一:在实验后所得溶液中滴入几滴无色酚酞试液,若溶液颜色没有变化,则恰好完全反应.
方法二:在氢氧化钠溶液中预先滴入几滴无色酚酞试液,然后再加入稀盐酸,若溶液颜色刚好由红色变为无色,则恰好完全反应.
你认为他们提出的方法中,方法一(填“正确”或“不正确”,下同)______,方法二______.
(3)探究物质组成的变化:反应后减少了的粒子是______.
(4)关于实验中的细节:实验中,稀盐酸必须用胶头滴管逐滴滴加______,这样做的目的是______.
-
化学兴趣小组同学进行氢氧化钠与盐酸的反应,并利用温度传感器和pH传感器得出如图图象,下列对于图象分析正确的是( )
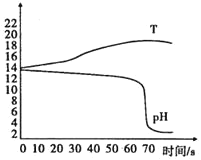
A. 该实验是将氢氧化钠溶液滴入盐酸中
B. 约70秒时恰好完全反应
C. 温度的变化能够直接证明二者发生化学变化
D. 中和反应放热,所以放热的反应一定是中和反应
-
某化学兴趣小组用数字化传感器探究稀氢氧化钠与盐酸反应过程中温度和pH的变化如图所示,测定结果如图A、B图所示。下列说法正确的是( )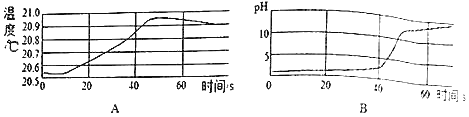
A. 该实验是将盐酸溶液滴入氢氧化钠溶液
B. 稀盐酸与氢氧化钠溶液反应是吸热反应
C. 20s至40s之间的某一时刻,两溶液恰好完全反应
D. 60s时溶质为NaOH和NaCl










