-
人类制得并利用金属有着悠久的历史:
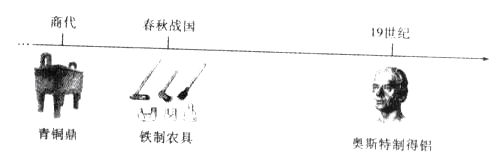
(1)利用孔雀石冶炼铜的主要反应:①Cu2(OH)2CO3 2CuO+H2O+CO2↑,该反应的类型是_____反应(填“化合”、”分解”或“置换”);
2CuO+H2O+CO2↑,该反应的类型是_____反应(填“化合”、”分解”或“置换”);
② 2CuO+C 2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_。
2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_。
( 2 )高炉炼铁的主要反应过程如下.请写出对应的化学方程式:
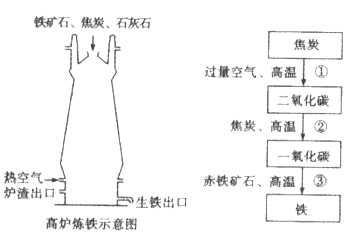
①_________;②_________;③_________。
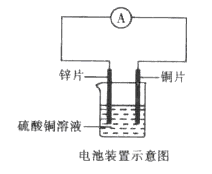
(3)冶炼金属铝的主要反应:2Al2O3 4Al+3O2↑,该反应的条件是______。下图的装置中,两种金属的活动性:Zn______ Cu (填“>”或“<”)。当电流表指针发生偏转时,化学能转化为______。
4Al+3O2↑,该反应的条件是______。下图的装置中,两种金属的活动性:Zn______ Cu (填“>”或“<”)。当电流表指针发生偏转时,化学能转化为______。
-
人类制得并利用金属有着悠久的历史:
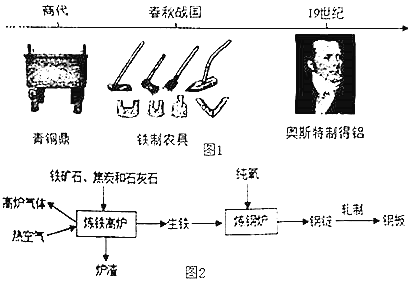
(1)利用孔雀石冶炼铜的主要反应:
①Cu2(OH)2CO3 =2CuO+H2O+CO2↑,该反应的基本反应类型是_____________;
=2CuO+H2O+CO2↑,该反应的基本反应类型是_____________;
②2CuO+C 2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_____________。
2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_____________。
(2)工业上炼铁炼钢和轧制钢材的主要流程如图2。
①高炉炼铁原理的化学方程式_____________。
②炼铁高炉中焦炭的作用:①提供高温;②_____________(用化学方程式表示)。
③生铁的硬度_____________(填“>”“<”或“=”)纯铁。将钢锭轧成钢板,体现了金属的_____________。
(3)常温下铝是一种活泼金属,但铝却有较强的抗腐蚀性,用化学方程式表示其原因_____________;根据所学的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关?_____________(填字母)
a.地壳中金属元素的含量 b.金属的导电性 c.金属的活动性 d.金属的延展性 e.金属冶炼的难易程度
-
孔雀石的主要成分是碱式碳酸铜 化学式为Cu2(OH)2CO3,碱式碳酸铜受热会分解生成二氧化碳等三种氧化物,
(1)写出该反应的化学方程式______ 2CuO+H2O+CO2↑
-
铜是人类最早利用的金属之一。 冶炼铜常用铜矿石——孔雀石,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],生成铜的简要流程如下:
(查阅资料)碱式碳酸铜是一种绿色的不溶于水的固体,受热易分解,从组成上分析,它兼备碱和碳酸盐的化学性质,所以能与酸发生反应。
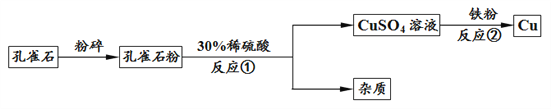
(1)反应前,将孔雀石粉碎的目的是_________________________。
(2)写出反应②的化学方程式_____________________。
(3)反应①后进行的操作名称是__________,若所得CuSO4溶液为浑浊的,则可能的原因是___________(写一种即可)。
(4)反应①除生成CuSO4外,还生成了两种氧化物,其化学式分别为_________、__________。
-
(7分)铜是人类最早利用的金属之一。 冶炼铜常用铜矿石——孔雀石,其主要成分为碱式碳酸铜[Cu2(OH)2CO3]。碱式碳酸铜是一种绿色的不溶于水的固体,受热易分解,从组成上分析,它兼备碱和碳酸盐的化学性质,所以能与酸发生反应。
斌斌同学准备在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取铜,设计实验流程如下:

请回答以下问题:
(1)碱式碳酸铜中含有 种元素。
(2)碱式碳酸铜受热分解生成三种常见的氧化物,其中有一种通常是黑色固体,请写出该黑色固体与木炭发生反应的化学方程式 。碱式碳酸铜与稀盐酸反应的化学方程式为Cu2(OH)2CO3+4HCl====2CuCl2+CO2↑+3H2O。预测实验现象: 。
(3)若孔雀石样品中含有44.4g Cu2(OH)2CO3,充分反应后,理论上能得到铜的质量为 g。
-
(2007•海淀区二模)孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
冶炼铜的反应原理为:Cu(OH)2CO3 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
2CuO+C 2Cu+CO2↑
2Cu+CO2↑
某校课外小组同学在实验室验证上述反应.
(1)加热分解碱式碳酸铜,生成氧化铜.装置如下图所示.
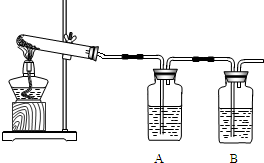
①瓶A中盛有的试剂是______,用来吸收水,证明碱式碳酸铜加热分解的产物中有水.
②瓶B中盛有的试剂是澄清石灰水,用来______,反应的化学方程式为______.
③反应结束,熄灭酒精灯前,应______.
(2)木炭和氧化铜反应,生成铜.
将木炭粉末和氧化铜粉末混合均匀,放进试管,加热充分反应.将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
查阅资料:部分内容如下:木炭和氧化铜都是黑色粉末.氧化铜与稀硫酸反应生成硫酸铜,木炭与稀硫酸不反应.
| | 操作和药品 | 现象 | 分析和结论 |
| 方案Ⅰ | 取少量剩余黑色粉末,充分灼烧 | ①______________
________________ | 原剩余黑色粉末是
氧化铜 |
| 方案Ⅱ | ②_______________
__________________ | ③_____________
_________________ | 原剩余黑色粉末是
氧化铜 |
猜想与验证:
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比.设计方案如下:
| | 配方1 | 配方2 | 配方3 | 配方4 |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
上述设计方案的主要研究方法是______.
-
以 CuSO4 为原料制备碱式碳酸铜[Cu2(OH)2CO3]的过程如下:

(资料)碱式碳酸铜受热易分【解析】
Cu2(OH)2CO3 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
(1)“沉淀”时的反应为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2______ +CO2↑
(2)检验沉淀是否洗涤干净应选用的试剂是_______ (填化学式),烘干时若产品出现少量 黑色物质,可能的原因为________.
(3)若所得产品的产率偏高,可能的原因为_______ (填序号)
A.反应物未完全沉淀 B.过滤时滤纸破损
C.Cu2(OH)2CO3 未洗涤干净 D.Cu2(OH)2CO3 未完全烘干
-
铜锈主要成分是Cu2(OH)2CO3。加热分解的化学方程式为:Cu2(OH)2CO3 2X+H2O+CO2↑,其中X的化学式是( )
2X+H2O+CO2↑,其中X的化学式是( )
A. Cu B. CuO C. Cu(OH)2 D. CuCO3
-
铜锈主要成分是Cu2(OH)2CO3。加热分解的化学方程式为:Cu2(OH)2CO3 2X+H2O+CO2↑,其中X的化学式是( )
2X+H2O+CO2↑,其中X的化学式是( )
A. Cu B. CuO C. Cu(OH)2 D. CuCO3
-
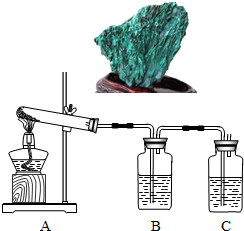
孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
查阅资料:①Cu2(OH)2CO3 2CuO+CO2↑+H2O 2CuO+C
2CuO+CO2↑+H2O 2CuO+C 2Cu+CO2↑
2Cu+CO2↑
②CuO为黑色固体,化学性质和氧化铁相似.
(1)实验l:加热分解碱式碳酸铜.装置如图所示.
①A中固体的变化为________.
②欲证明反应后有水生成,B中所盛试剂为________.
③反应结束时的操作应该是________,理由是________.
(2)实验2:木炭和氧化铜反应.
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
做出猜想:剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜.
实验验证:填写下表.
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:
| 配方l | 配方2 | 配方3 | 配方4 |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
上述设计方案的主要研究方法是________.

=2CuO+H2O+CO2↑,该反应的基本反应类型是_____________;
2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_____________。







