-
氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备 Mg3N2 并进行有关实验。实验装置如下所示: (部分加热装置已略去)
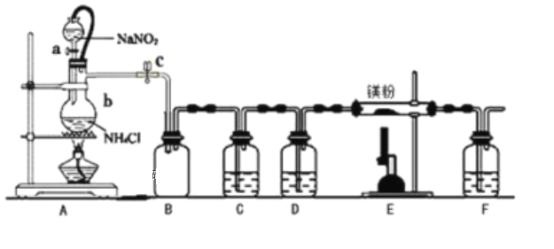
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器 b 的名称是__________,写出装置 A 中发生反应的化学方程式___________。
(2)加热至反应开始发生,需移走 A 处酒精灯,原因是__________________。
(3)装置 C 中为饱和硫酸亚铁溶液, 其作用是______________。
(4)定性分析产物
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量产品于试管中, 加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | 反应的化学方程式为______________________ |
| 弃去上层淸液, 加入足量稀盐酸 | 观察到固体全部溶解, 且有气泡冒出 | 气泡冒出的原因为________________ |
-
氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备 Mg3N2 并进行有关实验。实验装置如下所示: (部分加热装置已略去)
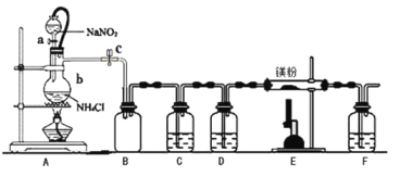
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器 b 的名称是__________,写出装置 A 中发生反应的化学方程式___________。
(2)某同学检验装置 A 部分的气密性,关闭止水夹 c 后,开启活塞 a,水不断往下滴,直至全部流入烧瓶。试判断:
A 部分装置是否漏气? ________ (填“漏气”、“不漏气”或“无法确定”),判断理由是____________。
(3)装置 C 中为饱和硫酸亚铁溶液, 其作用是___________,装置 F 的作用是________。
(4)加热至反应开始发生,需移走 A 处酒精灯,原因是__________________。
(5)定性分析产物
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量产品于试管中, 加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | 反应的化学方程式为 __________________________________ |
| 弃去上层淸液, 加入足量稀盐酸 | 观察到固体全部溶解, 且有气泡冒出 | 气泡冒出的原因为___________________________________________________ |
-
氮化镁(Mg3N2) 在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备Mg3N2并进行有关实验。实验装置如下所示:
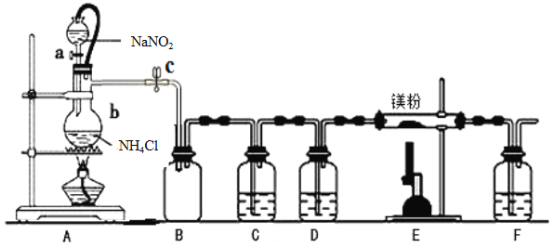
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器a、b的名称分别是____________,____________;写出装置A 中发生反应的化学方程式____________。
(2)装置C中为饱和硫酸亚铁溶液,作用是_________,该装置中发生反应的离子方程式为____________;装置D 中的试剂是____________,F 装置的作用是____________。
(3)加热至反应开始发生,需移走A 处酒精灯,原因是____________。
(4)实验结束后,取装置E的硬质玻璃管中的少量固体于试管中,加少量蒸馏水,把润湿的红色石蕊试纸放在管口,观察实验现象,该操作的目的是______________。反应的化学方程式为操作的目的是__________;再弃去上层清液,加入盐酸,观察是否有气泡产生,该操作的目的是__________。
-
氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备Mg3N2并进行有关实验。实验装置如下所示:
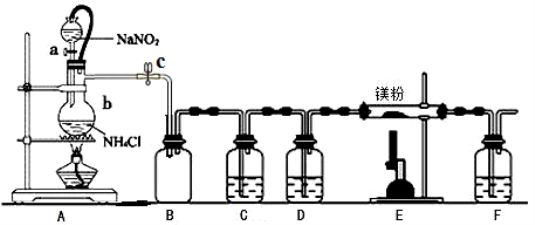
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器b的名称是________,写出装置A中发生反应的化学方程式___________________。
(2)某同学检验装置A部分的气密性,关闭止水夹c后,开启活塞a,水不断往下滴,直至全部流入烧瓶。试判断:A部分装置是否漏气?________(填“漏气”、“不漏气”或“无法确定”),判断理由:____________。
(3)装置C中为饱和硫酸亚铁溶液,作用是___________,F装置的作用是_______________________。
(4)加热至反应开始发生,需移走A处酒精灯,原因是_______________________________________。
(5)反应结束后,取m g E中样品于试管中,加足量蒸馏水,得V mL气体(换算为标准状况),则样品中氮化镁的质量分数为__________________。
-
氮化镁(Mg3N2) 是工业上应用广泛的离子化合物,常温下为浅黄色粉末,极易与水反应。某校化学兴趣小组用镁与氮气反应制备Mg3N2,并测定氮化镁的纯度。
I.制备氮化镁
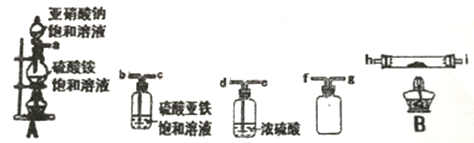
己知:亚硝酸钠和硫酸铵制取氮气的反应剧烈放热,产生氮气的速度较快。
(1)制取氮气的离子反应方程式为___________________
(2)实验装置(可重复使用)的连接顺序为a→____,______→______,_____→______→h,i→_____,→b→c,(按气流方向,用小写字母表示)。
II.测定氮化镁的含量
(3)定性分析
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量氮化镁样品于试管 中,加足量蒸馏水 | ______________ | ①写出反应的化学方程式 ____________ |
| 弃去上层清液,加入足量稀 盐酸 | 观察到固体全部溶解且冒气泡 | ②冒气泡的原因是 _______________ |
(4)定量测定
兴趣小组设计了一个简单的实验测定氮化镁的纯度,将实验操作补充完整(数据用字母表示,不用体现计算过程)。取ag的氮化镁样品于试管中,加入足量蒸馏水,__________________
-
氮化镁(Mg3N2)可用于核废料的回收,常温下为浅黄色粉末,易水解。某兴趣小组拟在实验室里通过氮气和镁粉反应制取少量氮化镁(Mg3N2),制备装置示意图如下。
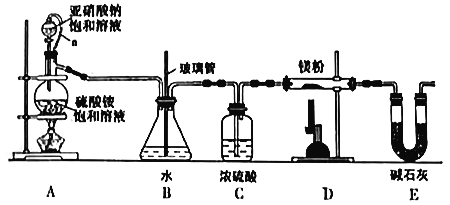
(1)工业上通常通过______________________获取氮气。
(2)装置A中橡胶管a的作用是______________________。
(3)NaNO2和(NH4)2SO4反应制备氮气的离子方程式______________________。
(4)装置B的作用为______________________。
(5)检验Mg3N2水解生成气体为NH3的方法为:取适量样品放入试管中,滴加蒸馏水,加热试管,_________________________________(填操作与现象)。
(6)为测定产物中Mg3N2纯度,该小组称取4.0g样品加入足量10%NaOH溶液并加热,生成的气体全部用100.00mL 0.500mol·L-1的硫酸溶液吸收。将所得溶液稀释到250.00mL,取25.00mL该溶液,用0.2000mol·L-1NaOH标准溶液滴定过剩的硫酸。重复实验平均消耗NaOH溶液25.25mL。样品中Mg3N2的质量分数为___________(保留一位小数)。滴定过程中若有NaOH溶液溅出,测定结果将___________(填“偏高”或“偏低”)
-
氮化镁(Mg3N2)在工业上应用广泛,通常条件下为黄绿色粉末,极易与水反应,常用作接触媒。
I.氮化镁的制备 下面是甲、乙两位学生提出的制备氮化镁的实验方案示意图(实验前系统内的空气已排除。图中箭头表示气体的流向)。
甲. 
乙. 
(1)Mg3N2的电子式为___________,甲同学的实验方案不能顺利制得氮化镁,原因为________ (用化学方程式表示)。
(2)乙同学方案中NaOH固体的作用为_____________________________________________。
(3)丙同学利用空气中含有大量N2的事实,用以下装置设计了另外一种制备氮化镁的方案 (夹持装置略去):
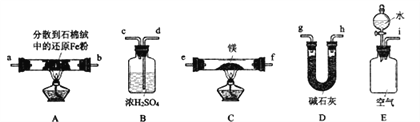
①按气流由左到右的方向,上述装置合理的连接顺序为____________(填接口字母);
②装置B的作用为___________,装置D的作用为__________________________。
Ⅱ.定性分析产物
| 操作步明 | 实验现象 | 解释原因 |
| 取少量产品于试管中,加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | (4)反应的化学方程式为___________ |
| . |
| 弃去上层淸液,加入足量稀盐酸 | 观察到固体全部溶解,且有气泡冒出 | (5)气泡冒出的原因为_____________ |
Ⅲ.定量测定氮化镁纯度
i.称取4.0 g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00 mol/L盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00 mL稀释后的溶液,用0.2 mol/L NaOH标准溶液滴定过量的盐酸,达到终点时消耗标准溶液25.00 mL。
(6)产物中氮化镁的质量分数为_______________。
-
氮化镁(Mg3N2)是工业上应用广泛的离子化合物,通常条件下为黄绿色的粉末,极易与水反应,常用作接触媒。
I.氮化镁的制备
下面是甲、乙两位学生提出的制备氮化镁的两种实验方案示意框(实验前系统内的空气已排除, 图中箭头表示气体的流向)。
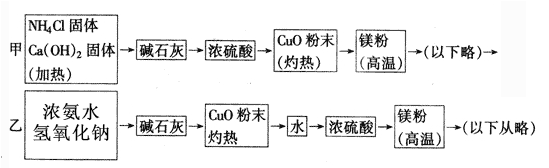
(1)Mg3N2的电子式为__________________。
(2)请结合化学方程式分析乙同学方案中氢氧化钠的作用:_____________________________。
(3)上述方案中,可制得氮化镁的方案为________________。
(4)丙同学利用空气中含有大量N2的事实,用以下装置设计了另外一种制备氮化镁的方案(夹持装置略去):
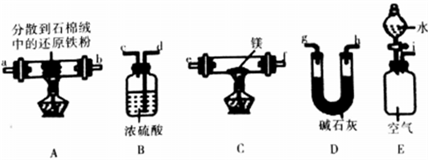
①按气流由左到右的方向,上述装置合理的连接顺序为____________________(填装置字母)。
②装置D的作用为__________________。
Ⅱ.定性分析产物
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量产品于试管中,加足量蒸馏水 | 试管底部有固体不溶物,有刺激性气味的气体产生 | (5)写出反应的化学方程式__________________________ |
| 弃去上层清液,加入足量稀盐酸 | 观察到固体全部溶解且冒气泡 | (6)冒气泡的原因___________ |
Ⅲ.定量测定氮化镁纯度
i.称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL1.00mol/L盐酸中,充分反应后,将所得溶液稀释到200.00mL
ii.取20.00 mL稀释后的溶液,用0.2 mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25.00 mL
(7)所取固体中氮化镁的质量分数为____________________。
-
SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
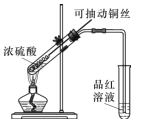
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
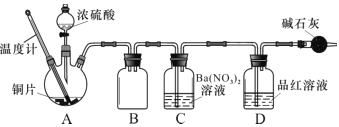
实验记录 A 中现象如下:
| 序号 | 反应温度/℃ | 实验现象 |
| 1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
| 2 | 158 | 黑色固体产生的同时,有气体生成 |
| 3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
| 4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
| 5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
-
SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
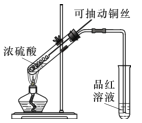
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
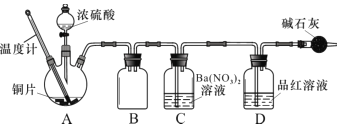
实验记录 A 中现象如下:
| 序号 | 反应温度/℃ | 实验现象 |
| 1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
| 2 | 158 | 黑色固体产生的同时,有气体生成 |
| 3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
| 4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
| 5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。














