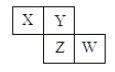四种短周期元素在周期表中的相对位置如下所示,其中Y元素原子最外层电子数是其电子层数的3倍。
请回答下列问题:
(1)元素W的最高价氧化物对应的水化物的化学式为 ;
(2)这些元素的氢化物中,水溶液碱性最强的化合物是 (写化学式);
(3)X、Y、Z、W形成的简单阴离子半径大小顺序为 (用离子符号填空);证明W的非金属性比强Z的最简单方法是 (用化学方程式填空);
(4)Z的低价氧化物通入W的单质形成的水溶液中反应的化学方程式: ;
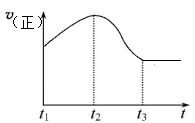
(5)Z的低价氧化物能与Y的单质在一定体积的密闭容器反应,该反应属于 (填“可逆反应”或“非可逆反应”),反应速率与时间关系如图所示,t1到t2反应速率逐渐加快的原因是 ,在 (填“t1”“t2”或“t3”)时达到平衡;对该反应,下列说法正确的是 。
A.Y的单质是氧化剂
B.混合气体的密度不再改变,可以判断反应达到平衡状态
C.Z的低价氧化物能使品红褪色
D.反应达到平衡状态时,反应停止
(6)将一定量的W单质通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaW、NaWO、NaWO3共存体系,则消耗的W单质的物质的量为 。
高一化学简答题极难题