-
菱铁矿主要成分是碳酸亚铁(FeCO3),是一种分布广泛的矿物。某同学对碳酸亚铁和氧气充分反应后的固体成分进行了如下探究。
(查阅资料)① FeCO3在空气中加热生成铁的氧化物和二氧化碳。
②FeO是一种黑色粉末,在空气中加热,能迅速被氧化成四氧化三铁。Fe2O3能与盐酸反应生成氯化铁和水。Fe3O4能与盐酸反应生成氯化亚铁、氯化铁和水。
③酸性条件下,FeCl2能使高锰酸钾溶液褪色。向FeCl3溶液中滴加KSCN溶液,溶液变红色。
(猜想与假设)
猜想1:固体成分是Fe2O3 猜想2:固体成分是Fe3O4 猜想3:固体成分是FeO
(进行实验)
利用如图装置进行实验(加热和固定装置已略去,装置气密性良好)。

打开弹簧夹K,通入氧气,加热FeCO3。当瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。取玻璃管里的少量固体于试管中,滴加过量盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验。
| 实验编号 | 实验步骤 | 实验现象 |
| a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
| b | 向乙溶液中滴加高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(解释与结论)
(1)在实验前就可以判断猜想________(填“1”“2”或“3”)不成立,因为___________。
(2)实验 b 的目的是_____________,由实验a、b的现象可知,猜想__________(填“1”“2”或“3”)成立,则FeCO3与氧气在加热时反应的化学方程式为________________。
(3)该同学反思后发现,不做实验a也能得出相同的结论,理由是___________________。
(拓展与应用)
(4)氧化铁是铁锈的主要成分,写出用盐酸除铁锈的化学方程式______________。
-
要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与华雪同学的探究:
【查阅资料】
①碳酸亚铁(FeCO3)具有还原性,在空气中灼烧生成的氧化物和CO2气体。
②FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水。
③FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色。
【猜想与假设】
猜想1:固体成分是氧化铁。
猜想2:固体成分是四氧化三铁。
猜想3: 。
【活动与探究】
连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X。当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。
取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验:
| 实验编号 | 实验步骤 | 实验现象 |
| a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
| b | 向乙溶液中滴加高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
【结论与反思】
(1)由上述实验现象可知,FeCO3在氧气中高温灼烧得到的固体产物是 ,因此,猜想 (填“1”或“2”或“3”)是正确的。
(2)FeCO3在氧气中高温灼烧的化学方程式为 。
(3)上述实验 (填“a”或“b”)是多余的,因为 。
【总结与提升】
(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙.碳酸氢钙的化学式为 。
(2)CO2使澄清石灰水变浑浊的化学方程式为 。
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到 ,就不能确定哪个猜想是正确的。所以华雪同学又对该实验进行了定量探究:取11.6g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6g。通过计算即可确定:FeCO3和氧气充分反应后的固体成分是 。

-
碳酸亚铁(FeCO3)是一种重要的工业盐,也是炼铁所用菱铁矿的主要成分,外观为白色固体,难溶于水,遇水和氧气会发生反应,化学方程式为4FeCO3+6H2O+O2=4Fe(OH)3+4CO2.
(1)小亮同学提出三种生成碳酸亚铁的情况,其中正确的是(填序号)______
A.+3价铁的盐溶液与可溶性碳酸盐发生复分解反应;B.+2价铁的盐溶液与可溶性碳酸盐作用;C.铁与氧气、水发生复杂的氧化反应
(2)小亮同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后(不考虑水分蒸发),观察到天平的指针会______(填“偏左”、“偏右”、“不发生偏转”之一);另外,放置过程中还可观察到的一项实验现象为______.
(3)待上述烧杯中物质的质量不发生变化时,向烧杯中加入溶质质量分数为10%的稀盐酸109.5g,恰好完全反应,求反应后所得不饱和溶液中溶质的质量.(计算结果精确到0.01g)
-
为测定菱铁矿石中碳酸亚铁FeCO3的含量(假设其中杂质的成分不溶于水,也不参加反应),某化学小组进行如下的实验,请回答下列问题:
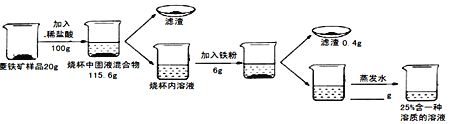
(1)用36.5%的浓盐酸配制100 g 14.6%的稀盐酸加入水的质量是 _________;
(2)写出菱铁矿石中加盐酸的化学反应方程式 ________________________;
(3)列出该菱铁矿石中发生反应的物质的质量(x)的比例式 _____________;
(4)该菱铁矿石中碳酸亚铁的含量是 ___________________ ;
(5)最终烧杯中溶液中溶质的质量分数为25%,则过滤后需蒸发水的质量是 ______________。
-
菱铁矿(主要成分是FeCO3)是炼铁的原料。现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。
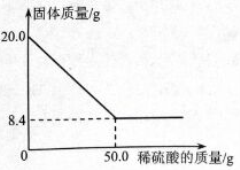
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O
②菱铁矿中杂质不参加反应,且难溶于水。
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。1%)
-
菱铁矿(主要成分是FeCO3)是炼铁的原料。现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。
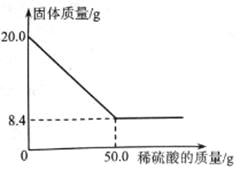
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O
②菱铁矿中杂质不参加反应,且难溶于水。
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。1%)
-
菱铁矿(主要成分是FeCO3)是炼铁的原料。现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。已知:
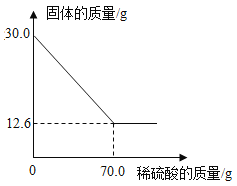
①FeCO3+H2SO4=FeSO4+CO2↑+H2O;②菱铁矿中杂质不参加反应,且难溶于水。请计算:
(1)30.0g菱铁矿中FeCO3的质量为__________g。
(2)所用稀硫酸的溶质质量分数(结果准确到0.1%)____________.
-
菱铁矿(主要成分是FeCO3)是炼铁的原料。现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。已知:
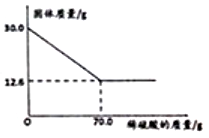
①FeCO3+H2SO4=FeSO4+CO2↑+H2O;②菱铁矿中杂质不参加反应,且难溶于水。请计算:
(1)30.0g菱铁矿中FeCO3的质量为__________g。
(2)所用稀硫酸的溶质质量分数(结果准确到0.1%)____________.
-
碳酸亚铁(FeCO3)是生产补血剂的原料.以下是某同学设计的利用铁矿烧渣(主要成分是Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
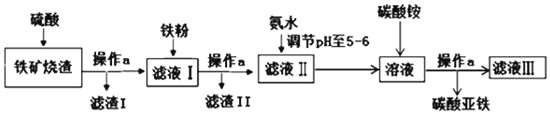
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和__.
(2)滤液Ⅰ中含有的金属阳离子:Fe2+、__ (填离子符号).
(3)滤液Ⅰ中加入铁粉后可能发生的化学反应方程式:①__;②Fe+H2SO4=FeSO4+H2↑.
(4)“调节滤液Ⅱ的pH”的操作用__测定加入氨水后溶液的pH.
(5)加入碳酸铵得到碳酸亚铁的反应化学方程式:__.
-
碳酸亚铁(FeCO3)是生产补血剂的原料。以下是某同学设计的利用铁矿烧渣(主要成分为Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
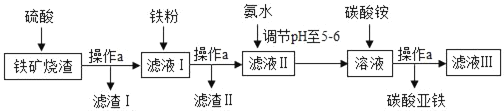
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和_____。
(2)加入过量稀硫酸前要将铁矿烧渣粉碎的目的是_____滤液I中含有的溶质是:FeSO4、_____(填化学式)。
(3)滤液Ⅰ中加入铁粉后可能发生的化学方程式:
①Fe+Fe2(SO4)3=3FeSO4
②_____。
(4)加入碳酸铵得到碳酸亚铁的反应化学方程式:_____。








