-
随着各地“限牌”政策的推出,电动汽车成为汽车界的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图所示。其中 A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导 Li+的高分子材料,隔膜只允特定的离子通过,电池反应式为:LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是( )
C6+LiCoO2。下列说法不正确的是( )
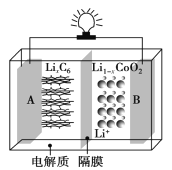
A. 该隔膜只允许 Li+通过,放电时 Li+从左边流向右边
B. 放电时,正极锂的化合价未发生改变
C. 充电时 B 作阳极,该电极放电时的电极反应式为 Li1-xCoO2+xLi++xe-=LiCoO2
D. 废旧钴酸锂(LiCoO2)电池进行“放电处理”让 Li+进入石墨中而有利于回收
-
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是
C6+LiCoO2。下列说法不正确的是
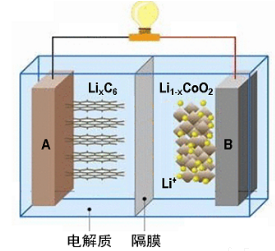
A.据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边流向右边
B.充电时,A为阴极,发生还原反应
C.放电时,B为正极,电极反应式为:Li1-x CoO2+ xLi++ xe-= LiCoO2
D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收
-
特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A极材料是金属锂和石墨的复合材料(石墨作为金属锂的载体),电解质中通过传导Li+实现导电,隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是( )
C6+LiCoO2。下列说法不正确的是( )
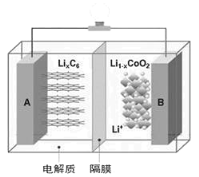
A.放电时,电子沿导线由A移向B,电解质溶液是含Li+的水溶液
B.充电时A为阴极,发生还原反应为C6+xLi++xe-=LixC6
C.放电时B为正极,电极反应式为Li1-xCoO2+xLi++xe-=LiCoO2
D.废旧钴酸锂(LiCoO2)电池进行“充电处理”使锂进入石墨中而有利于回收
-
2019年诺贝尔化学奖颁给了对锂离子电池研发作出卓越贡献的三位科学家。笔记本电脑的电池常用钴酸锂电池,其工作原理如下图所示,总反应为LixC6+Li1-xCoO2  C6+LiCoO2。下列说法不正确的是( )
C6+LiCoO2。下列说法不正确的是( )

A.放电时,LixC6做负极,发生氧化反应
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阳极的电极反应式:LiCoO2-xe-=xLi++Li1-xCoO2
D.充电时,当导线中传递1mol电子,理论上将有1mol Li+向B极移动
-
中国在2009年推出了国产燃料电池概念汽车,该车装有“绿色心脏”——质子交换膜燃料电池.如图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )

A.工作时“X极”周围溶液的酸性增强
B.氢气在电极上发生还原反应
C.图中标出的“Y极”实际是原电池的负极
D.工作过程中,质子(H+)从“Y极”一边透过质子交换膜移动到“X极”一边与OH-反应生成水
-
华为研发人员利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1﹣xCoO2C6+LiCoO2,其主要优势在于使用寿命长和充电速度快,其工作原理如图所示。下列关于该电池的说法错误的是( )
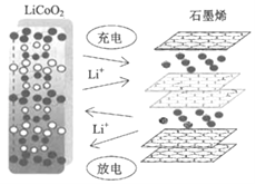
A.该电池若用隔膜,可选用阳离子交换膜
B.充电时,阴极反应为C6+xLi++xe﹣=LixC6
C.放电时,LiCoO2极发生的电极反应为:LiCoO2﹣xe﹣=Li1﹣xCoO2+xLi+
D.废旧的该电池进行“放电处理”,让Li+嵌入 LiCoO2中有利于回收石墨烯
-
现代生产、生活和国防中大量使用电池。如照相机、手机、汽车、卫星等均要使用电池。了解常见电池的工作原理是中学生的必修课之一。请同学们用所学知识回答以下问题。
(1)铅蓄电池放电时的总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O。请写出放电时正极反应的电极反应式:_________________________。
(2)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。
①请在图中标出电极材料及电解质溶液(写化学式)①___________,②____________,③_______________,④__________________
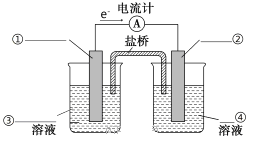
②盐桥中装有含琼胶的KCl饱和溶液,电池工作过程中盐桥中的Cl-向________极移动(填“左”或“右”)。
(3)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。
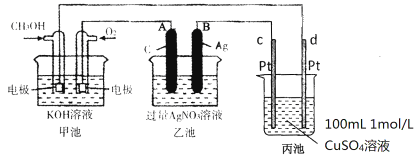
①A(石墨)电极的名称是_______________。
②通入CH3OH的电极的电极反应式是________________________________。
③乙池中反应的化学方程式为________________________________________。
④当电路中通过0.01mol电子时,丙池溶液的c(H+) = __________mol/L(忽略电解过程中溶液体积的变化)。
-
锂离子电池的正极材料是含锂的钴酸锂(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,用LiC6表示。电池反应为CoO2+LiC6 LiCoO2+C6,下列说法正确的是( )
LiCoO2+C6,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e-=Li++C6
B.放电时,电池的正极反应为CoO2+Li++e-=LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
-
钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
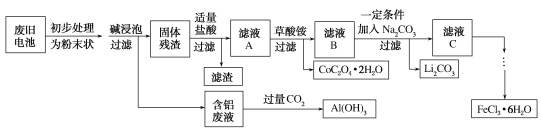
已知:还原性:Cl−>Co2+;
回答下列问题:
(1)废旧电池初步处理为粉末状的目的是___________。
(2)从含铝废液得到Al(OH)3的离子方程式为________。
(3)滤液A中的溶质除HCl、LiCl外还有FeCl3、CoCl2。写出LiCoO2和盐酸反应的化学方程式_______。
(4)滤渣的主要成分为______(填化学式)。
(5)已知Li2CO3的溶度积常数Ksp=8.64×10−4,将浓度为0.02mol·L−1的Li2SO4和浓度为0.02 mol·L−1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L−1。
(6)从FeCl3溶液得到FeCl3·6H2O固体的操作关键是________。
-
2006年巴黎车展示上,世界各大汽车商纷纷推出环保动力小汽车,使用的新型环保电池为( )
A.氢氧燃料电池
B.锌锰电池
C.镍镉电池
D.铅蓄电池
C6+LiCoO2。下列说法不正确的是( )








