-
定量研究是科学研究的重要方法之一,利用它可以解决许多生产生活中的实际问题。
⑴将20g质量分数为4%的氢氧化钠溶液与7.3g稀盐酸混合,恰好完全反应,所得溶液的PH为7,试计算所用稀盐酸的溶质质量分数。
⑵实验室浓盐酸(分析纯)的溶质质量分数在36%-38%之间为合格药品。(1)题中的稀盐酸是用一定体积(折算成质量为2g)的浓盐酸(分析纯)加水配制而成的。通过计算判断该浓盐酸是否为合格药品。(只写结果,不写计算过程)
九年级化学计算题困难题查看答案及解析
-
定量研究是科学研究的重要方法之一,利用它能解决许多生产、生活中的实际问题.
(1)将20g质量分数为4%的氢氧化钠溶液与7.3g稀盐酸混合,恰好完全反应,所得溶液的pH为7.试计算所用稀盐酸溶质质量分数.
(2)实验室浓盐酸(分析纯)的溶质质量分数在36%~38%之间为合格药品.(1)题中的稀盐酸是用一定体积(折算成质量是2g)的浓盐酸(分析纯)加水配制而成的.通过计算判断该浓盐酸是否为合格药品.九年级化学解答题中等难度题查看答案及解析
-
定量研究是科学研究的重要方法之一,利用它能解决许多生产生活中的实际问题。
(1)将20g质量分数为4%的氢氧化钠溶液与7.3g稀盐酸混合,恰好完全反应,所得溶液的pH为7,试计算所用稀盐酸的溶质质量分数为_______________。
(2)实验室浓盐酸的溶质质量分数在36%~38%之间为合格药品。(1)题中的稀盐酸是用质量为2g的浓盐酸加水配制而成的。请通过计算判断该浓盐酸是否为合格药品。______________
九年级化学计算题困难题查看答案及解析
-
某工厂化验室为了测定一定量石油产品中所含硫酸的质量分数,向20g溶质质量分数为4%的氢氧化钠溶液中,不断滴加含少量硫酸的石油产品(其它成分不与氢氧化钠反应),测定过程中溶液的pH随所滴加溶液质量的变化关系图。根据图中数据,计算这种石油产品中所含硫酸的质量分数。
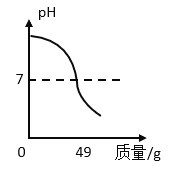
九年级化学计算题简单题查看答案及解析
-
(6分)实验室有4%的氢氧化钠溶液200g,并用此溶液测定某盐酸溶液的溶质质量分数。
(1) 恰好完全反应时,消耗4%的氢氧化钠溶液20g和25g某质量分数盐酸溶液,试计算该盐酸溶液中溶质的质量分数为多少?
(2)用配得的氢氧化钠溶液与待测溶质质量分数的盐酸溶液反应,实验过程中溶液的pH变化曲线如图所示,那么a点对应的溶液中,在单位体积中微粒数目最多的是 (填写化学符号)。

(3)将b点对应的溶液放在蒸发皿中慢慢地蒸干,所得的固体中除了NaCl外,还可能含有__ ____ _(写化学式)
九年级化学计算题困难题查看答案及解析
-
溶液在日常生活、工农业生产和科学研究中具有广泛的应用。下图是某同学在实验室配制氯化钠溶液的操作示意图,请结合相关知识,回答问题:
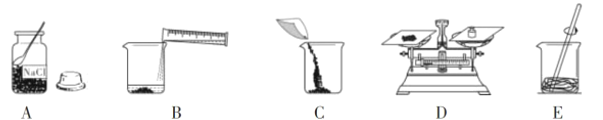
(1)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是_____(填序号)。
(2)已知20 °C时NaCl的溶解度是36g。该温度下,若将30 gNaCl放入50 g水中,充分溶解,溶液的溶质质量分数为_____,形成的是_____。(填“饱和”或“不饱和”)溶液。
九年级化学实验题中等难度题查看答案及解析
-
(7分)质量守恒定律是重要的三大定律之一,应用它可以帮助我们解决许多生产、科学实验和生活上的问题。现有氯酸钾和二氧化锰的混合物共26.5 g,加热使之反应,待反应至不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g.求:
(1)制取氧气的质量共为___________ g。(2分);
(2)原混合物中氯酸钾多少克?(写出解题过程)(5分)
九年级化学计算题中等难度题查看答案及解析
-
质量守恒定律是重要的三大定律之一,应用它可以帮助我们解决许多生产、科学实验和生活上的问题.现有氯酸钾和二氧化锰的混合物共26.5g,加热使之反应,待反应至不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g.求:
(1)制取氧气的质量共为______ g.(2分);
(2)原混合物中氯酸钾多少克?(写出解题过程)九年级化学解答题中等难度题查看答案及解析
-
将40g稀盐酸逐滴加入到20g溶质质量分数为4%的氢氧化钠溶液中并搅拌,随着稀盐酸的滴加,溶液的pH变化如图所示,请计算:此盐酸的溶质质量分数(精确到0.01%)。
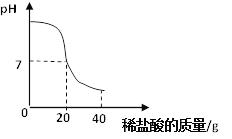
九年级化学计算题中等难度题查看答案及解析
-
某工厂化验室为检验石灰石的纯度,取6g样品(不含碱性杂质)粉碎后放入烧杯中,加入120g溶质的质量分数为3.65%的盐酸,生成的气体全部放出后,发现尚需20g溶质的质量分数为4%的氢氧化钠溶液去中和多余的盐酸.求石灰石中碳酸钙的质量分数.
九年级化学解答题中等难度题查看答案及解析