25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示,下列说法正确的是( )
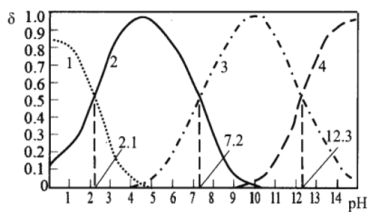
A. 曲线1和曲线2分别表示δ(H3PO4)和δ(HPO42-)的变化
B. 25℃时,H3PO4的电离常数K1=10-2.1
C. pH=7.2时,溶液中c(H2PO4ˉ)+c(HPO42-)+c(OHˉ)=c(Na+)+c(H+)
D. pH=12.3时,溶液中由水电离出的c(H+)=10-12.3mol/L
高二化学单选题困难题
25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示,下列说法正确的是( )

A. 曲线1和曲线2分别表示δ(H3PO4)和δ(HPO42-)的变化
B. 25℃时,H3PO4的电离常数K1=10-2.1
C. pH=7.2时,溶液中c(H2PO4ˉ)+c(HPO42-)+c(OHˉ)=c(Na+)+c(H+)
D. pH=12.3时,溶液中由水电离出的c(H+)=10-12.3mol/L
高二化学单选题困难题
25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示,下列说法正确的是( )

A. 曲线1和曲线2分别表示δ(H3PO4)和δ(HPO42-)的变化
B. 25℃时,H3PO4的电离常数K1=10-2.1
C. pH=7.2时,溶液中c(H2PO4ˉ)+c(HPO42-)+c(OHˉ)=c(Na+)+c(H+)
D. pH=12.3时,溶液中由水电离出的c(H+)=10-12.3mol/L
高二化学单选题困难题查看答案及解析
25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如图所示:下列说法正确的是( )
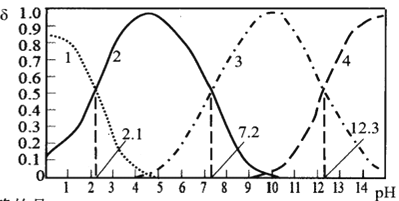
A.pH=7.2时,溶液中c(H2PO4ˉ)+c(HPO42-)+c(OHˉ)=c(Na+)+c(H+)
B.曲线1和曲线2分别表示δ(H3PO4)和δ(HPO42-)的变化
C.pH=12.3时,溶液中由水电离出的c(H+)=10-12.3mol/L
D.25℃时,H3PO4的电离常数K1=10-2.1
高二化学单选题中等难度题查看答案及解析
25℃时,向20mL0.1mol·L-1H3PO2溶液中滴加0.1mol·L-1的NaOH溶液,滴定曲线如图1,含磷微粒物质的量浓度所占分数(δ)随pH变化关系如图2。下列说法不正确是
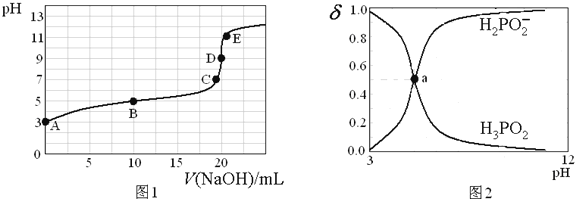
A. H3PO2的电离方程式为H3PO2H2PO2-+H+ Ka≈10-5
B. B点时,溶液中存在关系:2c(H+)+c(H2PO2-)=2c(OH-)+c(H3PO2)
C. C点时,溶液中存在关系:c(Na+)+c(H+)=C(H2PO2-)+c(OH-)
D. D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
高二化学单选题困难题查看答案及解析
25℃时,向20mL0.1mol·L-1H3PO2溶液中滴加0.1mol·L-1的NaOH溶液,滴定曲线如图1,含磷微粒物质的量浓度所占分数(δ)随pH变化关系如图2。下列说法不正确是
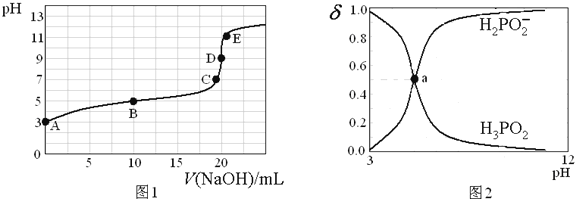
A. H3PO2的电离方程式为H3PO2H2PO2-+H+ Ka≈10-5
B. B点时,溶液中存在关系:2c(H+)+c(H2PO2-)=2c(OH-)+c(H3PO2)
C. C点时,溶液中存在关系:c(Na+)+c(H+)=C(H2PO2-)+c(OH-)
D. D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
高二化学单选题困难题查看答案及解析
H2R为二元弱酸,向一定体积的0.1mol/L的H2R溶液中逐滴加入一定浓度的NaOH溶液,溶液中不同形态的粒子(H2R、HR-、R2-)的物质的量分数a(X)随pH的变化曲线如图所示[a(X)=c(X)/[c(H2R)+c(HR-)+c(R2-)]]。下列说法错误的是
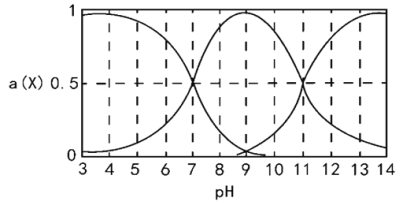
A. 常温下,K2(H2R)=1.0×10-11
B. 常温下,HR-在水中的电离程度大于其水解程度
C. pH=9时, c(Na+)>c(HR-)+2c(R2-)
D. pH=7时,c(H2R)=c(HR-)
高二化学单选题中等难度题查看答案及解析
若向25mLNaOH溶液中逐滴加入0.2mol/LCH3COOH溶液过程中溶液pH的变化曲线如图所示。
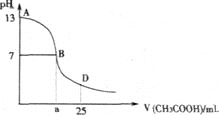
(1)该NaOH溶液的物质的量浓度为_________________。
(2)a____12.5mL(填“>”,“<”或“=”),若由体积相等的氢氧化钠和醋酸溶液混合而且恰好呈中性
(3)在D点溶液中各离子浓度由大到小顺序为_____________________ .
高二化学填空题中等难度题查看答案及解析
298K时,在H3PO4溶液中滴入NaOH溶液,溶液中H3PO4、H2PO4-、HPO42-、PO43-的物质的量分数δ(X)随pH的变化如图所示。下列叙述错误的是
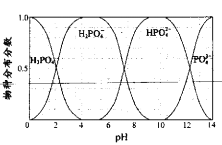
A. K(H3PO4)的数量级为10-8
B. Na2HPO4溶液中:c(PO43-) <c(H2PO4-)
C. pH=7时c(H2PO4-)>c(HPO42-)
D. NaH2PO4溶液显碱性
高二化学单选题中等难度题查看答案及解析
25℃时,草酸溶液中部分微粒的物质的量浓度随NaOH溶液的加入pH 的变化如图所示。其中c (H2C2O4) +c (HC2O4-)+ c (C2O42-)=0.1mol/L,下列说法不正确的是
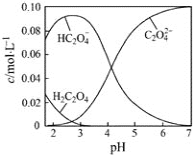
A. H2C2O4的Ka2数量级为10-5
B. NaHC2O4溶液中,c (Na+)>c(HC2O4-)>c (H+)>c (OH-)
C. 0.1mol/L 的H2C2O4溶液,H2C2O4的电离度为80%
D. pH=7.0的溶液中,c (Na+)=0.1 + c(C2O42-) - c (H2C2O4)
高二化学单选题困难题查看答案及解析
已知H2A为二元弱酸,20℃时,配制一组c(H2A)+c(HA-)+c(A2-)=0.100mol/L的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法错误的是
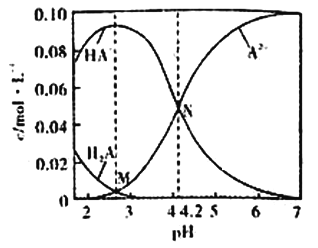
A.Ka2(H2A)的数量级为10-5
B.NaHA溶液中:c(H+)>c(OH-)
C.M点由水电离出的c(H+)>N点由水电离出的c(H+)
D.pH=7的溶液中:c(Na+)>2c(A2-)
高二化学单选题困难题查看答案及解析
已知H2A为二元弱酸,20℃时,配制一组c(H2A)+c(HA-)+c(A2-)=0.100mol/L的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法错误的是
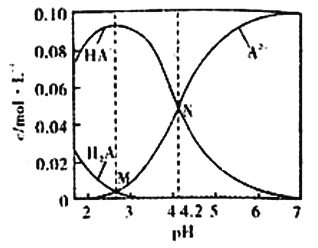
A. Ka2(H2A)的数量级为10-5
B. NaHA溶液中:c(H+)>c(OH-)
C. M点由水电离出的c(H+)>N点由水电离出的c(H+)
D. pH=7的溶液中:c(Na+)>2c(A2-)
高二化学单选题困难题查看答案及解析