-
用所学知识填写下列空白:(填代号)
(1)下列物质:①金属铜 ②固态NaCl ③液氧 ④盐酸 ⑤碳棒 ⑥酒精 ⑦KOH水溶液 ⑧熔融状态的KNO3 ⑨葡萄糖 ⑩天然气
属于电解质的是__________;属于非电解质是__________;能导电的化合物是__________。
(2)常温下,将1mLpH=1的H2SO4的溶液加水稀释到100mL,稀释后的溶液中c(SO42-)∶c(OH-) =_______________;
(3)某温度时,测得0.01 mol•L-1 NaOH溶液的pH为11,则该温度下水的离子积常数Kw=______。在该温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合.若所得混合液为中性,且a=12,b=2,则Va:Vb=______。
高二化学填空题困难题查看答案及解析
-
(15分)(1)从NaCl、CuSO4两种电解质中选取适当的物质,按电解要求填写(填化学式):
①以铜为电极,进行电解时电解质浓度不变,则采用的电解质是__________。
②以碳棒为电极,进行电解时使电解质和水的质量均变小,则采用的电解质是________。
此电解反应的阳极反应式: ,电解池的总反应化学方程式: 。
(2)①甲同学用直流电源、碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)===CuSO4+H2↑,则该同学选用的阳极材料是_______。
②乙同学在做铜与稀硫酸的上述反应实验时,看到碳棒和铜棒上都有气泡产生,但铜棒却没有被腐蚀。请你选出最可能的原因 (填字母代号)
A.铜被稀硫酸钝化 B.碳棒和铜棒与电源正负极接反
此时的电解池的总反应为____________ ____________
高二化学填空题困难题查看答案及解析
-
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第 周期、第 族 ;
(2)写出反应①的化学方程式 ;
(3)写出反应④的离子方程式 ;
(4)写出反应③的电极方程式:
阳极: 阴极:
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是 。(填序号)
高二化学推断题中等难度题查看答案及解析
-
现有八种物质:①干冰 ②碳化硅 ③氮化硼 ④晶体硫 ⑤过氧化钠 ⑥二氧化硅晶体 ⑦氯化铵 ⑧氖。请用编号填写下列空白。
(1)固态时属于原子晶体的是________________________
(2)固态时属于分子晶体的是________________________
(3)属于分子晶体,且分子为直线形的是______________
(4)由单原子分子构成的分子晶体是__________________
(5)通过极性键形成的原子晶体是_____________________
高二化学填空题简单题查看答案及解析
-
根据所学知识填写下列空白。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =__________________。
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式____________________________________________。
(3)某温度下纯水中的c(H+) = 1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)= 5×10-5mol/L,则由水电离出的c(H+) =__________mol/L。
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=_________。
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-, HB-
H++B2-。
已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是____________________________________。
高二化学综合题中等难度题查看答案及解析
-
下图每一方框中的字母代表一种反应物或生成物:

产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(l)L的化学式为:__________________
(2)用电子式表示F的形成过程__________________________________
(3)写出E+F+L=J+I+H反应的离子方程式:________________________
(4)H和G之间反应的化学方程式为:_______________________________,每生成2.4克的D转移______ mol电子。
高二化学推断题中等难度题查看答案及解析
-
(一)下列物质:①Fe ②CO2③酒精④ NaHSO4⑤ Ba(OH)2⑥熔融 NaCl ⑦AgCl ⑧NaHCO3⑨ H2S。(填代号,以下同)
(1)属于盐的是__________。
(2)属于电解质的是___________。
(3)属于非电解质的是________。
(二)完成下列填空:
(1)28g氮气含有的原子数为___________个。
(2)9.03×1023个H2O分子所含氧原子数的物质的量为__________mol;与________克CO2中所含氧原子数相等。
(3)19 g某二价金属的氯化物ACl2中含有0.4mol Cl-,则A的摩尔质量为__________。
(4)在一定温度和压强下,10mL气体A2跟15mL的气体B2完全化合生成气体A2B3,则该气体在相同条件下的体积为______________mL。
高二化学综合题中等难度题查看答案及解析
-
某学生用已知物质的量浓度的标准盐酸测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制500mL溶液。除烧杯、量筒、胶头滴管和玻璃棒外,还需要的玻璃仪器是___________。取用25.00mL待测液时需要的仪器是_____________。
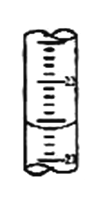
(2)滴定过程中,在锥形瓶底垫一张白纸的作用是_______________;若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图(上面数字:22,下面数字:23)。,则此时消耗标准溶液的体积为_________mL
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是________。
A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
(4)用标准盐酸滴定上述待测NaOH溶液时,判定滴定终点的现象是:直到加入最后一滴盐酸,_____________________________为止。
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数
待测NaOH溶液的体积/mL
0.1000mol/L盐酸的体积/mL
滴定前刻度
滴定后刻度
溶液体积/mL
第一次
25.00
0.00
26.28
26.28
第二次
25.00
1.55
31.30
29.75
第三次
25.00
0.20
26.42
26.22
计算该NaOH溶液的物质的量浓度:c(NaOH)=__________mol/L。(保留四位有效数字)
高二化学实验题中等难度题查看答案及解析
-
某学生用已知物质的量浓度的标准盐酸测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制500mL溶液。除烧杯、量筒、胶头滴管和玻璃棒外,还需要的玻璃仪器是___________。取用25.00mL待测液时需要的仪器是_____________。
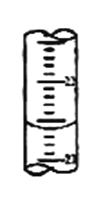
(2)滴定过程中,在锥形瓶底垫一张白纸的作用是_______________;若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图(上面数字:22,下面数字:23)。,则此时消耗标准溶液的体积为_________mL
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是________。
A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
(4)用标准盐酸滴定上述待测NaOH溶液时,判定滴定终点的现象是:直到加入最后一滴盐酸,_____________________________为止。
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数
待测NaOH溶液的体积/mL
0.1000mol/L盐酸的体积/mL
滴定前刻度
滴定后刻度
溶液体积/mL
第一次
25.00
0.00
26.28
26.28
第二次
25.00
1.55
31.30
29.75
第三次
25.00
0.20
26.42
26.22
计算该NaOH溶液的物质的量浓度:c(NaOH)=__________mol/L。(保留四位有效数字)
高二化学实验题中等难度题查看答案及解析
-
(17分)Ⅰ:现有如下物质:①酒精、②铜、③氢氧化钡、④氨气、⑤蔗糖、 ⑥高氯酸、⑦碳酸氢钠、⑧磷酸、⑨硫化氢、⑩Al2(SO4)3。请用物质的序号填写下列空白
(1)属于强电解质的有: 。
(2)液态时能导电且为物理变化的有: 。
(3)⑦在水溶液的电离方程式为 。
Ⅱ:A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。处理C物质可得到有价值的化学品,写出该化学品中的1种酸和1种盐的名称 、 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式 。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置是___ _____。写④反应离子方程 。
(4)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式 。
高二化学填空题困难题查看答案及解析