-
CH3OH是一种重要的化工原料,工业上可用合成气(CO和H2)来生产,主要副产物有CH4、C2H5OH等。已知生产CH3OH和副产物CH4的热化学方程式分别为
①CO(g)+2H2(g) CH3OH(g) △H=-90.7 kJ·mol-1
CH3OH(g) △H=-90.7 kJ·mol-1
②CO(g)+ 3H2(g) CH4(g)+H2O(g) △H=-206.2 kJ·mol-1
CH4(g)+H2O(g) △H=-206.2 kJ·mol-1
回答下面问题
(1)若CO(g)和CH3OH(g)的燃烧热△H分别为-283 kJ·mol-1和-726.1 kJ·mol-1,则H2(g)的燃烧热△H为 。
(2)下表列出了几种化学键断裂需要的能量数据。
| 化学键 | C≡O | H-H | C-H | H-O |
| 断裂1mol需要能量 / kJ | a | 436 | 414 | 463 |
则a= 。
(3)工业生产CH3OH过程中,提高合成CH3OH反应选择性的关键因素是 。
(4)下表列出了在一定条件下,在 3个1L容器中发生反应①时测得的一些数据。
3个1L容器中发生反应①时测得的一些数据。
| 容器序号 | 温度 / ℃ | 物质的起始浓度 / mol·L-1 | 物质平衡时浓度/ mol·L-1 |
| H2 | CO | CH3OH | CH3OH |
| Ⅰ | 100 | 0.2 | 0.1 | 0 | 0.02 |
| Ⅱ | 100 | 0.4 | 0.2 | 0.1 | |
| Ⅲ | 200 | 0 | 0 | 0.10 | b |
| | | | | |
① CO(g)+2H2(g) CH3OH(g)的平衡常数表达式为 ;
CH3OH(g)的平衡常数表达式为 ;
② 容器Ⅱ中,开始时,v(正) v(逆) (填“<、>、=”) ;
③ 容器Ⅲ中,达平衡时 b 0.02(填“<、>、=”) ;
④ 达到平衡时,正反应速率:容器Ⅲ中的比容器Ⅰ中的 (填“大、小、相等”)。
-
丙烯腈(CH2===CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2===CHCHO)和乙腈(CH3CN)等。回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+3/2O2(g)===C3H3N(g)+3H2O(g)ΔH=-515 kJ·mol-1
②C3H6(g)+O2(g)===C3H4O(g)+H2O(g)ΔH=-353 kJ·mol-1
有利于提高丙烯腈平衡产率的反应条件是__________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460 ℃。低于460 ℃时,丙烯腈的产率____(填“是”或“不是”)对应温度下的平衡产率,判断理由是________________;高于460 ℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
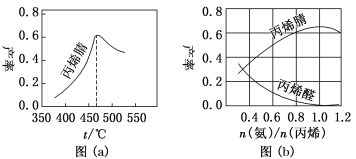
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为_____,理由是______________________________。进料气氨、空气、丙烯的理论体积比约为_________。
-
丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的 热化学方程式如下:
热化学方程式如下:
①C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
②C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________________;有利于提高丙烯腈平衡产率的反应条件是_____________;提高丙烯腈反应选择性的关键因素是___________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________________(填“是”或者“不是”)对应温度下的平衡
产率,判断理由是______________;高于460℃时,丙烯腈产率降低的可能原因是_____________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大

(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为 ,理由是_________________。进料气氨、空气、丙烯的理论体积比约为________________。
-
丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈CH3CN 等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯睛(C3H3N)和副产物丙烯醛(CH2=CHCHO)的热化学方程式如下:
① C3H6(g)+NH3(g)+O2(g)=C3H3N(g)+3H2O(g)△H=-515kJ/mol
② C3H6(g)+O2(g)=C3H4O(g)+H2O(g) △H=-353kJ/mol
有利于提高丙烯腈平衡产率的反应条件是______;提高丙烯腈反应选择性的关键因素是_____.
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是_____;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D. 反应活化能增大

(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为 _________ ,理由是_______。进料氨、空气、丙烯的理论体积约为____________。

-
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收akJ |
请回答:
①c1_____c2(填“>”、“<”或“=”);a=__________。
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是__________mol/(L·s)。
(2)压强为P1时,向体积为1L的密闭容器中充入bmol CO和2bmol H2,CO和氢气发生反应CO(g)+2H2(g) CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:
CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:

①该反应属于__________(填“吸”或“放”)热反应;P1__________P2(填“>”、“<”或“=”)。
②100℃时,该反应的平衡常数K=__________(用含b的代数式表示)。
(3)治理汽车尾气的反应是2NO(g)+2CO(g) 2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。
2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。

-
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。

(1)向体积为 2 L的密闭容器中充入1 mol CO和2 mol H2,在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g)。经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如右图所示。请回答:
CH3OH(g)。经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如右图所示。请回答:
① p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为_____________
② 图中压强p1 压强p2。(填“>”、“<” 或 “=” )
(2)一定温度下,在三个体积均为 1.0 L的恒容密闭容器中发生如下反应:2CH3OH(g)  CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
| 容器 编号 | 温度(℃) | 起始的物质的量(mol) | 平衡的物质的量(mol) |
| CH3OH(g) | CH3OCH3(g) | H2O(g) |
| I | 387 | 0. 20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| | | | |
①容器I中反应达到平衡所需时间比容器Ⅲ中的_________(填“长”、“短”或“相等”)
②达到平衡时,容器I中的CH3OH的体积分数_________(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数。
③若起始时向容器I中充入CH3OH 0.1 mol、CH3OCH3 0.15 mol和H2O 0.10 mol,则反应将向________方向进行(填“正反应”、“逆反应”或“不移动”)。
(3)一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。若反应在恒容绝热(不与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高。
CH3OH(g)+H2O(g)。若反应在恒容绝热(不与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高。
| 物质 | CO2 | H2 | CH3OH | H2O |
| 起始投料/ mol | 1 | 3 | 2 | 0 |
则升高温度,该反应的平衡常数将 (填“增大”“减小”或“不变”)。
-
“C化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH=-49.0 kJ/mol。相关数据如下:
CH3OH(g) + H2O(g) ΔH=-49.0 kJ/mol。相关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 1 mol CH3OH(g)和1 mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4 kJ | 吸收a kJ |
请回答:①c1 c2(填“>”、“<”或“=”);a= 。
②若甲中反应达到平衡耗时10 s,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是_____mol/(L·s)。
(2)向体积为1 L的密闭容器中充入b mol CO和2b mol H2,发生反应CO(g)+2H2(g) CH3OH(g)。平衡时CO的转化率与温度的关系如图所示。请回答下列问题:
CH3OH(g)。平衡时CO的转化率与温度的关系如图所示。请回答下列问题:

①正反应属于 (填“吸”或“放”)热反应。
②100℃时,该反应的平衡常数K= (用含b的代数式表示)。
(3)治理汽车尾气的反应是2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母)
2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母)

-
(8分)氨的合成是最重要的化工生产之一。
(1)工业上可用甲烷与水反应得到合成氨用的H2:其热化学反应方程式为
CH4(g)+H2O(g) CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示:
CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示:

则△H4=______________(用a、b、c表示)
(2)在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:
3H2(g)+N2(g) 2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 |
| 达到平衡的时间(min) | t | 5 |
| 平衡时N2的浓度(mol·L-1) | 3 | c |
①甲容器达到平衡所需要的时间t 5min(填“>”、“<”或“=”,下同);乙容器达到平衡时N2的浓度c 3 mol·L-1。
②下图中虚线为该反应在使用催化剂条件下,关于起始N2与H2投料比和H2平衡转化率的关系图。当其他条件完全相同时,用实线画出不使用催化剂情况下H2平衡转化率的示意图。

-
(8分)氨的合成是最重要的化工生产之一。
(1)工业上可用甲烷与水反应得到合成氨用的H2:其热化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示:
CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示:

则△H4=______________(用a、b、c表示)
(2)在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g) 2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 |
| 达到平衡的时间(min) | t | 5 |
| 平衡时N2的浓度(mol·L-1) | 3 | c |
①甲容器达到平衡所需要的时间t 5min(填“>”、“<” 或“=”,下同);乙容器达到平衡时N2的浓度c 3 mol·L-1。
②下图中虚线为该反应在使用催化剂条件下,关于起始N2与H2投料比和 H2平衡转化率的关系图。当其他条件完全相同时,用实线画出不使用催化剂情况下H2平衡转化率的示意图。

-
使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如下图:

(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇。
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)此流程的第I步反应为:C H4(g) + H2O(g)
H4(g) + H2O(g)  CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1_________P2。(填“<”、“>”或“=”)100℃时,将1 mol CH4和2 mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K=____________。
CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1_________P2。(填“<”、“>”或“=”)100℃时,将1 mol CH4和2 mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K=____________。

(3)此流程的第II步反应CO(g) + H2O(g)  CO2(g) + H2(g),
CO2(g) + H2(g),
的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500[ | 830 |
| 平衡常数K | 10 | 9 | 1 |
从上表可以推断:该 反应是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为 。
反应是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为 。
右图表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图中t2时刻发生改变的条件是____(写出一种)。

(4)某化学兴趣 小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是 。
小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是 。

CH3OH(g) △H=-90.7 kJ·mol-1
CH4(g)+H2O(g) △H=-206.2 kJ·mol-1
3个1L容器中发生反应①时测得的一些数据。
CH3OH(g)的平衡常数表达式为 ;
















