-
[s1] X、Y、Z、M是周期表前四周期中的四种常见元素,原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子最外层电子数是内层电子数的2倍
Y
基态原子最外层电子排布为
Z
与Y同周期,第一电离能小于Y
M
与X形成的合金为目前用量最多的金属材料
(1)Z位于周期表第________周期第族。Y、Z的氢化物稳定性较强的是________(写化学式)。
(2)X与氢可形成一种原子个数比为1:1的化合物,相对分子质量为78,该分子中存在________个
键。H—X、H—Y、H—Z三种共价键中,键长最长的是________。
(3)M元素基态原子的电子排布式是________。
(4)已知下列数据:
M(s)+
Z2(g) MZ(s) △H=-272.kJ·mol-1
2M(s)+
Z2(g) M2Z3(s) △H=-824.2.kJ·mol-1
MZ转化为M2Z3的热化学方程式是________
[s1]18.
高三化学填空题中等难度题查看答案及解析
-
(12分)X、Y、Z、M是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素
相关信息
X
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等
Y
常温常压下,Y单质是黄色固体,常在火山口附近沉积
Z
Z和Y同周期,Z的电负性大于Y
M
M的一种核素的质量数为63,中子数为34
(1)属于主族元素的原子半径从大到小的顺序是(写化学式,下同)________,Y和Z的最高价氧化物对应的水化物的酸性较强的是________,在H-Y、H-Z两种共价键中,键的极性较强的分子是________。
(2)XY2是一种常用的溶剂,XY2的电子式是________,XY2的分子中存在________个σ键。
(3)M位于周期表第____周期第________族,M的基态原子核外电子排布式是________;M2Y在空气中煅烧生成M2O的化学方程式是________。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+
O2(g)= XO2(g) △H = -283.0 kJ·mol-1
Y(g)+ O2(g)= YO2(g)△H = -296.0 kJ·mol-1
写出此反应的热化学方程式____________。
高三化学填空题中等难度题查看答案及解析
-
(12分)X、Y、Z、M是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素
相关信息
X
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等
Y
常温常压下,Y单质是黄色固体,常在火山口附近沉积
Z
Z和Y同周期,Z的电负性大于Y
M
M的一种核素的质量数为63,中子数为34
(1)属于主族元素的原子半径从大到小的顺序是(写化学式,下同)________,Y和Z的最高价氧化物对应的水化物的酸性较强的是________,在H-Y、H-Z两种共价键中,键的极性较强的分子是________。
(2)XY2是一种常用的溶剂,XY2的电子式是________,XY2的分子中存在________个σ键。
(3)M位于周期表第____周期第________族,M的基态原子核外电子排布式是________;M2Y在空气中煅烧生成M2O的化学方程式是________。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+
O2(g)= XO2(g) △H = -283.0 kJ·mol-1
Y(g)+ O2(g)= YO2(g)△H = -296.0 kJ·mol-1
写出此反应的热化学方程式____________。
高三化学填空题简单题查看答案及解析
-
A、B、C、D、E、F周表前四周期中的常见元素,其相关信息如下表:
元素 相关信息
A A是周期表中原子半径最小的元素
B B元素的原子价电子排布为ns11np14
C M的基态原子L层电子数是K层电子数的3倍
D D是第三周期中第一电离能最小的元素
E E是地壳中含量最多的金属元素
F 有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构
(1)F位于元素周期表中位置________,其基态原子核外价电子排布式为________;
(2)B的电负性比M的________(填“大”或“小”);B2A3分子中
键与
键与个数之比为________;
(3)写出E的单质与D的最高价氧化物的水化物溶液反应的化学方程式:________;
(4)已知每5.4gE可与最低价F的氧化物反应,放出346.2kJ的热量。则请写出该反应的热化学方程式:________。
高三化学填空题困难题查看答案及解析
-
A、B、C、D、E是元素周期表中前四周期中五种常见元素,其相关信息如下表:
元素 相关信息
A 原子核外L层电子数是K层的2倍
B 其一种单质被称为地球生物的“保护伞”
C 原子的第一电离能在第三周期中最小
D 基态原子最外层电子排布为(n+1)sn (n+1)p(n+2)
E 可形成多种氧化物,其中一种为具有磁性的黑色晶体
请回答下列问题:
(1)C在元素周期表中位于第________周期、第族;E的基态原子核外电子排布式是________
(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同)________,B、D的简单气态氢化物中稳定性较大的是________
(3)B、C的单质按物质的量比1:2形成的化合物中化学键的类型为 ________ ;该化合物属于 ________晶体。
(4)E的黑色磁性晶体发生铝热反应的化学方程式是________
(5)处理含AO、DO2烟道气污染的一种方法是将其在催化剂作用下转化为单质D。
已知:2AO(g)+ O2(g) =2AO2(g) ΔH=-566.0 kJ•mol-1
D(s)+ O2(g) = DO2(g) ΔH=-296.0 kJ•mol-1
此反应的热化学方程式是________ 。
高三化学填空题困难题查看答案及解析
-
A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:(NA为阿伏加德罗常数的值),请用化学用语回答下列问题:
元素
相关信息
A
基态原子的价电子排布式为nSnnPn
B
元素原子的核外p电子数比s电子数少1个
C
最外层电子数是电子层数的3倍
D
简单离子是第三周期元素中离子半径最小的
E
价电子层中的未成对电子数为4
(1)写出D元素在周期表的位置______,基态E2+价电子的排布图为_______,B元素能量最高的电子其轨道呈_______形。
(2)A与C形成的最高价化合物,中心原子轨道杂化类型为___________。
(3)A、B、C三种基态原子的第一电离能由大到小的顺序为_____________,B、C、D简单离子的半径由大到小的顺序为_________。
(4)写出C的核外有18个电子的氢化物的电子式________。
(5)E可用做某些反应的催化剂,CO易导致E失去催化活性:E+5CO = E(CO)5,E(CO)5熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为___________。
(6)已知沸点:B2H4>A2H6 ,主要原因为____________________。
(7)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________;设晶胞边长为a cm,该晶体的密度为________ g·cm-3(用含a和NA的式子表示)。

高三化学综合题中等难度题查看答案及解析
-
A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:(NA为阿伏加德罗常数的值),请用化学用语回答下列问题:
元素
相关信息
A
基态原子的价电子排布式为nSnnPn
B
元素原子的核外p电子数比s电子数少1个
C
最外层电子数是电子层数的3倍
D
简单离子是第三周期元素中离子半径最小的
E
价电子层中的未成对电子数为4
(1)写出D元素在周期表的位置______,基态E2+价电子的排布图为_______,B元素能量最高的电子其轨道呈_______形。
(2)A与C形成的最高价化合物,中心原子轨道杂化类型为___________。
(3)A、B、C三种基态原子的第一电离能由大到小的顺序为_____________,B、C、D简单离子的半径由大到小的顺序为_________。
(4)写出C的核外有18个电子的氢化物的电子式________。
(5)E可用做某些反应的催化剂,CO易导致E失去催化活性:E+5CO = E(CO)5,E(CO)5熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为___________。
(6)已知沸点:B2H4>A2H6 ,主要原因为____________________。
(7)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________;设晶胞边长为a cm,该晶体的密度为________ g·cm-3(用含a和NA的式子表示)。
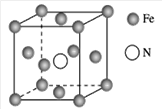
高三化学综合题中等难度题查看答案及解析
-
(15分)X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
元素
相关信息
X
X原子基态时最外层电子数是其内层电子数的2倍
Y
Y原子基态时2p原子轨道上有3个未成对的电子
Z
Z的基态原子最外层电子排布式为:nsnnpn+2
W
W的原子序数为29
(1)基态W原子的价电子排布式是_________________。
(2)X、Y、Z三种元素第一电离能从大到小的顺序是____________。(填化学式)
(3)Y的氢化物分子的空间构型是_______________;该氢化物分子中Y原子轨道的杂化类型是___________。
(4)X的气态氢化物 和Y的气态氢化物中沸点高的是________,(填化学式)其主要原因是。
(5)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为 ,每个Ba2+与 个O2-配位。
高三化学填空题简单题查看答案及解析
-
(15分)X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
元素
相关信息
X
X原子基态时最外层电子数是其内层电子数的2倍
Y
Y原子基态时2p原子轨道上有3个未成对的电子
Z
Z的基态原子最外层电子排布式为:nsnnpn+2
W
W的原子序数为29
(1)基态W原子的价电子排布式是_________________。
(2)X、Y、Z三种元素第一电离能从大到小的顺序是____________。(填化学式)
(3)Y的氢化物分子的空间构型是_______________;该氢化物分子中Y原子轨道的杂化类型是___________。
(4)X的气态氢化物 和Y的气态氢化物中沸点高的是________,(填化学式)其主要原因是________。
(5)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为 ,每个Ba2+与 个O2-配位。
高三化学填空题简单题查看答案及解析
-
A、B、C、D、E、F是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
元素
相关信息
A
可形成自然界硬度最大的单质
B
与A元素同周期,核外有三个未成对电子
C
最外层电子数是其电子层数的3倍
D
第一电离能至第四电离能分别是I1=578KJ/mol,I2=1817KJ/mol,I3=2745KJ/mol,
I4=11575KJ/mol
E
常温常压下,E的单质是固体,其氧化物是形成酸雨的主要物质
F
F的一种同位素的质量数为63,中子数为34
(1)A、B、C元素的第一电离能由大到小的顺序为 (用元素符号表示)。F的基态原子核外电子排布式为 。
(2)AE2是一种常用的溶剂,是 (填“极性”或“非极性”)分子,分子中σ键与π键个数比为 。
(3)写出D与NaOH溶液反应的离
子方程式 。DB形成的晶体与金刚石类似,它属于 晶体。B的最简单氢化物容易液化,理由是

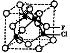
(4)已知F的晶体结构如图所示,又知F的密度为9.00g·cm-3,则晶胞边长为 ;FEC4常作电镀液,其中EC42-的空间构型是 ,其中E原子的杂化轨道类型是 。
(5)F的一种氯化物晶胞体结构如图所示,该氯化物的化学式是 。
高三化学填空题困难题查看答案及解析