-
25℃时,CH3COOH的电离常数Ka=1.8×10-5。常温下,往25ml氢氧化钠标准溶液中逐滴加入0.2 mol·L-1的CH3COOH溶液,pH变化曲线如下图所示:

(1)该氢氧化钠溶液的物质的量浓度为________mol·L-1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH-)=____ mol·L-1。
(3)B点所示溶液中,c(CH3COO-)-c(Na+)=_______________ mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=_______。
(4)C点所示溶液中,c(CH3COOH)_______c(CH3COO-)。(填“>”、“<”或“=”)
(5)向300 mL上述NaOH溶液中通入448 mL CO2(标准状况)气体,充分反应后,溶液中粒子浓度关系正确的是________.
A.c(Na+)+ c(H+)= c(OH-)+ c(HCO3-)+ c(CO32-)
B.2/3c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.c(Na+)> c(CO32-)> c(HCO3-)> c(OH-)> c(H+)
D.c(Na+)> c(HCO3-)> c(CO32-)> c(OH-)> c(H+)
高二化学填空题中等难度题查看答案及解析
-
已知亚磷酸(H3PO3)是具有强还原性的弱酸,可以被银离子氧化为磷酸。1摩尔亚磷酸最多消耗2摩尔氢氧化钠。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式__________。
(2)Na2HPO3是____(填“正盐”或“酸式盐”) 。
(3)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为______________。
(4)某温度下,0.10 mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2 mol•L-1,该温度下H3PO3的电离平衡常数K1=___________________;(结果保留两位有效数字)。
(5)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)_____c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”,下同);在NaH2PO3溶液中,c(H+)+c(H3PO3)_____c(HPO32-)+c(OH-)。
高二化学填空题中等难度题查看答案及解析
-
在一定温度下,醋酸溶液中存在电离平衡:CH3COOH
CH3COO- + H+
(1)某温度时,0.1 mol·L-1的醋酸溶液中的c(H+) 与0.01 mol·L-1 的醋酸溶液中的c(H+)的比值 ____(填“大于”“小于”或“等于”)10,理由是_________。
(2)常温下0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是:_____________。
A.c(H+) B.
C.c(H+)·c(OH−) D.c(OH−)/c(H+)
(3)现有pH均为3的醋酸、硫酸两瓶溶液:
①设两种溶液的物质的量浓度依次为c1、c2,则其关系式为_________(用“<”“>”或“=”表示,下同)。
②取相同体积的两种酸分别加入等体积的蒸馏水后,再分别加入少量等量的锌粉,反应开始时放出氢气的速率依次为v1、v2,则其关系式为_______,反应结束放出的氢气的体积依次为V1、V2,则其关系式为_____。
高二化学填空题中等难度题查看答案及解析
-
磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-、和PO43-四种粒子形式存在,当溶液的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化。下图是H3PO4溶液中,各种粒子的物质的量分数δ随pH的变化曲线:
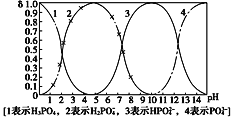
(1)向Na3PO4溶液中逐滴滴入稀盐酸,当pH从9降到6的过程中发生的主要反应的离子方程式为________。当pH=7时,溶液中主要存在的阴离子(OH-离子除外)是__________。
(2)从图中推断NaH2PO4溶液呈______性(填“酸”“碱”或“中”),其原因是_________。
(3)在Na3PO4溶液中,c(Na+)/c(PO43-)______3(填“>”“=”或“<”);向该溶液中滴入几滴浓KOH溶液后,c(Na+)/c(PO43-)的值减小,原因是____。
高二化学填空题中等难度题查看答案及解析
-
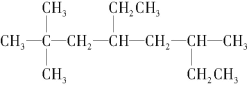
(1)有机物结构如图所示,用系统命名法命名,名称是_____;该烃的一氯代物有_____种。
(2)有机物结构如图所示,用系统命名法命名,名称是_____,将其在催化剂存在下完全氢化,所得烷烃用系统命名法命名,名称是_____。
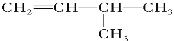
(3)现有 CH4、C2H4、C3H4、C2H6、C3H6 五种有机物。同质量的以上物质中,在相同状况下体积最大的是_____;同质量的以上物质完全燃烧时消耗 O2 的量最多的是_____;同质量的以上物质燃烧时,生成 H2O 的量最多的是_____;同状况、同体积的以上物质完全燃烧时消耗 O2 的量最多的是_____。
高二化学填空题中等难度题查看答案及解析
-
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+) ③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶液是__________,上述四种离子的浓度的大小顺序为__________(填序号)
(2)若上述关系中③是正确的,则溶液中的溶质为_______;若上述关系中④是正确的,则溶液中的溶质是______
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_________c(NH3·H2O)(填“大于”“小于”或“等于”)
高二化学填空题中等难度题查看答案及解析
-
(1)写出铜原子价电子排布式:______。与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有________(填元素符号)。
(2)第三周期第一电离能处于Al和P之间的元素有______种。
(3)某种原子的结构示意图为
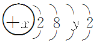 。则该原子的核电荷数x取值范围为______。
。则该原子的核电荷数x取值范围为______。(4)Cr在周期表中位于_____周期___族,属于___区,价电子排布图为______
(5)ClO4-互为等电子体的分子或离子为____。
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_____。
高二化学填空题中等难度题查看答案及解析
-
阿托酸甲酯是一种治疗肠道疾病的药物,是由阿托酸(
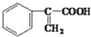 )和甲醇反应制得,完成下列填空:
)和甲醇反应制得,完成下列填空:(1)写出阿托酸甲酯的结构简式:________。
(2)A是比
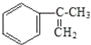 多两个碳原子且苯环上只有一个取代基的一种同系物,且A的所有碳原子可以处于同一平面上,写出A的结构简式____________。
多两个碳原子且苯环上只有一个取代基的一种同系物,且A的所有碳原子可以处于同一平面上,写出A的结构简式____________。(3)
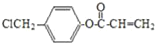 是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为_____________、_______________。
是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为_____________、_______________。(4)工业上由
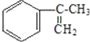 经过四步不同类型的反应制得阿托酸。
经过四步不同类型的反应制得阿托酸。①请按实际进行的反应顺序写出指定反应步骤中所需要的试剂和反应条件:
第一步_________________;第二步________________。
②写出第四步反应的化学方程式:________________。
高二化学填空题中等难度题查看答案及解析
-
3-对甲苯丙烯酸甲酯(E) 是一种用于合成抗血栓药的中间体,其合成部分路线如下:
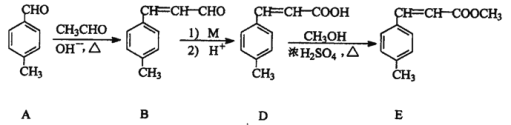
(1)B中含有的官能团名称为_______、__________。
(2)由A转化为B,反应分两步完成,请判断反应类型依次为___________,_________。
(3)D 的分子式为_________________。
(4)1mol E最多能与___________mol 的氢气发生加成反应。
(5)1molB与5mol H2在适当条件下完全加成后,产物分子中含手性碳原子的数目为_____;
(6)D转化为E 的化学反应方程式为________________,
(7)试剂M 可以选用下列中的_________。
A.NaOH 溶液 B.银氨溶液
C.酸性高锰酸钾溶液 D.新制Cu(OH)2 悬浊液
高二化学填空题中等难度题查看答案及解析
-
(1)
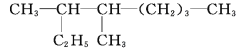 的名称是_______。
的名称是_______。(2)分子式符合C7H16且含有四个甲基的结构有__________种。
(3)核磁共振仪处理
,氢谱图中有___种氢,峰面积之比为____。
(4)水的熔沸点比同主族其它氢化物的都高,原因是______。
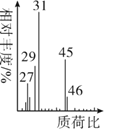
(5)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),则A的实验式是___,用质谱仪测定A的相对分子质量,得到如图所示质谱图,则其相对分子质量为____,A的分子式是____。
高二化学填空题中等难度题查看答案及解析