-
按要求填空:
(1)用系统命名法命名下列物质或者根据名称写出对应的结构简式
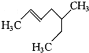 _________________________
_________________________CH3CH(CH3)CH2CH(CH3)CH(CH3)CH3 ___________________________
3,4,4-三甲基-1-戊炔_____________
(2)指出下列物质中的官能团
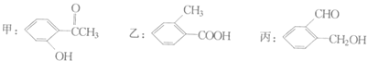
甲_______________ 乙____________ 丙_______________
(3)① C5H10Cl2的同分异构体有__________种
② 苯环上含 -C3H6Cl -CH3 -C4H9三个取代基的同分异构体有_____种
(4)某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究.

步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收.2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水.
步骤二:通过仪器分析得知X的相对分子质量为106.
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2:3 (如图Ⅰ)

步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ. 试填空:
①X的分子式为___________;X的习惯命名为___________;
②步骤二中的仪器分析方法称为___________
高二化学填空题困难题查看答案及解析
-
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为___________________________________________________________________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________mol;用平衡移动原理解释阴极区pH增大的原因:___________________________________________________________
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-。电池工作时正极反应式为___________________
高二化学填空题困难题查看答案及解析
-
(1)已知:Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)ΔH=+19 kJ·mol-1 ③
请写出CO还原FeO的热化学方程式:_______________________。
(2)某研究小组向某2 L密闭容器中加入一定量的固体A和气体B,发生反应A(s)+2B(g)
 D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:时间(min)
物质的量(mol)
0
10
20
30
40
50
B
2.00
1.36
1.00
1.00
1.20
1.20
D
0
0.32
0.50
0.50
0.60
0.60
E
0
0.32
0.50
0.50
0.60
0.60
①T ℃时,该反应的平衡常数K=________。
②30 min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的B b.加入一定量的固体A
c.适当缩小容器的体积 d.升高反应体系温度
③若该密闭容器绝热,实验测得B的转化率随温度变化的示意图如图所示。由图可知,Q________0(填“大于”或“小于”),c点v正________v逆(填“大于”、“小于”或“等于”)。

高二化学填空题困难题查看答案及解析
-
(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量是___mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___,又变为棕黄色的原因是(用离子方程式解释)____。
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有
 的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为_____mol/L。
的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为_____mol/L。(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。
①写出该反应的化学方程式____。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是___。
高二化学填空题困难题查看答案及解析
-
一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。
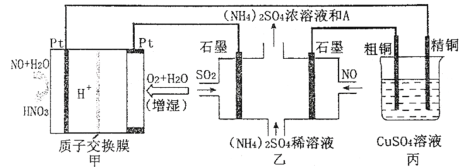
(1)燃料电池放电过程中负极的电极反应式____。
(2)乙装置中物质A是____(填化学式),理由是___;电解过程中阳极附近pH___(填“增大”“减小”或“不变”),阴极的电极反应式是____。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将__(填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有____mol;丙装置中阴极析出铜的质量为___g。
高二化学填空题困难题查看答案及解析
-
已知25℃时,几种常见弱酸的Ka如下表所示:
电解质
H2C2O4
CH3COOH
HCN
H2CO3
电离常数(mol•L-1)
K1=5.6×10-2
K2=5.4×10-3
K=1.7×10-5
K=6.2×10-10
K1=4.2×10-7
K2=5.6×10-11
(1)草酸(H2C2O4)是一种___(填“一元”、“二元”、“多元”)弱酸。25℃时,0.1mol•L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3溶液的pH由大到小的顺序是__。
(2)KHC2O4溶液呈酸性,向10mL0.01mol•L-1的H2C2O4溶液滴加0.01mol•L-1KOH溶液V(mL)。回答下列问题:
①当V<10mL时,反应的离子方程式为___。
②当V=10mL时,溶液中
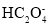 、
、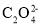 、H2C2O4、H+的浓度由大到小的顺序为__。
、H2C2O4、H+的浓度由大到小的顺序为__。③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(
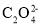 )+c(
)+c(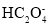 );当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(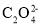 )+c(
)+c(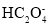 )+c(H2C2O4);则a__b(填“<”“=”或“>”).
)+c(H2C2O4);则a__b(填“<”“=”或“>”).高二化学填空题困难题查看答案及解析
-
铜制印刷电路板蚀刻液的选择及再生回收是研究热点。
(1)用HCl-FeCl3溶液作蚀刻液
①该溶液蚀刻铜板时发生主要反应的离子方程式为__________.
②从废液中可回收铜井使蚀刻液再生。再生所用的试剂有Fe和______(填化学式)。
(2)用HCl-CuCl2溶液作蚀刻液蚀刻铜后的废液中含Cu+ 用下图所示方法可使蚀刻液再生并回收金属铜。
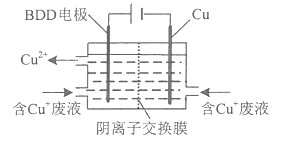
第一步BDD电极上生成强氧化性的氢氧自由基(HO·):H2O-e-==HO·+H+: .
第二步HO·氧化Cu+实现CuCl蚀刻液再生:________(填离子方程式) .
(3)用碱性CuCl2溶液(用NH3·H2O-NH4Cl调节pH)作蚀刻液
原理为:CuCl2+ 4NH3·H2O==Cu(NH3)4Cl2+ 4H2O;Cu(NH3)4Cl2+Cu== 2Cu(NH3)2Cl
①过程中只须及时补充NH3·H2O和NH4Cl就可以使蚀刻液再生,保持蚀刻能力。蚀刻液再生过程中作氧化剂的是_________(填化学式) 。
②50℃,c(CuCl2)=2.5mol·L-1, pH对蚀刻速串的影响如图所示。适宜pH约为8.3~9.0,pH过小或过大,蚀刻速率均会减小的原因是______________.
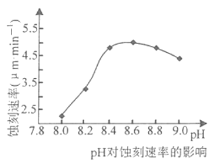
高二化学填空题困难题查看答案及解析
-
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
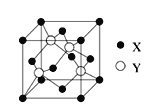
①在1个晶胞中,X离子的数目为_____。
②该化合物的化学式为_________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_______。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是______________。
(4)Y 与Z 可形成

①
 的空间构型为__________(用文字描述)。
的空间构型为__________(用文字描述)。②写出一种与
 互为等电子体的分子的化学式:_________。
互为等电子体的分子的化学式:_________。(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___。
高二化学填空题困难题查看答案及解析
-
香豆素类化合物具有抗病毒、抗癌等多种生物活性。香豆素3羧酸可由水杨醛
制备。
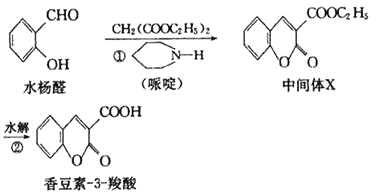
(1)中间体X的化学式为____。
(2)水杨醛发生银镜反应的化学方程式为_____________________________。
(3)香豆素3羧酸在NaOH溶液中彻底水解生成的有机物的结构简式为___________。
(4)下列说法中错误的是_______。
A.中间体X不易溶于水
B.水杨醛分子中所有原子一定处于同一平面
C.水杨醛除本身外,含有苯环且无其他环的同分异构体还有4种
D.水杨醛和香豆素3羧酸都能使酸性高锰酸钾溶液褪色
(5)反应①中的催化剂“哌啶”可以由“吡啶”合成,其反应为:
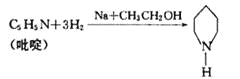
已知吡啶为环状,性质与苯类似。则吡啶的结构简式为____;吡啶与混酸(浓硝酸与浓硫酸混合物)在加热条件下,发生硝化反应生成氮原子间位的一取代物的化学方程式为_______________________。
高二化学填空题困难题查看答案及解析
-
锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:
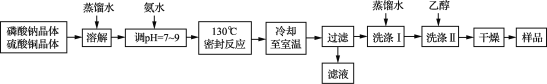
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1) 实验室进行“过滤”操作使用的玻璃仪器主要有____________________。
(2) 流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是__________________。
(3) 准确称取上述流程所得的样品38.56 g [假定样品中只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量的硝酸中,再加入氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为27.20 g。计算所得样品中磷酸氧铜的质量分数_______。(写出计算过程)
高二化学填空题困难题查看答案及解析