-
甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
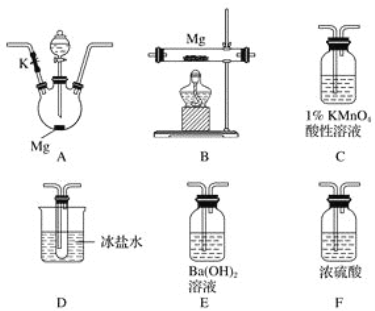
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________→E,确定还原产物中有二氧化氮的现象是______________________________________,实验中要多次使用装置F,第二次使用F的目的是______________________________________________。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________。
高二化学实验题困难题查看答案及解析
-
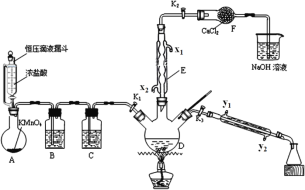
如图是某小组设计的用干燥氯气和甲苯合成一氯化苄(C6H5CH2Cl,其中C6H5-表示苯基)并分离产物的实验装置。甲苯及各种氯化苄的物理性质如表所示。
物理性质
熔点℃
沸点℃
密度g∙cm-3
甲苯
-95
110
0.86
一氯化苄(C6H5CH2Cl)
-45
179
1.10
二氯化苄(C6H5CHCl2)
-17
205
1.26
三氯化苄(C6H5CCl3)
-4.4
221
1.37
回答下列问题:
(1)仪器F的名称是__________;
(2)瓶B和C中盛放的试剂应分别为__________(填序号);
a.蒸馏水;浓硫酸 b.饱和食盐水;浓硫酸
c.浓硫酸;酸性KMnO4溶液 d.饱和NaHCO3溶液;浓硫酸
(3)两处冷凝水的进水口应分别为__________(填序号);
A . x1、y1 B. x1、y2 C. x2、y1 D.x2、y2
(4)在回流反应的过程中,由于温度控制不当,部分产物从K2处被蒸出。取烧杯中的少量吸收液于试管中,滴入新制氢氧化铜悬浊液并加热,观察到有砖红色沉淀生成。则在吸收液中发生反应的化学方程式为______________________;
(5)反应结束后,撤去E、F及尾气吸收装置,插上玻璃塞。保持K1关闭,打开K3,加热三颈烧瓶,分馏出一氯化苄,应选择的温度范围是__________;
(6)由于某同学操作时不慎将含铁的沸石加入三颈烧瓶,在分馏时得到了异常馏分X。用质谱法测得X的相对分子质量与二氯化苄相同,核磁共振氢谱显示X中有3种不同化学环境的氢。已知苯环上存在甲基或氯甲基是,后续取代苯环的基团主要引入其邻位或对位,X的结构简式可能为__________。
高二化学实验题困难题查看答案及解析
-
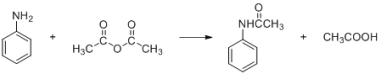
酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐加热来制取,该反应放热:
密度(g/mL)
相对分子质量
颜色、状态
溶解性
苯胺
1.04
93
无色油状液体
微溶于水,
易溶于乙醇、乙醚
乙酸酐
1.08
102
无色透明液体
遇水缓慢反应生成乙酸
乙酰苯胺
135
无色片状晶体,
熔点 114℃
不溶于冷水,可溶于热
水、乙醇、乙醚
实验步骤
①取5.00 mL苯胺,倒入100 mL锥形瓶中,加入20 mL水,在旋摇下分批加入6.00 mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至150 mL烧杯中,加入适量水配制成 80 ℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5 min,_______,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品6.2 g。
请回答:
(1)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是______。
A 加20 mL水 B 旋摇下分批加入6.0 mL乙酸酐
C 玻璃棒将块状物研碎 D 充分搅拌
(2)在步骤②中对粗产品进行洗涤需要用到以下操作:
a 加入洗涤剂至浸没固体;b 洗涤剂缓慢通过;c 关小水龙头;d 开大水龙头; e 重复 2~3 次。
请对以上操作做出正确的排序__________。
(3)步骤③加入过量 20%的水的目的是________,横线处的操作步骤是_________。
(4)下列说法不正确的是______。
A 活性炭吸附有色物质,可以提高产率
B 冷却时,室温冷却比冰水浴冷却更易得到大颗粒晶体便于抽滤
C 抽滤用如图装置,为防止倒吸,结束时可先关闭水龙头,后打开活塞a
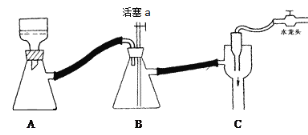
D 产品可放在表面皿上用热水浴烘干,烘干后可通过测量产品熔点判断产品纯度
(5)该实验的产率是___________。
高二化学实验题困难题查看答案及解析
-
实验室用少量的溴和足量的乙醇制备1,2一二溴乙烷的装置如图所示:

有关数据列表如下:
乙醇
1,2—二溴乙烷
乙醚
状态
无色液体
无色液体
无色液体
密度/g/cm−3
0.79
2.2
0.71
沸点/℃
78.5
132
34.6
熔点/℃
-130
9
-116
请按要求回答下列问题:
(1)写出A装置中的化学反应方程式___。
(2)装置C中盛有氢氧化钠溶液,其作用是___。
(3)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___。
(4)判断该制备反应已经结束的最简单方法是___。
(5)若产物中有少量未反应的Br2,最好用___洗涤除去。(填正确选项前的字母)
a.水 b.亚硫酸氢钠 c.碘化钠溶液 d.乙醇
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是___。
高二化学实验题困难题查看答案及解析
-
某同学进行影响草酸溶液与高锰酸钾酸性溶液反应速率因素的研究。室温下,实验数据如下:
实验序号
①
②
③
加入试剂
4mL 0.01mol/L KMnO4
2mL 0.1mol/L H2C2O4
4mL 0.01mol/L KMnO4
2mL 0.1mol/L H2C2O4
少量MnSO4固体
4mL 0.01mol/L KMnO4
2mL 0.1mol/L H2C2O4
少量Na2SO4固体
褪色时间/s
116
6
117
(1)草酸溶液与高锰酸钾酸性溶液反应的离子方程式为___________________。
(2)该实验结论是_______________________。
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论。请写出实验①的现象为____________________。
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是_________________。
(5)该同学拟采用如下图所示的实验方案继续探究外界条件对反应速率的影响。
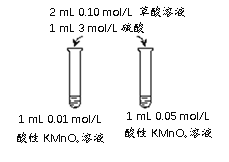
a.该同学拟研究的影响因素是___________________。
b.你认为该同学的实验方案_______________(填“合理”或“不合理”),理由是____________________________。
高二化学实验题困难题查看答案及解析
-
实验室制备无水二氯化锡的主要步骤如下:
步骤1:在圆底烧瓶中加入1.20 g碎锡箔和5 mL浓盐酸、1滴硝酸,实验装置如图所示。组装好后在95 ℃ 时回流0.5 h,待圆底烧瓶中只剩余少量锡箔为止;
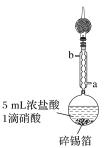
步骤2:将上述反应的上清液迅速转移到仪器X中,在二氧化碳气氛保护下,蒸发浓缩,冷却结晶,过滤得到二氯化锡晶体;
步骤3:在二氯化锡晶体中加入10 mL醋酸酐,即可得无水二氯化锡,过滤;
步骤4:用少量乙醚冲洗三次,置于通风橱内,待乙醚全部挥发后得到无水二氯化锡。
回答下列问题:
(1)步骤1中,圆底烧瓶中发生反应的化学方程式为___________________________________;
冷却水从接口________(填“a”或“b”)进入。实验采取的加热方式是______________;球形冷凝管上连接装有碱石灰的干燥管的目的是____________________________________。
(2)步骤2中,仪器X的名称为__________;二氧化碳气氛的作用是__________________。
(3)步骤3中,醋酸酐的作用是____________________;二氯化锡晶体在进行步骤3操作前应采取的加工措施是________,该加工措施需要仪器的名称是________。
高二化学实验题困难题查看答案及解析
-
FeCl3是中学实验室常用的试剂。
(1)写出氯化铁在水中的电离方程式:_________。
(2)利用氯化铁溶液制备氢氧化铁胶体。
①下列制备氢氧化铁胶体的操作方法正确的是_______(填字母)。
A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体
②区别氯化铁溶液和氢氧化铁胶体的方法是___________。
(3)为了探究离子反应的本质,设计如下实验:

①写出生成A的离子方程式:_________。
②上述流程中,加入足量稀硝酸的目的是________。如何判定无色溶液B与稀硝酸发生了离子反应?________。
高二化学实验题困难题查看答案及解析
-
实验室制备 1,2-二溴乙烷的反应原理如下:
CH3CH2OH
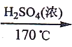 CH2=CH2+H2O
CH2=CH2+H2OCH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备 1,2-二溴乙烷的装置如下图所示:
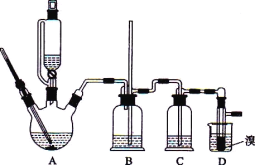
有关数据列表如下:
乙醇
1,2-二溴乙烷
乙醚
状态
无色液体
无色液体
无色液体
密度/g∙cm-3
0.79
2.2
0.71
沸点/℃
78.5
132
34.6
熔点/℃
一l30
9
-1l6
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃ 左右,其最主要目的是_____;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入_____,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量未反应的 Br2,最好用_____洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(4)判断该制各反应已经结束的最简单方法是_____;
(5)若产物中有少量副产物乙醚,可用_____的方法除去;
(6)反应过程中应用冷水冷却装置D,其主要目的是____;但又不能过度冷却(如用冰水),其原因是_____
高二化学实验题困难题查看答案及解析
-
某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Fe2+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
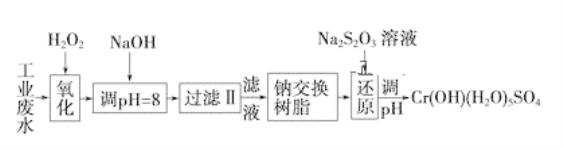
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物
Fe(OH)3
Fe(OH)2
Mg(OH)2
Al(OH)3
Cr(OH)3
pH
3.7
9.6
11.1
8
9(>9溶解)
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR→MRn+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+B.Al3+C.Ca2+D.Mg2+
(3)还原过程中,每消耗0.8 mol Cr2O72-转移4.8 mol e-,该反应离子方程式为____________。
高二化学实验题困难题查看答案及解析
-
实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
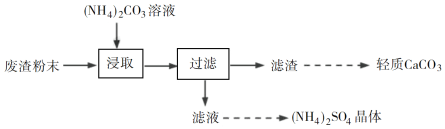
(1)室温下,反应CaSO4(s)+
(aq)
CaCO3(s)+
(aq)达到平衡,则溶液中
=________[Ksp(CaSO4)=4.8×10−5,Ksp(CaCO3)=3×10−9]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为________;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是________。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________。
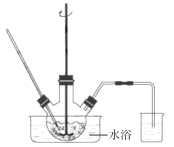
(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:______[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。
高二化学实验题困难题查看答案及解析