-
若在铜片上镀银时,下列叙述正确的是( )
①将铜片接在电源的正极上
②将银片接在电源的正极上
③在铜上发生的反应是:Ag++e-= Ag
④在银片上发生的反应是:4OH—-4e—= O2↑+2H2O
⑤需用硫酸铜溶液为电镀液
⑥需用硝酸银溶液为电镀液
A. ①③⑥ B. ②③⑥ C. ①④⑤ D. ②③④⑥
高三化学单选题中等难度题查看答案及解析
-
微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为: Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH- 根据上述反应式,判断下列叙述中正确的是:( )
A. 在使用过程中,电池负极区溶液的PH不断增大
B. 使用过程中,电子由Ag20极经外电路流向Zn极
C. Zn是负极,Ag2O是正极
D. Zn电极发生还原反应,Ag2O电极发生氧化反应
高三化学单选题中等难度题查看答案及解析
-
1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为( )
A. C + H2O ==CO + H2ΔH ==+131.3KJ·mol—1
B. C(s)+ H2O(g) ==CO(g) + H2(g) ΔH ==+10.94KJ·mol—1
C. C(s)+ H2O(l) ==CO(g) + H2(g) ΔH ==+131.3KJ·mol—1
D. C(s)+ H2O(g) ==CO(g) + H2(g) ΔH ==+131.3KJ·mol—1
高三化学单选题中等难度题查看答案及解析
-
在下列各溶液中,离子一定能大量共存的是( )
A. 强碱性溶液中:NO3-、 HCO3- 、Cl- 、SO42-
B. 含有Fe3+的溶液中:K+、Mg2+、H+、AlO2-
C. 某无色溶液中:Na+、Cu2+、SO42-、Cl-
D. 室温下,pH=1的溶液中:K+、Al3+、NO3-、SO42-
高三化学单选题中等难度题查看答案及解析
-
下列说法中正确的是( )
A. 非金属氧化物一定能与碱发生反应 B. 金属氧化物一定不能与碱发生反应
C. 酸性氧化物一定能与水反应生成酸 D. 酸性氧化物可能与酸发生反应
高三化学单选题中等难度题查看答案及解析
-
质量分数为n的NaOH溶液,其物质的量浓度为amol/L,加热蒸发水分使其质量分数变为2n,此时,该溶液中NaOH的物质的量浓度为b mol/L,则a与b的关系正确的是( )
A. b=2a B.a=2b
C. b>2a D.b<2a
高三化学单选题中等难度题查看答案及解析
-
东晋《华阳国志·南中志》已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子价层电子排布式为_____,
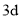 能级上未成对电子数为_____。
能级上未成对电子数为_____。(2)硫酸镍溶于氨水形成
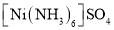 蓝色溶液。
蓝色溶液。①
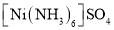 中阴离子的立体构型是______。
中阴离子的立体构型是______。②在
 中
中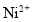 与
与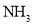 之间形成的化学键称为___,提供孤电子对的成健原子是___。
之间形成的化学键称为___,提供孤电子对的成健原子是___。③氨是___分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___。
④向硫酸铜溶液逐滴加入氨水,会先生成难溶物而后溶解也能形成深蓝色溶液,写出难溶物溶于氨水的离子方程式:__。
(3)单质铜及镍都是由_____键形成的晶体;元素铜与镍的第二电离能分别为:
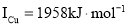 ,
,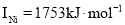 ,
,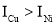 的原因是______。
的原因是______。(4)某镍白铜合金的立方晶胞结构如图所示。
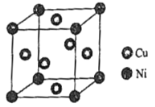
①晶胞中铜原子与镍原子的数量比为__。
②若合金的密度为
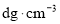 ,该立方晶胞的边长约为___
,该立方晶胞的边长约为___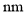 。
。高三化学结构与性质中等难度题查看答案及解析
-
如图甲是利用一种微生物将废水中的尿素(
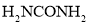 )的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是
)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是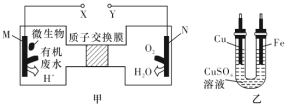
A.铜电极应与Y相连接
B.乙装置中溶液的颜色不会变浅
C.标准状况下,当N电极消耗
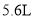 气体时,则铁电极质量增加
气体时,则铁电极质量增加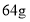
D.M电极反应式:
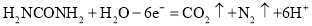
高三化学单选题中等难度题查看答案及解析
-
为减少温室气体的排放,科学家研究出以
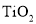 为催化剂,光热化学循环分解
为催化剂,光热化学循环分解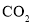 的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。
的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。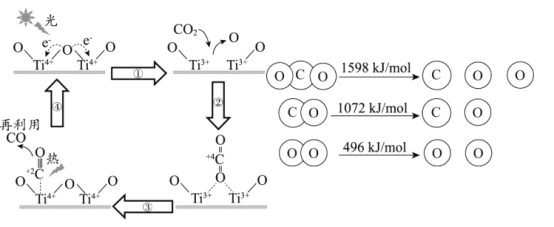
下列说法正确的是
A.该反应中,光能和热能转化为化学能
B.该过程中没有电子的转移
C.使用
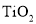 作催化剂可以降低反应的焓变,从而提高化学反应速率
作催化剂可以降低反应的焓变,从而提高化学反应速率D.分解
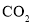 反应的热化学方程式:
反应的热化学方程式: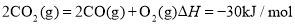
高三化学单选题中等难度题查看答案及解析
-
下列实验的反应原理用离子方程式表示正确的是
A.室温下,测的氯化铵溶液
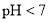 ,证明一水合氨是弱碱:
,证明一水合氨是弱碱: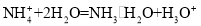
B.将过量二氧化硫气体通入冷氨水中:
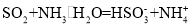
C.硫代硫酸根与稀硫酸反应:

D.用高锰酸钾标准溶液滴定草酸:
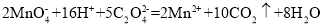
高三化学单选题中等难度题查看答案及解析