-
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,5.6 L CCl4中含有的Cl原子数为NA
B.密闭容器中,1mol NO与足量O2反应,混合气体中NO2的分子数为NA
C.3.0g乙烷中含有的共价键数为0.7NA
D.常温下,1mol Cl2溶于足量Ca(OH)2溶液中,转移的电子数为NA
高三化学多选题中等难度题查看答案及解析
-
氧化铅-铜电池是一种电解质可循环流动的新型电池(如图所示),电池总反应为
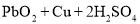
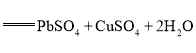 。下列有关该电池的说法正确的是( )
。下列有关该电池的说法正确的是( )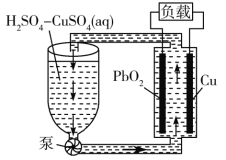
A.电池工作时,电子由Cu电极经电解质溶液流向PbO2电极
B.电池工作过程中,电解质溶液的质量逐渐减小
C.正极反应式:
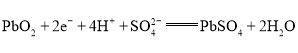
D.电池工作过程中,两个电极的质量均减小
高三化学单选题中等难度题查看答案及解析
-
一定条件下,发生反应
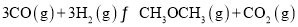
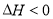 ,下列判断正确的是( )
,下列判断正确的是( )A.恒容时,升高温度,CO的平衡转化率增大
B.恒温恒容时,充入CO,v(正)增大,平衡右移
C.恒温时,缩小容器容积,平衡右移,平衡常数K不变
D.分离出CH3OCH3时,v(正)增大,平衡右移
高三化学多选题中等难度题查看答案及解析
-
目前新冠肺炎的药物研发和疫苗研制取得了很大进展,其中法匹拉韦药物(结构如图)显示有一定的临床疗效。下列关于此物质的说法正确的是( )
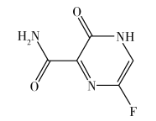
A.由5种元素组成 B.结构中存在手性碳原子
C.能使酸性KMnO4溶液褪色 D.3个N原子的杂化方式相同
高三化学多选题中等难度题查看答案及解析
-
下列有关物质性质的比较错误的是( )
A.熔点:MgO>CaO>KCl B.沸点:AsH3>PH3>NH3
C.离子半径:S2->Cl->Ca2+ D.稳定性:H2O>H2S>H2Se
高三化学单选题中等难度题查看答案及解析
-
氮化硅(Si3N4)可用作高级耐火材料、新型陶瓷材料、LED基质材料等。已知:Si的电负性比H的小,利用硅烷(SiH4)制备氮化硅的反应为
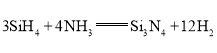 。下列有关说法正确的是( )
。下列有关说法正确的是( )A.硅烷中Si的化合价为-4价 B.NH3在该反应中作还原剂
C.H2既是氧化产物,也是还原产物 D.转移1.2mol电子时,生成26.88 L H2
高三化学单选题中等难度题查看答案及解析
-
2020年初,一场疫情席卷中国。防疫抗疫的措施有勤洗手,对环境进行消毒等。下列说法错误的是( )
A.用肥皂洗手可以去油污,冲走携带的细菌
B.84消毒液能对环境消毒是因为该消毒液中含有强氧化性的次氯酸盐
C.用酒精对环境杀菌消毒时,酒精的浓度越高越好
D.含盐酸的清洁剂不能与84消毒液混合使用,否则易使人中毒
高三化学单选题中等难度题查看答案及解析
-
(1)基态溴原子的价层电子轨道表达式为________。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________(填标号)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________;
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构, 如图所示。下列有关黑磷晶体的说法正确的是_________。
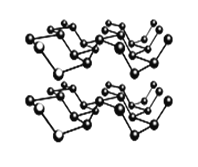
A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
高三化学解答题中等难度题查看答案及解析
-
化石燃料燃烧时会产生 SO2进入大气,有多种方法可用于 SO2的脱除。
(1)NaClO 碱性溶液吸收法。工业上可用 NaClO 碱性溶液吸收SO2。
①反应离子方程式是__________________________________________。
②为了提高吸收效率,常用 Ni2O3作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示:

a.过程1的离子方程式是Ni2O3+ClO- =2NiO2 +Cl-,则过程2的离子方程式____________。
b.Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是________________。
(2)碘循环工艺也能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:
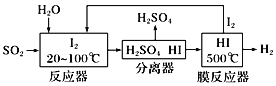
则碘循环工艺的总反应为:___________________________________________。
高三化学综合题中等难度题查看答案及解析
-
硫酸锌被广泛应用于医药领域和工农业生产。工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图:
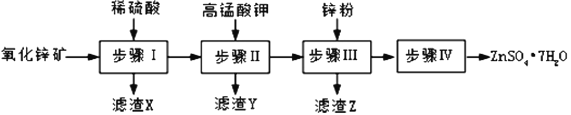
(1)步骤Ⅰ的操作是____________。
(2)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为____________________________________。
(3)步骤Ⅲ中,加入锌粉的作用是______________。
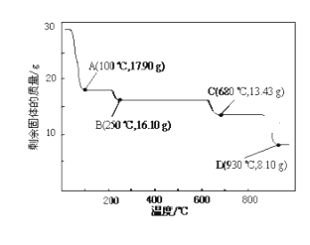
(4)取28.70 g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如下图所示。实验室中应置于____________(填仪器名称)焙烧样品。分析数据,100℃时发生反应的化学方程式为 ______________________________;680℃时所得固体的化学式为__________(填字母符号)。
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O
高三化学综合题中等难度题查看答案及解析