-
电解1mol/L CuSO4和0.1mol/L Cu(NO3)2的混合液100mL,当阳极析出896mL(标准状况)气体时,切断电源,使电极仍浸在溶液中,经充分反应后,阴极比原来增重多少克?溶液的pH是多少?(lg2=0.3)
高三化学计算题中等难度题查看答案及解析
-
如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL。
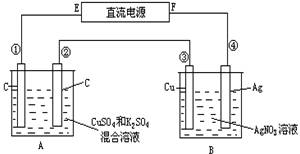
试求:
(1)请写出①、②的电极反应式;
(2)通电前A池中原混合溶液Cu2+的浓度。
高三化学计算题中等难度题查看答案及解析
-
一定条件下1molN2和4mol H2通入到V升的容器中发生反应,反应前容器中的压强为P,保持温度和体积不变,10min后反应达到平衡,此时容器内混合气体平均相对分子质量为9,试求
(1)平衡时,体系内压强为多少?
(2)平衡时,氨气的体积分数为多少?
高三化学计算题中等难度题查看答案及解析
-
铁铝合金是一种新型高温结构材料。
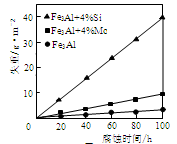
(1)图9表示室温时不同组份的Fe3Al在65%浓HNO3 中的腐蚀情况。由图9可看出添加了(填符号)元素的合金耐蚀性最差。
(2)高温条件下,Al和Fe2O3按一定比例混合反应可制
得Fe3Al,写出该反应的化学方程式________。(3)某校兴趣小组欲测定另一种铁铝硅合金(FexAlySiz)粉末的组成。
①小明同学提出如下方案:准确称取1.46g该合金粉末,再加入足量NaOH溶液(Si+2NaOH+H2O=Na2SiO3+2H2↑),充分反应后过滤,通过测定剩余固体质量及收集到气体的体积,可计算出此合金的组成。写出Al与NaOH溶液反应的离子方程式________。
②小军同学认为该方案难以测定标准状况下气体的体积,操作不简便。于是他设计了第二种方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g。试通过计算确定此合金的组成。
高三化学计算题中等难度题查看答案及解析
-
工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
O2
(1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(2)硝酸厂尾气常用的处理方法是催化还原法:催化剂存在时用H2将NO2还原为N2 。已知:
2H2(g)+O2(g)=2H2O(g) △H= a kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H= b kJ·mol-1
H2O(1)=H2O(g) △H= c kJ·mol-1
则反应2NO2(g)+4H2(g)=N2(g)+4H2O(1)的△H=_________。(用a、b、c表示)
(3)①合成氨反应的化学方程式为N2+3H2
2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的相对分子质量保持不变
E.1mol N≡N键断裂,同时1mol H—H键断裂
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L的密闭容器中,5min反应达平衡,n(N2)=1mol,n(H2)=1mol,n(NH3)=2mol,则反应速率v(N2)=________________,H2的平衡转化率=_________________;若保持容器的温度不变,在10min时将容器的容积压缩为lL,请在答题卡坐标图中,画出从反应开始至15min时c(NH3)随时间变化曲线示意图。
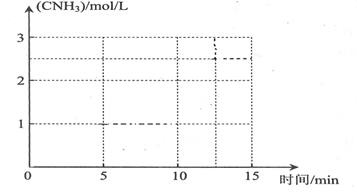
高三化学计算题中等难度题查看答案及解析
-
(5分)某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放人烧杯中,将烧杯放在电子称上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
时间/s
0
5
10
15
读数/g
215.2
211.4
208.6
208.6
请你据此分析计算:
(1)该产品中碳酸钠的质量分数?(结果精确到0。l%)
 (2)若反应后溶液为150.0 mL,计算溶液中NaCI物质的量浓度。
(2)若反应后溶液为150.0 mL,计算溶液中NaCI物质的量浓度。高三化学计算题中等难度题查看答案及解析
-
硫有多种含氧酸,如亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3)等,其中硫酸最为重要,在工业上有广泛的应用。完成下列计算:
(1)浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48 L(标准状况),若将反应后的溶液稀释至500 mL,该溶液中硫酸铜的物质的量浓度为__________ mol·L-1。
(2)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445 g焦硫酸溶于水配成4.00 L硫酸,该硫酸的物质的量浓度为____________ mol·L-1。
高三化学计算题中等难度题查看答案及解析
-
(4分 )(1)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101.3 kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH= 436 kJ·mol-1],形成化学键时ΔH<0[如2H(g)=H2(g) ΔH = - 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH = -185 kJ·mol-1
ΔH298(H2)= 436 kJ·mol-1 ,ΔH298(Cl2)= 247 kJ·mol-1
则ΔH298(HCl)= ________________________ 。
(2)已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH = -25 kJ·mol-1
3 Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH = - 47 kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH = 19 kJ·mol-1
请写出CO还原FeO的热化学方程式:________________________________________
高三化学计算题中等难度题查看答案及解析
-
在A容器中盛有80%的H2和20%的O2(体积分数)的混合气体,试求:
(1)其中H2与O2的分子数之比是__________?质量比是_____________?
(2)混合气体的平均式量_____________?混合气体在标准状况下的密度是__________?
(3)在某温度(高于100℃)时,引燃A容器中的气体,回复到原来温度,则A容器内混合气体的平均摩尔质量是____________?引燃前后,A容器内压强如何变化__________?A容器内混合气体的密度是否变化________________?
高三化学计算题中等难度题查看答案及解析
-
与c(H+)·c(OH-)=Kw类似,FeS饱和溶液中存在:FeS(s)
Fe2+(aq)+S2-(aq),
c(Fe2+)·c(S2-)=Ksp。常温下Ksp=8.1×10-17。
(1)理论上FeS的溶解度为____________________________________________。
(2)又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:[c(H+)]2·c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1 mol/L,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)为______。
高三化学计算题中等难度题查看答案及解析