-
长期缺碘和碘摄入过量都会对健康造成危害,目前加碘食盐中碘元素绝大部分以IO3-存在,少量以I-存在。现使用Na2S2O3对某碘盐样品中碘元素的含量进行测定。
I.I-的定性检测
(1)取少量碘盐样品于试管中,加水溶解。滴加硫酸酸化,再滴加数滴5%NaNO2和淀粉的混合溶液。若溶液变________色,则存在I-,同时有无色气体产生并遇空气变红棕色。试写出该反应的离子方程式为 ___________________________________。
Ⅱ.硫代硫酸钠的制备
工业制备硫代硫酸钠的反应原理为2Na2S + Na2CO3 +4SO2 =3Na2S2O3 +CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠如下图。
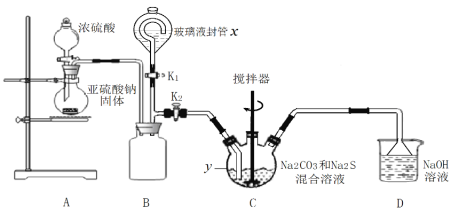
先关闭K1打开K2,打开分液漏斗,缓缓滴浓硫酸,控制好反应速率。
(2)y仪器名称___________ 。此时B装置的作用是___________________________。
(3)反应开始后,C中先有淡黄色浑浊,后又变为澄清,此浑浊物为____________。(填化学式)装置D的作用是____________________________________。
(4)实验结束后,关闭K2打开K1。玻璃液封管x中所盛液体最好为________(填序号)
A.NaOH溶液 B.浓硫酸 C.饱和NaHSO3溶液
Ⅲ.碘含量的测定
巳知:①称取10.00g样品,置于250mL锥形瓶中,加水100mL溶解,加2mL磷酸,摇匀。
②滴加饱和溴水至溶液呈现浅黄色,边滴加边摇,至黄色不褪去为止(约1mL)。
③加热煮沸,除去过量的溴,再继续煮沸5min,立即冷却,加入足量15%碘化钾溶液,摇匀。
④加入少量淀粉溶液作指示剂,再用0.002mol/L的Na2S2O3标准溶液滴定至终点。
⑤重复两次,平均消耗Na2S2O3溶液9.00mL
相关反应为:I-+3Br2+3H2O = IO3-+6H++6Br-
IO3-+5I-+6H+ = 3I2+3H2O
I2+2S2O32-= 2I-+S4O62-
(5)请根据上述数据计算该碘盐含碘量为_______ mg·kg—1。
-
长期缺碘和碘摄入过量都会对健康造成危害,目前加碘食盐中碘元素绝大部分以IO3-存在,少量以I-存在。现使用Na2S2O3对某碘盐样品中碘元素的含量进行测定。
I.I-的定性检测
(1)取少量碘盐样品于试管中,加水溶解。滴加硫酸酸化,再滴加数滴5%NaNO2和淀粉的混合溶液。若溶液变________色,则存在I-,同时有无色气体产生并遇空气变红棕色。试写出该反应的离子方程式为 ___________________________________。
Ⅱ.硫代硫酸钠的制备
工业制备硫代硫酸钠的反应原理为2Na2S + Na2CO3 +4SO2 =3Na2S2O3 +CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠如下图。
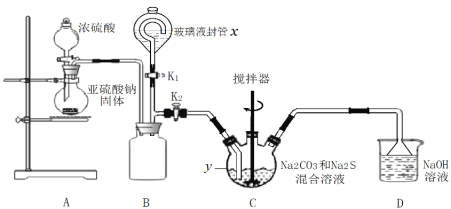
先关闭K1打开K2,打开分液漏斗,缓缓滴浓硫酸,控制好反应速率。
(2)y仪器名称___________ 。此时B装置的作用是___________________________。
(3)反应开始后,C中先有淡黄色浑浊,后又变为澄清,此浑浊物为____________。(填化学式)装置D的作用是____________________________________。
(4)实验结束后,关闭K2打开K1。玻璃液封管x中所盛液体最好为________(填序号)
A.NaOH溶液 B.浓硫酸 C.饱和NaHSO3溶液
Ⅲ.碘含量的测定
巳知:①称取10.00g样品,置于250mL锥形瓶中,加水100mL溶解,加2mL磷酸,摇匀。
②滴加饱和溴水至溶液呈现浅黄色,边滴加边摇,至黄色不褪去为止(约1mL)。
③加热煮沸,除去过量的溴,再继续煮沸5min,立即冷却,加入足量15%碘化钾溶液,摇匀。
④加入少量淀粉溶液作指示剂,再用0.002mol/L的Na2S2O3标准溶液滴定至终点。
⑤重复两次,平均消耗Na2S2O3溶液9.00mL
相关反应为:I-+3Br2+3H2O = IO3-+6H++6Br-
IO3-+5I-+6H+ = 3I2+3H2O
I2+2S2O32-= 2I-+S4O62-
(5)请根据上述数据计算该碘盐含碘量为_______ mg·kg—1。
-
下列有关叙述不正确的是
A.2011年9月29日卫生部出台《食用盐碘含量》国家标准,碘盐中碘含量的平均水平(以碘元素计)为20 mg/kg—30mg/kg,说明摄入过少和过量的碘都对人体健康不利
B.“地沟油”危害健康,不仅是因为人体所必需的维生素E、脂肪酸油脂已经被破坏,营养低,而且含有黄曲霉素、苯并芘,这两种毒素都是致癌物质
C.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
D.2012年3月2日修订的《环境空气质量标准》增设了PM2.5平均浓度限值, PM2.5受到普遍的关注,因为PM2.5在空气中能形成了气溶胶,富含大量的有毒、有害物质,对空气质量影响较大(PM2.5是指大气中直径接近于2.5×10-6m的颗粒物)
-
目前,人们的饮食追求是“吃得营养,吃出健康”,下列说法不正确的是( )
A.每天都应摄入一定量的蛋白质
B.油脂会使人发胖,故禁食油脂
C.过多摄入微量元素不利于健康
D.每天食用少量纤维素有利于健康
-
人的胃液是一种强酸性液体,pH在0.9~1.5之间,氢氧化铝是一种治疗胃酸过多的胃药的主要成分。目前这种胃药已不常用,原因主要是( )
A.长期摄入铝元素不利于人体健康
B.它不能中和胃液
C.它不易溶于胃液
D.它的疗效太差
-
人的胃液是一种强酸性液体,pH在0.9~1.5之间,氢氧化铝是一种治疗胃酸过多的胃药的主要成分。目前这种胃药已不常用,原因主要是( )
A.长期摄入铝元素不利于人体健康
B.它不能中和胃酸
C.它不易溶于胃酸
D.它的疗效太差
-
已知氧化性:Cl2>IO3->Fe3+>I2,则对实验结果分析或预测正确的是( )
A.加碘食盐溶液中滴入少量白醋和淀粉 KI 溶液,溶液变蓝色,说明可能是 IO
B.加碘食盐溶液中加入过量氯水后加淀粉,溶液不变蓝色,说明不可能是 I-
C.FeI2 溶液中滴加少量氯水,溶液中一定有 Fe3+生成
D.FeCl2 溶液中滴加足量碘水和 KSCN 溶液,溶液一定变红色
-
食品安全问题已引起人们广泛关注.下列行为不会对人体健康造成危害的是
A.利用地沟油制售食用油
B.在牛奶中添加三聚氰胺,提高牛奶含氨量
C.在食盐中添加适量碘酸钾,补充人体所需的碘元素
D.在生产豆芽过程中添加尿素、恩诺沙星、无根剂等非食品添加剂
-
羰基硫(COS)主要存在于煤、石油和天然气中,会造成设备腐蚀、环境污染,更危害人体健康。目前,我国已经实现了在催化剂(γ-Al2O3)、低温条件下的精度脱除COS,如图为天然气中脱除COS反应流化床示意图:
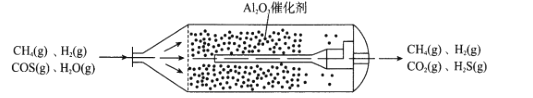
(1)①已知:H2(g)+COS(g) H2S(g)+CO(g) △H1=+6.2kJ•mol-1
H2S(g)+CO(g) △H1=+6.2kJ•mol-1
H2(g)+CO2(g) H2O(g)+CO(g) △H2=+41.2kJ•mol-1
H2O(g)+CO(g) △H2=+41.2kJ•mol-1
则COS精度脱除反应H2O(g)+COS(g) H2S(g)+CO2(g)的△H=__kJ•mol-1。
H2S(g)+CO2(g)的△H=__kJ•mol-1。
②将H2O与COS以体积比1:2置于恒温恒容密闭容器中反应,若测得该反应平衡时H2O与COS的体积比1:6,则该温度下,脱除反应的平衡常数K=__(保留两位小数)。
(2)T℃时,以一定流速、不同物质的量的H2O(g)和COS(g)通过流化床,测得COS(g)脱除速率变化关系如图。
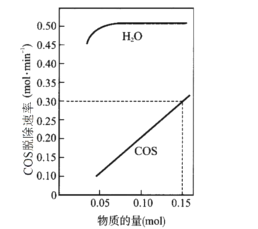
已知:COS脱除反应机理如下,其中吸附在催化剂表面的物种用*标注。
a.吸附:H2O→H2O*
b.反应:COS+H2O*→CO2+H2S*
c.脱附:H2S*→H2S
①若COS(g)脱除速率v=knx(COS)•ny(H2O)(mol•min-1),由图中的数据可算出x、k的值:x=__,k=__。
②“吸附”步骤为__(填“快反应”或“慢反应”),理由是__。
③脱除反应的决速步骤为__(填“a”、“b”或“c”)。
④少量氢气可以抑制催化剂积硫(S*)中毒,分析该流化床中可能存在的可逆反应是__。
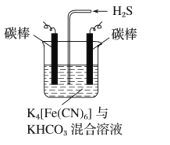
(3)工业上常采用下图所示电解装置,将气态废弃物中的硫化氢转化为可利用的硫。首先通电电解K4[Fe(CN)6]与KHCO3的混合溶液,通电一段时间后,再向所得溶液通入H2S时发生反应的离子方程式为2[Fe(CN)6]3-+2CO32-+H2S═2[Fe(CN)6]4-+2HCO3-+S↓.电解过程中阴极区电极反应式为_。
-
(12分)食盐是重要调味品,随着对饮食健康的重视,出现了各种类型的特种食盐。
(1)常说“饮食过咸会伤骨”,长期摄入食盐过多可能导致骨骼脱钙,下列物质中,可以作为补钙药品主要成分的是 (填标号)。
A.CaCO3 B.CaO C.Ca(OH)2 D.Ca
(2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的化学方程式是 。
(3)加硒盐中含有的硒元素是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实: 。
(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子 mol,该反应的离子方程式为 。




