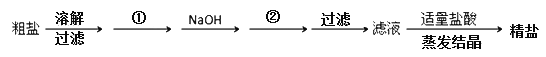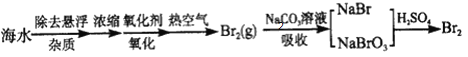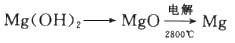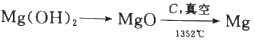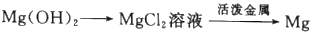-
海水是自然赐给人类的宝藏,海水的综合利用是全世界研究的重点。完成下列问题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO42-等杂质,粗盐获得精盐一般步骤如下:
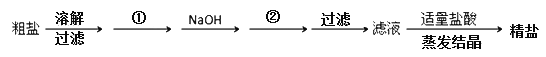
加入的试剂①、②分别是:_________、_________。
(2)某学生在实验室中模拟海水提取溴的步骤为: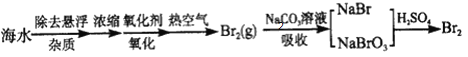
取25 L除去悬浮杂质后的海水,浓缩至2L,向其中通入足量氯气。
① 氧化步骤中生成Br2的离子方程式为_______________________________。
② 将吹出的Br2(g)用纯碱溶液全部吸收,发生反应:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ ,产生的CO2通入足量澄清石灰水中,得到1g白色沉淀。计算海水中溴的浓度为_______g/L。
③实验室中若用CCl4提取少量的溴:向溴水中加入CCl4振荡、静置……得溴的四氯化碳溶液,该分离提纯溴的方法叫________;用到的主要仪器为_____________。
(3)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: _____________。
-
海水是自然賜给人类的宝藏,海水的综合利用是全世界研究的重点。
完成下列问题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO42-等杂质,粗盐获得精盐一般步骤:

加入氯化钡、纯碱和烧碱的目的依次是:_________、_________、_________。
(2)海水提取金属镁流程如下:

流程中加入熟石灰目的__________;沉淀与盐酸反应的离子方程式_____________。
(3)某学生实验室模拟河水提取溴的步骤为:海水→浓缩→氧化→提取→溴
①氧化步骤: 适宣作氧化剂的是_______。
A Br2 B.Cl2 C.I2 D HCl
②提取步骤:……溴水中加入CCl4振荡、静置……得溴的四氯化碳溶液,该分离提纯溴的方法叫________;用到的主要仪器为________。
(4)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: ________;Cu与硫磺反应的化学方程式________;
-
海水中含有非常丰富的化学资源,从海水中可提取多种化工原料.下图是某化工厂对海水资源综合利用的示意图.(注:母液中含有Mg2+)
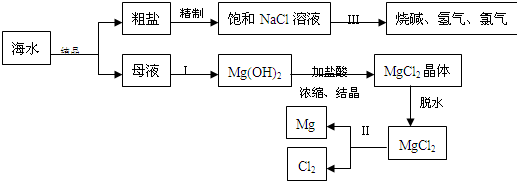
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得饱和NaCl溶液,精制时通常在溶液中加入以下物质,最后使溶液呈中性.
①过量的Na2CO3溶液、②盐酸、③过量的NaOH溶液、④过量的BaCl2溶液则,加入的顺序是______.
(2)写出加入最后一种试剂后可能发生的化学反应的离子方程式______、______.
(3)①写出反应Ⅱ的化学方程式______ Mg+Cl2↑
-
海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
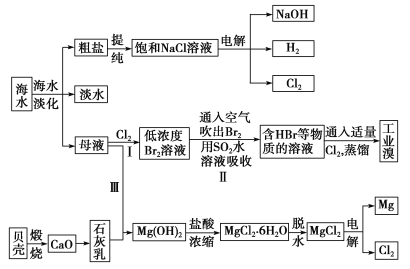
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是________(填编号)。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_____________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_______________________。
(3)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入MgCl2溶液,充分搅拌后经________(填操作方法)可得纯净的Mg(OH)2。
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________(填字母)。
A.H2 B.CO2 C.N2 D.O2 E.水蒸气
-
海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
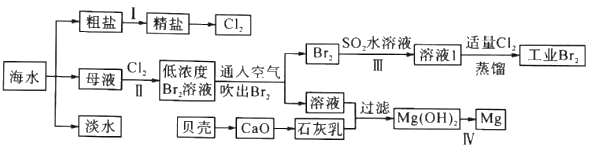
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________、_________。
(2)步骤Ⅱ中已获得Br2,步骤Ⅲ中又将Br2还原为Br-,其目的是_________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A. 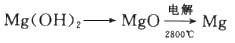
B.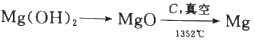
C.
D. 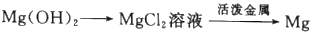
-
海水中有取之不尽的化学资源,从海水中可提取多种化工原料。如图是某工厂综合利用海水资源的示意图。
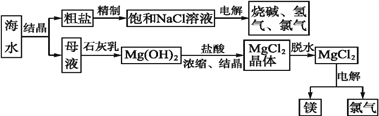
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得饱和NaCl溶液。精制过程中所用试剂有a、BaCl2溶液、b、Na2CO3溶液、c、 NaOH溶液、d、盐酸。加入试剂顺序正确的是____________;
A、a.b.c.d B、c.b.a.d C、b.a.d.c D、a.c.b.d
(2)写出电解饱和食盐水方程式________________________________________,产生的Cl2和烧碱反应能生成____________(填商品名称),反应方程式________。
(3)海水中提取食盐后的母液中含有K+、Na+、Mg2+等。从离子反应的角度考虑,向母液中加入石灰乳的作用是_________________________。
(4)电解熔融的氯化镁所得的镁蒸气冷却后即为固体镁,可以冷却镁蒸气的气体氛围为_____。
A.H2 B.CO2 C.空气 D.Ar
-
海水中有取之不尽的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源的综合利用的示意图。
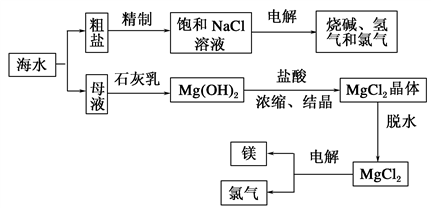
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
①粗盐溶液中加入过量的Na2CO3溶液:____________________;_____________________。
②滤液中加入盐酸至溶液呈中性:________________________;_______________________。
(2) 母液中含有K+、Na+、Mg2+等阳离子,从以上流程可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是_____________________;若加入石灰乳后所制取的产品中还混杂着熟石灰,那么将熟石灰从该产品中除去的方法是________________________。
②电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是________(填字母序号)。
A.H2 B.CO2 C.O2 D.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新的母液中加入一种常见的气态氧化剂,又抽取了重要的化工原料溴单质。
①生成溴单质的化学反应的离子方程式是___________________________________;生产中利用溴单质的挥发性将溴单质从化合物中分离出来的方法是________________________。
②以下是对生产溴单质所用的气态氧化剂寻找供货源的设想,其中合理的是_________(填字母序号)。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
③从多种经营、综合开发、打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是_________________________________。
-
海洋是资源宝库。下图是工业上对海水的一种综合利用的流程图:
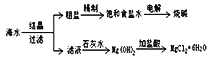
请回答下列问题:
(1) 在实验室对海水进行过滤,所需要玻璃仪器为烧杯、漏斗和_________。
(2) 若粗盐中含有Ca2+、Mg2+、SO42-三种杂质离子。精制提纯时,备用的除杂试剂有:A.盐酸,B.Na2CO3溶液,C.NaOH溶液,D.BaCl2溶液。请你正确排列加入试剂的顺序:NaOH溶液、_______、_______、_______(填编号)。
(3) 用如图电解食盐水,石墨电极上产生的气体为_______;在铁棒周围的溶液里滴加酚酞试剂,溶液变_______色;小烧杯中NaOH溶液的作用是(用化学方程式表示):______________。
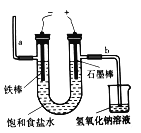
(4)在盛有Mg(OH)2固体的烧杯中,加入足量盐酸,待固体全部溶解后,要从溶液中获取MgCl2·6H2O晶体,需要进行的实验操作依次为_________________(填编号)。
A.蒸馏 B.蒸发 C.冷却结晶 D.过滤
-
海洋是一个巨大的宝藏,期待着人们的开发和利用,下列有关海水综合利用的说法正确的是
A.从海水中提取溴单质只有物理变化发生
B.从海水制海盐主要是通过化学变化完成
C.电解熔融的氯化镁可制备镁和氯气
D.电解氯化钠溶液可以制得钠和氯气
-
合理开发和利用海水资源是世界各国研究的课题。下列对于海水利用的认识错误的是
A.海水中蕴藏有丰富的资源,人类可以大量开发,以弥补资源的短缺
B.海水可以成为廉价的资源基地,但要合理开发,综合利用
C.可以用太阳能电解海水以获取氢能源
D.人类在利用海水时要兼顾海洋生物和海洋生态平衡