-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
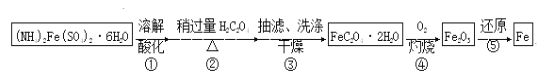
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n( )/mol )/mol | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
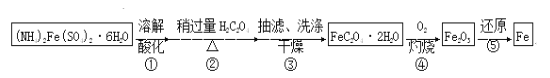
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n( )/mol )/mol | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁( ),进一步制备高纯度还原铁粉。
),进一步制备高纯度还原铁粉。
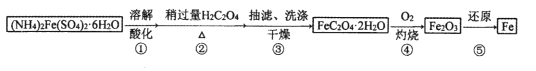
已知: 难溶于水;
难溶于水; 是二元弱酸,溶于水。
是二元弱酸,溶于水。
(1)步骤②中H2C2O4稍过量的目的是:_____________________;
(2)步骤②中得到FeC2O4.2H2O的离子反应方程式为:_________________________。
(3)实现步骤④,必须在 ______(填仪器名称)中进行,该步骤发生的化学反应方程式为:______________
(4)为实现步骤⑤,不宜用碳粉直接还原Fe2O3,理由是________________________。
(5)若将固体 放在一个可称出质量的容器内加热,
放在一个可称出质量的容器内加热, ( Mr=180)首先逐步失去结晶水,温度继续升高时.
( Mr=180)首先逐步失去结晶水,温度继续升高时. (Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g
(Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g ,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
| 温度/℃ | 25 | 150 | 300 | 350 | 400 | 450 | 500 | 600 | 700 | 800 |
| 固体质量/g | 18.00 | 16.20 | 14.40 | 14.40 | 7.20 | 7.20 | 8.00 | 8.00 | 7.73 | 7.73 |
根据上述数据计算并推断:150℃剩余的固体物质是________________(填化学式,下同);800℃剩余的固体物质是________________。
-
为充分利用资源,变废为宝,实验室里利用废铁屑制取硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]。某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4•2H2O),进一步制备高纯度还原铁粉。
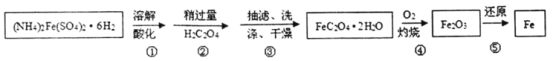
已知:FeC2O4•2H2O难溶于水,150℃开始失结晶水:H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)步骤②中,H2C2O4稍过量主要原因是_________________。
(2)为了提高步骤③得到的FeC2O4•2H2O的纯度,宜用_________________(填热水、冷水或无水乙醇)洗涤,检验洗涤是否干净的操作是_________________。
(3)实现步骤④必须用到的两种仪器是_________________(供选仪器:a.烧杯;b. 坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶):
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3, 理由是_________________。
(5)硫酸亚铁铵是重要的工业原料,其溶解性如表所示:
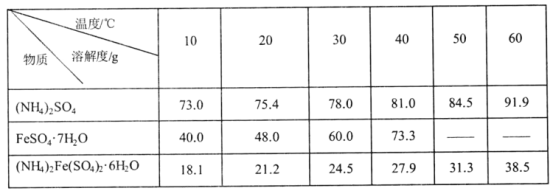
(注意:高于73.3℃,FeSO4•7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸较为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,_________________冷却,过滤,用蒸馏水洗涤铁屑至中性,将铁屑置于锥形瓶中,_________________至铁屑完全溶解,_________________,冷却结晶,用无水乙醇洗涤2-3次,低温干操。[实验中必须使用的试剂:铁屑、1.0mol•L-1的Na2CO3溶液、3.0mol•L-1的H2SO4溶液,饱和(NH4)2SO4溶液]
-
草酸亚铁(FeC2O4·nHO)溶解度冷水中0.22g,热水中0.026g,具有强还原性,常用作分析试剂及显影剂。某化学小组利用工业废铁屑设计如下装置制备草酸亚铁晶体。回答下列问题:
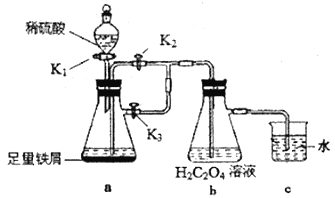
(1)实验前需将废铁屑在5%的Na2CO3溶液中加热并用蒸馏水洗涤干净,则Na2CO3溶液的作用是___________。
(2)组装好装置后首先需要检验装置的气密性,其方法是______________________。实验过程中装置c的作用是______________________。
(3)实验过程:在相应装置添加试剂后,需要让a瓶中反应先进行一段时间以排除空气,进行的操作是打开K1将一定量稀硫酸加入a瓶后关闭K1,同时还要进行的操作是___________,一段时间后,需要将a装置中的硫酸亚铁溶液导入装置b中,其操作是___________。
(4)b中生成的沉淀需过滤、洗涤、干燥,洗涤时最好选用下列试剂中的___________(填序号)。检验洗涤干净的方法是___________。
a.硫酸 b.冷水 c热水
(5)准确称取9g草酸亚铁晶体(FeC2O4·nH2O)于锥形瓶中,加入一定量硫酸溶解并加热至50℃,然后用1.0mol·L-1的KMnO4标准溶液滴定,达到滴定终点时用去30mL标准溶液。滴定反应为:10(FeC2O4·nH2O)+6KMnO4+24H2SO4=5Fe2(SO4)3+20CO2↑+6MnSO4+3K2SO4+(24+10n)H2O。
①判断滴定终点的依据为___________。②n=___________。
-
某研究小组利用乳酸钙和FeCl2为原料生产乳酸亚铁([CH3CH(OH) COO]2Fe·3H2O) 和医用二水合氯化钙晶体(CaCl2·2H2O的质量分数为97.3% ~99.3%),制备流程如下:
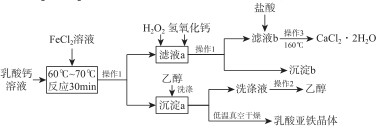
(1)实验室常用两种方案制备FeCl2,写出原子利用率为100%的反应的化学方程式 ;在FeCl2溶液中需要加
(2)制备乳酸亚铁晶体是向乳酸钙溶液中加入过量的FeCl2溶液,写出该反应的化学方程式 。
(3)操作1、操作2、操作3依次为 、 、 。
(4)向“滤液a”中先加H2O2溶,作用是 。然后再调节溶液
的 pH 约为5,目的是 。
(5)向“滤液b”加盐酸的目的是 。
(6)为测定样品中CaCl2·2H2O的含量,称取0.7600g样品并配成250mL 溶液,各取该溶液 25.00mL,分别置于三个锥形瓶中,用0.05000mol·L -1 AgNO3溶液进行三次滴定,消耗AgNO3溶液的平均体积为20.39mL。计算样品中CaCl2·2H2O的质量分数为 。
-
硫酸亚铁铵的化学式为(NH4)2SO4·FeSO4·6H2O,又名莫尔盐,是分析化学中常见的还原剂。某化学研究小组设计如下实验来制备莫尔盐并测定硫酸亚铁铵的纯度。
步骤一:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入Na2CO3溶液,加热、过滤、洗涤、干燥、称量,质量记为m1。
步骤二:FeSO4的制备。将上述铁屑加入到一定量的稀硫酸中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量记为m2。
步骤三:硫酸亚铁铵的制备。准确称取所需质量的(NH4)2SO4加入“步骤二”中的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥,称量所得晶体质量。
步骤四:用比色法测定硫酸亚铁铵的纯度。
回答下列问题:
(1)步骤三中称取的(NH4)2SO4质量为________。
(2)①铁屑用Na2CO3溶液处理的目的是_______________________________。

制备FeSO4溶液时,用右图装置趁热过滤,原因是
_______________________________________________________________。
②将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机是
________________________________________________________________________。
③比色法测定硫酸亚铁铵纯度的实验步骤为:Fe3+标准色阶的配制、待测硫酸亚铁铵溶液的配制、比色测定。标准色阶和待测液配制时除均需加入少量稀盐酸外,还应注意的问题是________________________________________________________________________。
④该实验最终通过____________________确定硫酸亚铁铵产品等级。











