-
硫酸亚铁铵的化学式为(NH4)2SO4·FeSO4·6H2O,又名莫尔盐,是分析化学中常见的还原剂。某化学研究小组设计如下实验来制备莫尔盐并测定硫酸亚铁铵的纯度。
步骤一:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入Na2CO3溶液,加热、过滤、洗涤、干燥、称量,质量记为m1。
步骤二:FeSO4的制备。将上述铁屑加入到一定量的稀硫酸中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量记为m2。
步骤三:硫酸亚铁铵的制备。准确称取所需质量的(NH4)2SO4加入“步骤二”中的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥,称量所得晶体质量。
步骤四:用比色法测定硫酸亚铁铵的纯度。
回答下列问题:
(1)步骤三中称取的(NH4)2SO4质量为________。
(2)①铁屑用Na2CO3溶液处理的目的是_______________________________。

制备FeSO4溶液时,用右图装置趁热过滤,原因是
_______________________________________________________________。
②将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机是
________________________________________________________________________。
③比色法测定硫酸亚铁铵纯度的实验步骤为:Fe3+标准色阶的配制、待测硫酸亚铁铵溶液的配制、比色测定。标准色阶和待测液配制时除均需加入少量稀盐酸外,还应注意的问题是________________________________________________________________________。
④该实验最终通过____________________确定硫酸亚铁铵产品等级。
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,可溶于水,在100℃~110℃时分解。在定量分析中常用作标定重铬酸钾、高锰酸钾等溶液的标准物质,还用于冶金、电镀等。
Ⅰ.化学课外活动小组研究莫尔盐晶体强热时的分解产物。
(1)甲组同学按照如图所示的装置进行研究,装置C中可观察到的现象是___________,由此可知分解产物中有_____________。
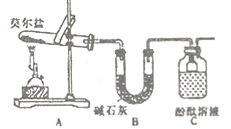
(2)乙组同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2。为进行验证,选用甲组实验中的装置A和下图所示的部分装置进行实验。
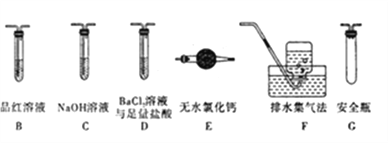
①乙组同学的实验中,装置依次连接的合理顺序为A、__________________。
②装置D中足量盐酸的作用是____________;含有SO3的实验现象是_______________。
Ⅱ.为测硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500mL溶液.甲、乙、丙三位同学设计了如下三个实验方案,请回答:
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol·L-1的酸性KMnO4溶液分三次进行滴定。
乙方案:取25.00mL硫酸亚铁铵溶液进行如下实验。
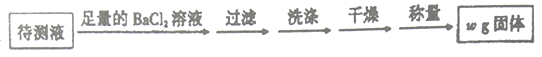
丙方案:(通过NH4+测定)实验设计图如下图所示,取25.00mL硫酸亚铁铵溶液进行该实验。
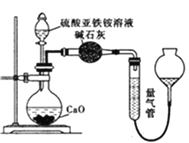
(3)甲方案中的离子方程式为______________________,若实验操作都正确,但其测定结果总是小于乙方案,可能原因为________________,验证推测的方法为___________________________________ 。
(4)乙方案中沉淀是否洗涤干净的检验方法是______________________________。
(5)丙方案中量气管中最佳试剂是__________________
a.水 b.饱和NaHCO3溶液 c.CCl4
(6)若测得NH3体积(已折算为标准状况下)为V L,则硫酸亚铁铵纯度为_________________。
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,其摩尔质量为392 g/mol,可溶于水,在100℃~ 110 ℃时分解。为探究其化学组成,甲乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如下图所示的装置进行实验,装置C中可观察到的现象是溶液变红,由此可知分解产物中有_____________。
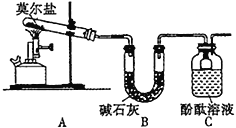
(2)乙同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验:
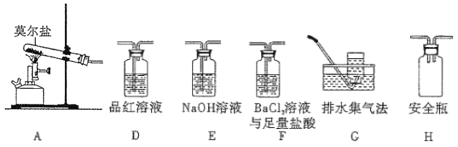
①乙组同学的实验中,装置依次连接的合理顺序为A→H→__________________________→G
②证明含有SO3的实验现象是_______________。
II.为测硫酸亚铁铵纯度,称取m g 莫尔盐样品,配成500 mL溶液。甲、乙两同学设计了如下两个实验方案。
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol•L-1的酸性K2Cr2O7溶液分三次进行滴定。
乙方案:(通过NH4+测定)设计装置如下图所示。取25.00 mL样品溶液进行该实验。
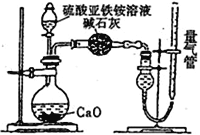
(1)滴定过程中,酸性K2Cr2O7溶液应装在_____________滴定管中。甲方案中的离子方程式为_________________________________。
(2)乙方案中量气管中最佳试剂是______(填字母)。
a.水 b.饱和NaHCO3溶液 c.CC14
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是______________________________。
(4)若测得NH3(已折算为标准状况下)为VL,则硫酸亚铁铵纯度为___________。(用含V、m的式子表示)
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,其摩尔质量为392 g/mol,可溶于水,在100℃~ 110 ℃时分解。为探究其化学组成,甲乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如下图所示的装置进行实验,装置C中可观察到的现象是溶液变红,由此可知分解产物中有_____________。
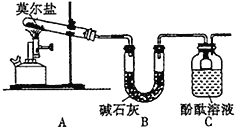
(2)乙同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验:
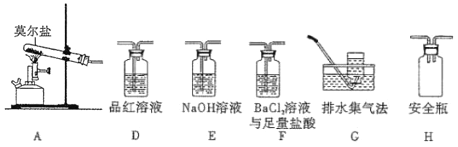
①乙组同学的实验中,装置依次连接的合理顺序为A→H→__________________________→G
②证明含有SO3的实验现象是_______________。
II.为测硫酸亚铁铵纯度,称取m g 莫尔盐样品,配成500 mL溶液。甲、乙两同学设计了如下两个实验方案。
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol•L-1的酸性K2Cr2O7溶液分三次进行滴定。
乙方案:(通过NH4+测定)设计装置如下图所示。取25.00 mL样品溶液进行该实验。
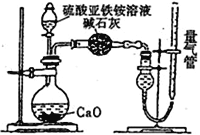
(1)滴定过程中,酸性K2Cr2O7溶液应装在_____________滴定管中。甲方案中的离子方程式为_________________________________。
(2)乙方案中量气管中最佳试剂是______(填字母)。
a.水 b.饱和NaHCO3溶液 c.CC14
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是______________________________。
(4)若测得NH3(已折算为标准状况下)为VL,则硫酸亚铁铵纯度为___________。(用含V、m的式子表示)
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] (俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
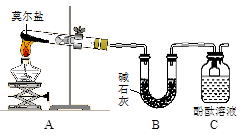
Ⅰ.探究莫尔盐晶体加热时的分解产物。
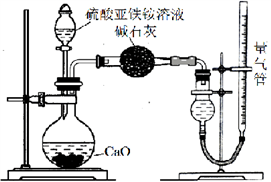
甲同学设计如右图所示的装置进行实验,装置C中可观察到的现象是____________________,由此可知分解产物中有_______________。
乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
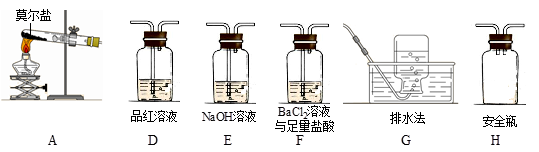
①乙同学的实验中,装置依次连接的合理顺序为:A→H→(____)→(____)→(____)→G。
②证明含有SO3的实验现象是______________;安全瓶H的作用是____。
Ⅱ.为测定硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取25.00 mL样品溶液用0.1000 mol·L-1的酸性K2Cr2O7 溶液分三次进行滴定。乙方案:(通过NH4+测定)实验设计装置如下图所示。取25.00 mL样品溶液进行该实验。
请回答:
(1)甲方案中的离子方程式为:________________________。
(2)乙方案中量气管中最佳试剂是________
a.水 b.饱和NaHCO3溶液 c.CCl4
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是________________。
(4)若测得NH3为V L(已折算为标准状况下),则硫酸亚铁铵纯度为_____(列出计算式)。
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)可溶于水,在100℃-110℃时分解。为探究其化学性质,甲、乙量同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如右图所示的装置进行实验,装置C中可观察到的现象是_____,由此可知分解产物中有_______。
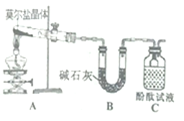
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
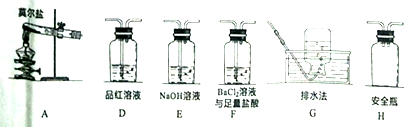
①乙同学的实验中,装置依次连接的合理顺序为: __________A→H→(_____)→(_____)→E→G。
②证明含有SO3的实验现象是__________;安全瓶H的作用是____________。
Ⅱ.为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成500mL溶液。甲、乙两位同学设计了如下两个实验方案。(已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]的分子量为392)
甲方案:取25.00mL样品溶液用0.1000 mol/L的酸性K2Cr2O7溶液分三次进行滴定。
乙方案:(通过NH4+ 测定)实验设计装置如下图所示。取25.00 mL样品溶液进行该实验。
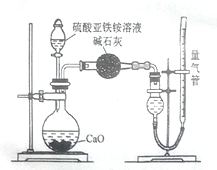
请回答:
(1)甲方案中的离子方程式为:_____________。
(2)乙方案中量气管中最佳试剂是_____________。
a.水 b.饱和NaHCO3溶液 c.CCl4
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是______________。
(4)若测得NH3(已折算为标准状况下)为V L,则硫酸亚铁铵纯度为______。
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] (俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
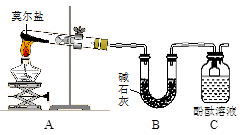
Ⅰ.探究莫尔盐晶体加热时的分解产物。
甲同学设计如右图所示的装置进行实验,装置C中可观察到的现象是____________________,由此可知分解产物中有_______________。
乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
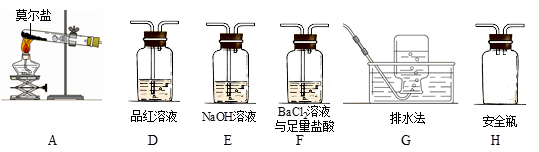
①乙同学的实验中,装置依次连接的合理顺序为:A→H→(____)→(____)→(____)→G。
②证明含有SO3的实验现象是______________;安全瓶H的作用是____。
Ⅱ.为测定硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取25.00 mL样品溶液用0.1000 mol·L-1的酸性K2Cr2O7 溶液分三次进行滴定。乙方案:(通过NH4+测定)实验设计装置如下图所示。取25.00 mL样品溶液进行该实验。
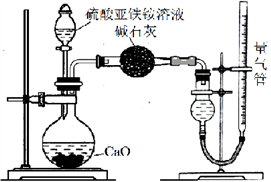
请回答:
(1)甲方案中的离子方程式为:________________________。
(2)乙方案中量气管中最佳试剂是________
a.水 b.饱和NaHCO3溶液 c.CCl4
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是________________。
(4)若测得NH3为V L(已折算为标准状况下),则硫酸亚铁铵纯度为_____(列出计算式)。
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。
(1)制备莫尔盐的流程如下:
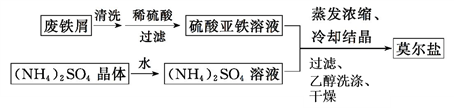
①用热的Na2CO3溶液清洗废铁屑的目的是__________。
②其中最后一步用少量无水乙醇洗涤晶体目的是________。
(2)现取0.4gCu2S和CuS的混合物在酸性溶液中用40mL0.150mol·L-1KMnO4溶液处理,发生反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O,
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O,
反应后煮沸溶液,赶尽SO2,剩余的KMnO4用0.2mol·L-1(NH4)2Fe(SO4)2溶液来滴定,完全反应消耗(NH4)2Fe(SO4)2溶液VmL。已知:MnO4-+Fe2++H+→Mn2++Fe3++H2O(未配平)
①滴定终点的现象为________。
②若V=35,试计算混合物中CuS的质量分数________(写出计算过程)。
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,是浅绿色晶体,可溶于水,在100℃~110℃时分解,常用作定量分析中的标准试剂。某化学小组以废铁屑为原料在实验室中进行实验探究——制备硫酸亚铁铵并检验其纯度,过程如下:
I.制备硫酸亚铁铵
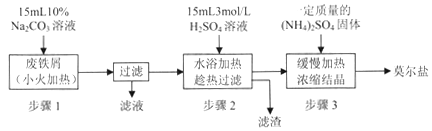
请回答下列问题:
(1)步骤l的作用是_________。(用离子方程式及必要的文字说明);
(2)步骤2中所加硫酸需过量,且不宜等到铁屑完全反应后才过滤,其中蕴含的道理是_______________;
II.测定硫酸亚铁铵的纯度
称取mg实验室制备的硫酸亚铁铵样品,配成500ml溶液,取25. 00mL硫酸亚铁按溶液,用0 . 1mol/L的酸性KMnO4溶液进行滴定,再重复滴定两次。
(3)配制(NH4)2SO4·FeSO4溶液所用的蒸馏水,通常需加热煮沸一段时间后,冷却至室温再使用,这样操作的好处是___________________;
(4)滴定时发生反应的离子方程式为___________________;
(5)滴定终点时的现象为 ___________________;
(6)三次滴定测得酸性KMnO4溶液的用量平均值为VmL,则硫酸亚铁铵样品的纯度为__________;
(7)化学小组分析发现这种检测纯度的方法不够准确,目前处理氮氧化物污染的方法有多种,请你帮助他们设计一种检测方案________________。
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,是浅绿色晶体,可溶于水,在100℃~110℃时分解,常用作定量分析中的标准试剂。某化学小组以废铁屑为原料在实验室中进行实验探究——制备硫酸亚铁铵并检验其纯度,过程如下:
I.制备硫酸亚铁铵
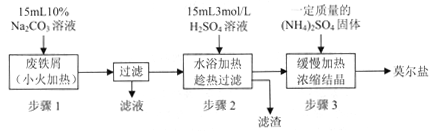
请回答下列问题:
(1)步骤l的作用是_________。(用离子方程式及必要的文字说明);
(2)步骤2中所加硫酸需过量,且不宜等到铁屑完全反应后才过滤,其中蕴含的道理是_______________;
II.测定硫酸亚铁铵的纯度
称取mg实验室制备的硫酸亚铁铵样品,配成500ml溶液,取25. 00mL硫酸亚铁按溶液,用0 . 1mol/L的酸性KMnO4溶液进行滴定,再重复滴定两次。
(3)配制(NH4)2SO4·FeSO4溶液所用的蒸馏水,通常需加热煮沸一段时间后,冷却至室温再使用,这样操作的好处是___________________;
(4)滴定时发生反应的离子方程式为___________________;
(5)滴定终点时的现象为 ___________________;
(6)三次滴定测得酸性KMnO4溶液的用量平均值为VmL,则硫酸亚铁铵样品的纯度为__________;
(7)化学小组分析发现这种检测纯度的方法不够准确,目前处理氮氧化物污染的方法有多种,请你帮助他们设计一种检测方案________________。





















