-
已知断裂1mol化学键吸收的能量或形成1mol化学键释放的能量称为键能,部分物质的键能如下表所示:
| 化学键 | C-H | C=O | N-H | C-N | H-O |
| 键能(kJ/mol) | a | b | c | d | e |
甲醛制备乌洛托品的反应如下,6 (g) + 4NH3(g) →
(g) + 4NH3(g) →  + 6H2O(l)
+ 6H2O(l)
该反应的⊿H为 ( )
A. 6(a+b+c-d-e)kJ/mol B. 6(d+e-a-b-c)kJ/mol
C. 6(b+2c-2d-2e)kJ/mol D. 6(2d+2a+2e-b-3c)kJ/mol
-
已知:①1mol H2分子中化学键断裂时需要吸收436kJ的能量
②1mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2mol氯化氢气体,反应的△H=﹣183kJ/mol
D.氢气和氯气反应生成1mol氯化氢气体,反应的△H=﹣183kJ/mol
-
已知:①1mol H2分子中化学键断裂时需要吸收436kJ的能量
②1mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1mol HCl分子时释放431kJ的能量
下列叙述正确的是( )
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
-
已知:①1 mol H2 分子中化学键断裂时需要吸收 436kJ 的能量
②1 mol Cl2 分子中化学键断裂时需要吸收 243kJ 的能量
③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量
则下列叙述正确的是( )
A. 氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g) + Cl2(g) = 2HCl(g)
B. 氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =-183kJ/mol
C. 氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H = 183kJ/mol
D. 氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H =-183kJ/mol
-
已知:①1 mol H2 分子中化学键断裂时需要吸收 436kJ 的能量
②1 mol Cl2 分子中化学键断裂时需要吸收 243kJ 的能量
③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量,则下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是 H2 (g) + Cl2 (g) =2HCl(g)
B.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =+183 kJ·mol-1
C.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =-183 kJ·mol-1
D.氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H =-183 kJ·mol-1
-
(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知:N≡N键的键能是948.9kJ•mol-1,H-H键的键能是436.0kJ•mol-1;由N2和H2合成1molNH3时可放出46.2kJ的热量.N-H键的键能是________.
(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:________.
-
(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷(P4)和P4O6的分子结构如图所示,
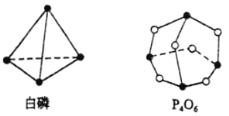
已知:
| 化学键 | P—P | P—O | O=O |
| 键能(kJ·mol1) | 198 | 360 | 498 |
则反应P4(g)+3O2(g)= P4O6(g)的△H=_________。
(2)已知①2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H= -483.6 kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+ H2(g)的△H=_______。
-
(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。
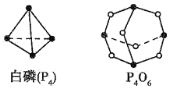
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
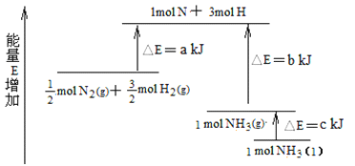
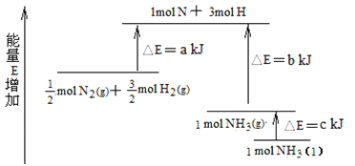
(3)化学反应N2+3H2 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
-
(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。
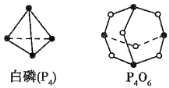
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H2 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
-
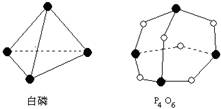
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O=O:498则反应P4(白磷)+3O2= P4O6的反应热ΔH为
A.-1638 kJ·mol-1 B.+1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
(g) + 4NH3(g) →
+ 6H2O(l)





