-
下列有关卤素的说法错误的是
A. 从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
B. HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C. 淀粉-碘化钾溶液在空气中变蓝,4I-+O2+2H2O===2I2+4OH-
D. 碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
高二化学单选题中等难度题查看答案及解析
-
下列有关性质的比较,不能用元素周期律解释的是
A. 酸性:HCl>HF B. 金属性:Na>Mg
C. 碱性:KOH>NaOH D. 热稳定性:HCl>HBr
高二化学单选题中等难度题查看答案及解析
-
下列事实中与氢键的形成有关的是( )
A.水加热到比较高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.水和乙醇分别与金属钠反应,前者比后者剧烈
D.HF 、 HCl 、 HBr 、 HI 的热稳定性依次减弱
高二化学单选题简单题查看答案及解析
-
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是( )
a.HCl、HBr、HI水溶液的酸性
b.Cl2、Br2、I2的熔点
c.HCl、HBr、HI的热稳定性
d.Cl2、Br2、I2的氧化性
(3)工业上,通过如下转化可制得KCl03晶体:

②Ⅱ反应过程能析出KCIO3晶体而无其他晶体析出的原因是
(4)一定条件下,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。
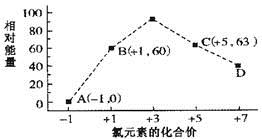
①D是_________(填离子符号)。
②B→A+c反应的热化学方程式为___________(用离子符号表示)。
高二化学填空题简单题查看答案及解析
-
下列说法正确的是
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的还原性依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
高二化学单选题简单题查看答案及解析
-
下列说法正确的是( )
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
高二化学选择题简单题查看答案及解析
-
下列说法不正确的是
A.Na、Mg、Al金属性依次减弱
B.HF、HCl、HBr、HI气态氢化物的稳定性依次减弱
C.H3PO4、H2SO4、HClO4的酸性依次增强
D.F2、Cl2、Br2、I2单质的氧化性依次增强
高二化学单选题简单题查看答案及解析
-
下列关系不正确的是( )
A.酸性:HClO4﹥H2SO4﹥H2SiO3
B.原子半径:K﹥Na﹥S﹥F
C.金属性:Na﹥Mg﹥Al
D.氢化物的沸点:HF﹤HCl﹤HBr﹤HI
高二化学单选题中等难度题查看答案及解析
-
下列有关物质性质的变化可以用元素周期律解释的是( )
A. 酸性:HCl>H2S>H2O B. 密度:Na>K>Li
C. 沸点:NH3>AsH3>PH3 D. 稳定性:HF>HCl>HBr
高二化学单选题中等难度题查看答案及解析
-
下列有关物质性质的变化可以用元素周期律解释的是( )
A. 酸性:HCl>H2S>H2O B. 密度:Na>K>Li
C. 沸点:NH3>AsH3>PH3 D. 稳定性:HF>HCl>HBr
高二化学单选题中等难度题查看答案及解析