-
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是( )
A.Y、Z两元素的简单离子的半径Y>Z
B.Y元素最高价氧化物对应水化物的化学式为H2YO4
C.原子序数由小到大的顺序为W<X<Y<Z
D.X与W可以形成W2X、W2X2两种化合物
高二化学选择题困难题查看答案及解析
-
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A. X与W可以形成W2X、W2X2两种氧化物
B. 原子半径由小到大的顺序为:W<X<Z<Y
C. Y、Z两元素的气态氢化物中,Z的气态氢化物稳定
D. Y元素最高价氧化物对应水化物的化学式为H2YO4
高二化学单选题简单题查看答案及解析
-
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A. X与W可以形成W2X、W2X2两种氧化物
B. 原子半径由小到大的顺序为:W<X<Z<Y
C. Y、Z两元素的气态氢化物中,Z的气态氢化物稳定
D. Y元素最高价氧化物对应水化物的化学式为H2YO4
高二化学选择题简单题查看答案及解析
-
A、X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置____________,位于周期表_____区;Q原子的核外电子排布式为________。
(2) X、Y、Z元素的第一电离能由大到小的顺序是________________。
(3)TZ3分子为________分子(填“极性”或“非极性”),YZ2-离子的VSEPR模型名称是________。(每空2分)
(4)Z和T的简单气态氢化物稳定性好的是_______(填化学式),原因是________________________________________________________________。
(5) A、X、Z、可形成分子式为A2XZ的有机物,则该化合物分子中B原子的轨道杂化类型是________;1mol该分子中含有π键的数目是________。
(6)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为配位数不变的+3价配离子.该反应的离子方程式是________________________________________________________________________。
高二化学简答题困难题查看答案及解析
-
x、Y、z、w是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属元素.x原子的最外层电子数与次外层电子数相等,Y原子的最外层电子数与次外层电子数之比为3:1,X与w两原子的最外层电子数之和为9,Z的单质既可与盐酸反应,又能与浓的NaOH溶液反应.据以上信息请回答下列问题.
(1)X的元素符号为:______,W元素在元素周期表中的位置是______ w与Y可以按原子个数比1:2形成一种高效安全灭菌消毒剂,其化学式为______
(2)两种非金属元素的气态氢化物中沸点较高是______(用化学式填写).
(3)将Z元素的氧化物投入到一定量盐酸中恰好完全反应,向反应后的溶液中逐滴加入氢氧化钠溶液至过量,现象为______
(4)以海水中含量最大的物质为原料可以生产w的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为______ 2NaOH+H2↑+Cl2↑高二化学解答题中等难度题查看答案及解析
-
(12分)化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为________;Y的电子排布式为________;Z的电子排布式为________;YX2的化学式是________,电子式是________ ;ZX2的化学式是________
高二化学填空题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9 ,单质Y可与NaOH溶液反应生成氢气。下列说法不正确的是
A.原子半径:Y>Z>W
B.XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体
C.YW3水溶液蒸干并灼烧可得固体YW3
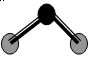
D.ZW2分子结构见上图,说明ZW2是极性分子
高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9 ,单质Y可与NaOH溶液反应生成氢气。下列说法不正确的是
A.原子半径:Y>Z>W
B.XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体
C.电解YW3固体可得单质Y
D.ZW2分子结构见上图,说明ZW2是极性分子
高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________。
(2)ZW2的电子式是________,它在常温下呈液态,形成晶体时,属于________晶体。
(3)工业生产单质Y的原理是(用化学方程式表示)________。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是________
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是_______比________。
高二化学填空题简单题查看答案及解析
-
M、N、R均为短周期主族元素,它们原子的最外层电子数之和为10,M与R同族,N最外层电子数等于M次外层电子数,且N原子半径大于R原子半径。下列叙述不正确的是( )
A.熔点:M的氧化物比N的氧化物高
B.热稳定性:M的氢化物大于R的氢化物
C.M与R形成的是共价化合物RM
D.N的单质能溶于浓硝酸,R的单质不溶于浓硝酸
高二化学单选题困难题查看答案及解析