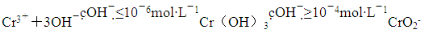-
金属加工前常用盐酸对金属表面氧化物进行清洗,会产生酸洗废水。pH在2左右的某酸性废水含铁元素质量分数约3%,其他金属元素如铜、镍、锌浓度较低,综合利用酸洗废水可制备三氯化铁。制备过程如下:
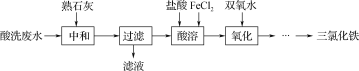
相关金属离子生成氢氧化物沉淀的pH如下表:
| Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 |
| 沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 |
回答下列问题:
(1)“中和”时调节pH至________,有利于后续制备得纯度较高的产品。
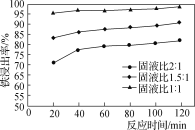
(2)处理酸洗废水中和后的滤渣,使铁元素浸出。按照不同的固液比投入“过滤”后滤渣和工业盐酸进行反应的铁浸出率如图所示,实际生产中固液比选择1.5∶1的原因是__________________。
(3)写出“氧化”中发生反应的离子方程式:____________________________________。
(4)“酸溶”后需根据溶液中Fe2+含量确定氧化剂的投入量。用K2Cr2O7标准溶液测定Fe2+(Cr2O 被还原为Cr3+)的含量,该反应离子方程式为____________________________。
被还原为Cr3+)的含量,该反应离子方程式为____________________________。
(5) 将三氯化铁溶液在一定条件下________、________、过滤、洗涤、在氯化氢气氛中干燥得FeCl3·6H2O晶体,在实验室过滤装置中洗涤固体的方法是___________________。
-
金属蚀刻加工过程中,常用盐酸对其表面氧化物进行清洗,会产生酸洗废水。 pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,其他金属元素如铜、镍、锌、 铬浓度较低,工业上综合利用酸洗废水可制备三氯化铁。制备过程如下:
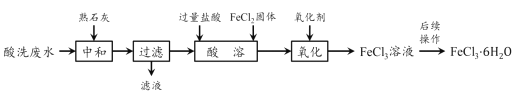
相关金属离子生成氢氧化物沉淀的pH如下表所示:
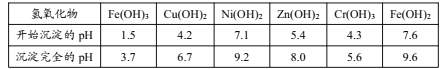
回答下列问题:
(1)“中和”时发生反应的化学方程式为__________________,调节pH至________范围,有利于后续制备得纯度较高的产品。
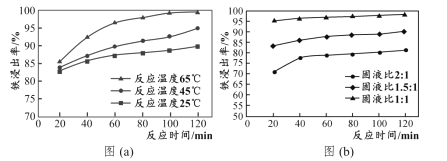
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下 铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为_______________。按照不同的固液比(滤渣和工业盐酸的投入体积比)进行反应时,铁浸出率随时间变化如 图(b)所示,实际生产中固液比选择1.5:1的原因是___________。
(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2mol∙L−1,则需投入的氧化剂过氧化氢的质量为_____________。
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,此时阴极的电极反应式为____,电解总反应的离子方程式是 ___。
(5)将得到的FeCl3溶液在HCl气氛中_________、过滤、洗涤、干燥得FeCl3∙6H2O晶体。
-
金属蚀刻加工过程中,常用盐酸对其表面氧化物进行清洗,会产生酸洗废水。 pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,其他金属元素如铜、镍、锌、 铬浓度较低,工业上综合利用酸洗废水可制备三氯化铁。制备过程如下:
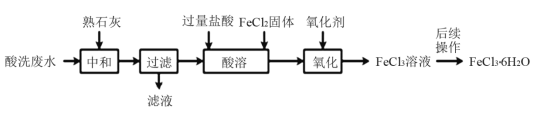
相关金属离子生成氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 | 4.3 | 7.6 |
| 沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 | 5.6 | 9.6 |
回答下列问题:
(1)“中和”时发生反应的化学方程式为__________________,调节pH至________范围,有利于后续制备得纯度较高的产品。
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下 铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为_______________。按照不同的固液比(滤渣和工业盐酸的投入体积比)进行反应时,铁浸出率随时间变化如图(b)所示,实际生产中固液比选择1.5:1的原因是___________。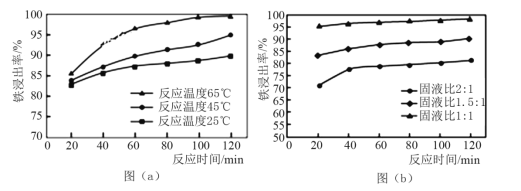
(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2mol∙L−1,则需投入的氧化剂过氧化氢的质量为__________。
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,此时阴极的电极反应式为__________,电解总反应的离子方程式是 __________。
(5)将得到的FeCl3溶液在HCl气氛中______、______、过滤、洗涤、干燥得FeCl3∙6H2O晶体。
-
铜的硫化物可用于冶炼金属铜。为测定某试样中Cu2S、CuS的质量分数,进行如下实验:
步骤1:在0.7500g试样中加入100.00 mL 0.1200mol/mol KMnO4的酸性溶液,加热,硫元素全部转化为SO42-,铜元素全部转化为Cu2+,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250 mL容量瓶中,定容。取25.00 mL溶液,用0.1000mol/molFeSO4溶液滴定至终点,消耗16.00 mL。
步骤3:在步骤2滴定所得溶液中滴加氨水至出现沉淀,然后加入适量NH4HF2溶液(使Fe、Mn元素不参与后续反应),加入约1gKI固体(过量),轻摇使之溶解并发生反应:2Cu2++4I-=2CuI↓+I2。用0.05000mol/molNa2S2O3溶液滴定至终点(离子方程式为2S2O32-+I2 2I-+S4O62-),消耗14.00 mL。
2I-+S4O62-),消耗14.00 mL。
已知:酸性条件下,MnO4-的还原产物为Mn2+。
(1)若步骤3加入氨水产生沉淀时,溶液的pH=2.0,则溶液中c(Fe3+)=___________。
(已知室温下Ksp[Fe(OH)3]=2.6×10-39)
(2)步骤3若未除去Fe3+,则测得的Cu2+的物质的量将___________(填“偏高”“偏低”或“不变”)。
(3)计算试样中Cu2S和CuS的质量分数(写出计算过程)。
-
铜的硫化物可用于冶炼金属铜。为测定某试样中Cu2S、CuS的质量分数,进
行如下实验:
步骤1:在0.7500g试样中加入100.00 mL 0.1200mol/L KMnO4的酸性溶液,加热,硫元素全部转化为SO42-,铜元素全部转化为Cu2+,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250 mL容量瓶中,定容。取25.00 mL溶液,用0.1000mol/L FeSO4溶液滴定至终点,消耗16.00 mL。
步骤3:在步骤2滴定所得溶液中滴加氨水至出现沉淀,然后加入适量NH4HF2溶液(使Fe、Mn元素不参与后续反应),加入约1gKI固体(过量),轻摇使之溶解并发生反应:2Cu2++4I-=2CuI↓+I2。用0.05000mol/L Na2S2O3溶液滴定至终点(离子方程式为2S2O32-+I2 2I-+S4O62-),消耗14.00 mL。
2I-+S4O62-),消耗14.00 mL。
(1)写出Cu2S与KMnO4酸性溶液反应的化学方程式________________
(2)步骤3中加入氨水的目的为__________________;如果未加入氨水,则测得的Cu2+的物质的量将__________(填“偏高”“偏低”或“不变”),混合固体中CuS的质量分数将__________(填“偏高”“偏低”或“不变”)
(3)当加入氨水使得溶液pH=2.0时,则溶液中c(Fe3+)=____________,
(4)根据题中数据,计算混合固体中Cu2S的质量分数w(Cu2S)=______CuS的质量分数w(CuS)=_______
-
(14分)铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(一)工业废水中含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶 液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是 。
(2)阴极附近溶液pH升高的原因是 (用电极反应式解释)溶液中同时生成的沉淀还有 。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在4000C以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁粉涉及的主要生产流程如下:

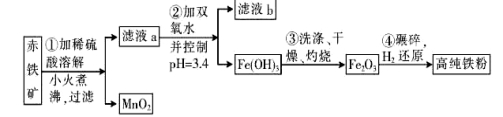
已知:①某赤铁矿石含60.0% Fe2O3、3.6% FeO,还含有A12O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:

(3)步骤②中加双氧水的目的是 ,pH控制在3. 4的作用是 。已知25°C时,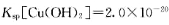 ,该温度下反应:Cu2++2H2O
,该温度下反应:Cu2++2H2O Cu(OH)2+2H+的平衡常数K= 。
Cu(OH)2+2H+的平衡常数K= 。
(4)如何判断步骤③中沉淀是否洗涤干净?
(5)制备氮化铁磁粉的反应: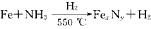 (未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为 。
(未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为 。
-
铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(―)工业废水中含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是________。
(2)阴极附近溶液pH升高的原因是_________(用电极反应式解释);溶液中同时生成的沉淀还有 。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在400℃以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁粉涉及的主要生产流程如下:
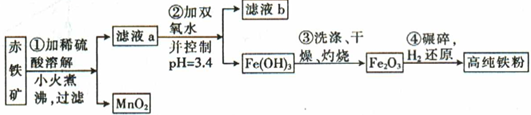
已知①某赤铁矿石含60.0%Fe2O3、3.6%FeO,还含有Al2O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:

(3)步骤②中加双氧水的目的是________,pH控制在3.4的作用是________,已知25℃时,Ksp[Cu(OH)2] =2.0 10-20,该温度下反应:Cu2++2H2O
10-20,该温度下反应:Cu2++2H2O Cu(OH)2+2H+的平衡常数K=________。
Cu(OH)2+2H+的平衡常数K=________。
(4)如何判断步骤③中沉淀是否洗涤干净?________。
(5)制备氮化铁磁粉的反应:Fe+NH3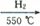 FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为________________。
FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为________________。
-
铁是地壳中含量第二的金属元素,其单质、合金化合物在生产生活中的应用广泛。
(一)工业废水中有一定量的Cr2O72--和CrO42-,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是____________________________________________________。
(2)阴极附近溶液pH升高的原因是___________(用电极反应式解释);溶液中同时生成的沉淀还有___________。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在400℃以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁涉及的主要生产流程如下:
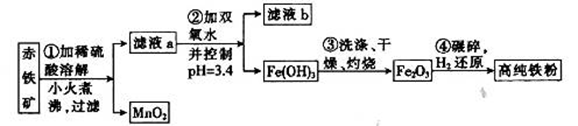
已知:①某赤铁矿石含60.0 Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH:

(3)步骤②中加双氧水的目的是__________________,pH控制在3.4的作用是_______________________;已知25℃时,Ksp[Cu(OH) 2] =2.0×10-20,该温度下反应:Cu2++2H2O Cu(OH) 2+2H+的平衡常数K=_______。
Cu(OH) 2+2H+的平衡常数K=_______。
(4)如何判断步骤③中沉淀是否洗涤干净?_____________________________________。
-
铬(Cr)属于重金属元素,含铬的废水和废渣排放必须经过处理达到有关的安全标准。
(1)铬原子核中质子数为24,铬位于周期表中第______周期。
(2)铬元素以Cr2O72-的形式存在于酸性废水中,常用FeSO4将其还原为Cr3+,再用沉淀法进行分离。已知:
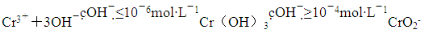
①FeSO4还原Cr2O72-的离子方程式为______________________________________________。
②Cr2(SO4)3溶液中加入过量NaOH浓溶液,反应的离子方程式为_____________________。
③沉淀法分离废水中的Cr3+,pH应控制的范围是________。
④下列关于铬及其化合物的说法中正确的是________。
A.K2Cr2O7是一种常用的强氧化剂
B.酸性K2Cr2O7溶液可用于检验司机是否酒后驾车
C.金属铬硬度大、耐腐蚀,是常用的镀层金属
-
下列应用中,主要利用物质氧化性的是
A.用烟道气中和碱性废水 B.重铬酸钾用于酒驾检查
C.用苯酚制造酚醛树脂 D.金属加工前用硫酸酸洗


被还原为Cr3+)的含量,该反应离子方程式为____________________________。







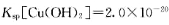 ,该温度下反应:Cu2++2H2O
,该温度下反应:Cu2++2H2O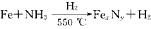 (未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为
(未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为

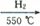 FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为________________。
FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为________________。