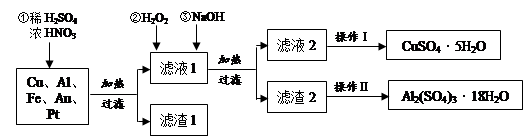-
碱式碳酸铜是一种用途广泛的化工原料,明矾是种常见的净水剂,某校化学兴趣小组探究将一废弃矿石进行处理制备碱式碳酸铜和明矾,从而实现变废为宝。经查资料:该矿石成分为:Al2Fe4CuSi2O13,该化学小组制定工艺流程如下:
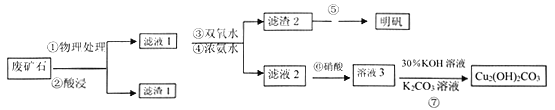
己知:Cu2+溶于足量的浓氨水中可形成铜氨溶液:Cu2++4NH3·H2O Cu(NH3)42++4H2O
Cu(NH3)42++4H2O
回答下列问题:
(1)将Al2Fe4CuSi2O13改写成氧化物形式___________;
(2)为了步骤②提高酸浸速率,可采取措施有________,_________(任写两种);
(3)写出步骤⑥的离子方程式__________;
(4)用从滤渣2到明矾需先后加入_____、____两种试剂(按使用顺序填写化学式);
(5)在步骤⑦中,若先加K2CO3溶液,后加KOH溶液,则易发生
CuCO3(s)+2OH-(aq)  Cu(OH)2(s)+CO32-(aq),则该反应平衡常数为:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
Cu(OH)2(s)+CO32-(aq),则该反应平衡常数为:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
(6)为了检验该碱式碳酸铜纯度,该小组称取25g样品,加入到100mL 3mol/L的盐酸中进行溶解。充分反应后,微热排除CO2,冷却后取出10mL,滴加2滴甲基橙,然后用2mol/L标准KOH溶液进行滴定,共用去5mL。则样品的纯度为_________
-
碱式碳酸铜是一种用途广泛的化工原料,明矾是种常见的净水剂,某校化学兴趣小组探究将一废弃矿石进行处理制备碱式碳酸铜和明矾,从而实现变废为宝。经查资料:该矿石成分为:Al2Fe4CuSi2O13,该化学小组制定工艺流程如下:

己知:Cu2+溶于足量的浓氨水中可形成铜氨溶液:Cu2++4NH3·H2O Cu(NH3)42++4H2O
Cu(NH3)42++4H2O
回答下列问题:
(1)将Al2Fe4CuSi2O13改写成氧化物形式___________;
(2)为了步骤②提高酸浸速率,可采取措施有________,_________(任写两种);
(3)写出步骤⑥的离子方程式__________;
(4)用从滤渣2到明矾需先后加入_____、____两种试剂(按使用顺序填写化学式);
(5)在步骤⑦中,若先加K2CO3溶液,后加KOH溶液,则易发生
CuCO3(s)+2OH-(aq)  Cu(OH)2(s)+CO32-(aq),则该反应平衡常数为:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
Cu(OH)2(s)+CO32-(aq),则该反应平衡常数为:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
(6)为了检验该碱式碳酸铜纯度,该小组称取25g样品,加入到100mL 3mol/L的盐酸中进行溶解。充分反应后,微热排除CO2,冷却后取出10mL,滴加2滴甲基橙,然后用2mol/L标准KOH溶液进行滴定,共用去5mL。则样品的纯度为_________
-
(14分)某化学兴趣探究小组将一批废弃的线路板简单处理后,得到含Cu(70%)、Al(25%)、Fe(4%)及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
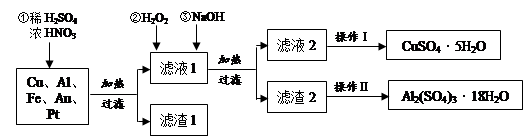
(1)在金属混合物与酸的反应中,表现氧化性的离子为________;得到滤渣1的主要成分为________。
(2)第②步加H2O2后发生反应的离子方程式为________;
通过加入NaOH调节溶液的pH,其目的是________;
(3)操作Ⅰ中包括的实验步骤有________、过滤;
(4)通过操作Ⅱ可以由滤渣2制取Al2(SO4)3·18H2O 。下列是操作Ⅱ的一种实验方案。

实验中:试剂1是________,试剂2是________。(填化学式)
-
(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
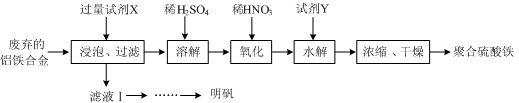
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;
浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
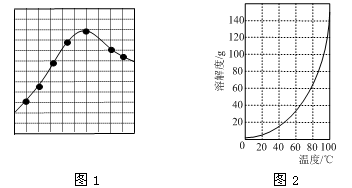
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料,试剂X应为 。
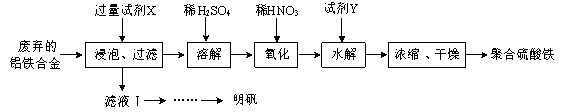
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH) x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
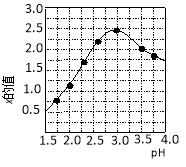
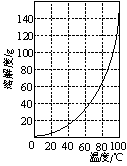
图1 图2
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
(15分)铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
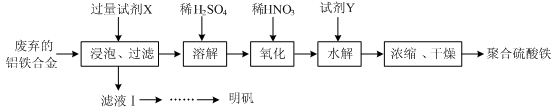
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
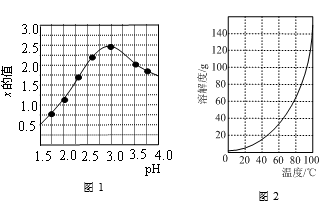
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
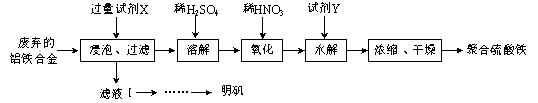
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH) x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
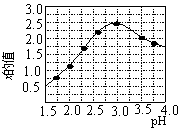
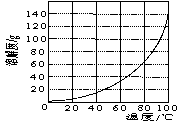
图1 图2
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
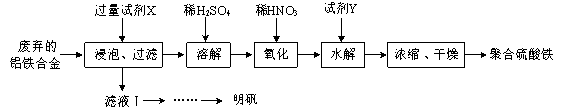
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
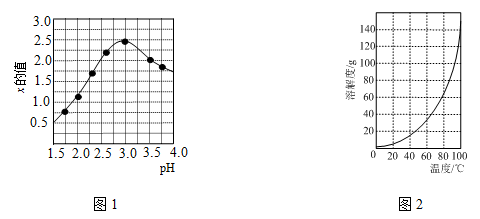
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生,过滤, 。将溶液 、 、过滤、并用酒精洗涤、干燥,最终得到明矾晶体。
-
(本题共12分)聚合氯化铝(PAC)的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种新兴的高效净水剂。
某兴趣小组尝试以工业废弃物铝灰为原料,利用酸溶法制备聚合氯化铝,主要流程如下:

完成下列填空:
40.用37.5%的浓盐酸配置100 mL 6 mol/L盐酸,所需的玻璃仪器有量筒、烧杯、_______。
41.步骤III调节pH至4.0~4.5,其目的是___________________________。为使得到的PAC晶体较纯净,所用的X物质可以是_______(填编号)。
a.氨水 b.铝 c.氢氧化铝 d.偏铝酸钠
42.步骤IV需要保持温度在85℃,可采用的加热方法是_____________。
43.为测定PAC样品中n的值,可以采用如下方法:
①称取一定质量样品,充分研碎后在_________(填仪器名称)中加热、灼烧至质量不再变化,得到1.020g固体,其成分是_________(填化学式)。
②另称取相同质量的样品,用_________(填化学式)溶解后,加入足量AgNO3溶液,得到3.157 g白色沉淀。
由上可知,该PAC样品中n的值为___________。
44.也可用烧碱溶解铝灰,再用稀盐酸调节pH至4.0~4.5,该法称为“碱溶法”。与“酸溶法”相比,“碱溶法”的缺点是______________________________(任写一点)。
-
聚合硫酸铁、明矾可用作净水剂。某课题组拟以废弃的铝铁合金为原料制备聚合硫酸铁和明矾,设计化工流程如下:
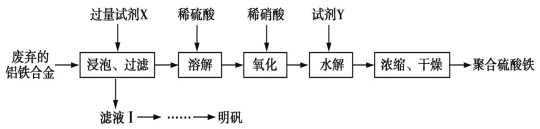
(1)聚合硫酸铁能溶于水,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①在聚合硫酸铁中,x、y之间的关系是_______。试剂X中溶质的化学式为________。
②上述流程图中的“氧化”设计存在缺陷,请提出改进意见;____________________为了降低聚合硫酸铁的溶解度,在浓缩过程中加入适量的溶剂是________(填结构简式)。
③加入试剂Y的目的是为了调节溶液的PH,若Y为氧化物,写出调节PH的离子方程式:________;溶液的pH对[Fe2(OH)x(SO4)y]n中x的值有较大影响(如图A所示),试分析pH过小(pH≤3.0)导致聚合硫酸铁中x的值减小的原因:________。
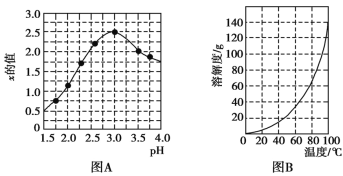
(2)明矾的化学式为KAl(SO4)2·12H2O。图B为明矾的溶解度随温度变化的曲线,由滤液Ⅰ制备明矾晶体的流程如下(供选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):
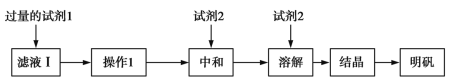
①试剂1是____;操作1的名称是________。
②结晶措施是________。

Cu(NH3)42++4H2O
Cu(OH)2(s)+CO32-(aq),则该反应平衡常数为:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。