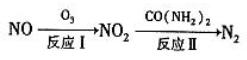-
研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:NO NO2
NO2 N2
N2
已知:NO(g)+O3(g)=NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-116.2 kJ·mol-1
则反应Ⅰ的热化学方程式为_____________________________________________。
(2)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g) ΔH>0,请你分析该设想能否实现并说明理由是____________________________________________。
(3)甲酸的电离平衡常数Ka=1.70×10-4。向20 mL 0.1 mol·L-1的甲酸钠溶液中滴加10 mL 0.1 mol·L-1的盐酸,混合液呈________(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序为______________________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.100 0 mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
| 温度 | 固体活性炭/mol | NO/mol | A/mol | B/mol |
| 200 ℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
| 335 ℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为________(填“吸热”或“放热”)反应。
②200 ℃时,平衡后向恒容容器中再充入0.1 mol NO,再次平衡后,NO的百分含量将________(填“增大”“减小”或“不变”)。
③计算反应在335 ℃时的平衡常数为________。
(5)工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5~26.5℃后用氨水吸收过量的CO2,该反应的化学方程式为_______________________。在用氨水吸收前,烟气需冷却至15.5~26.5℃的可能原因是____________________________。
-
研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1) 氧化还原法消除NOx的转化如下:

已知: NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ/mol
2NO(g)+O2(g)=2NO(g) △H=-116.2kJ/mol
则NO 与O3 只生成NO2 的热化学方程式为_____________________。
(2) 有人设想将CO按下列反应除去: 2CO(g)=2C(s)+O2(g) △H>0,请你分析该反应能否自发进行?_____( 填“是”或“否”),依据是_____________________。
(3)活性炭也可用于处理汽车尾气中的NO。在2L.恒容密闭容器中加入0.1000mo1NO和2.030mol 固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如下表:
| 固体活性炭/mol | NO/mol | A/mol | B/mol |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 |
①结合上表的数据,写出NO与活性炭反应的化学方程式______ 该反应的正反应为_______(填”吸热”或“放热”)反应。
②200℃时,平衡后向恒容容器中再充入0.1000mo1NO,再次平衡后,NO 的体积分数将____。(填“增大”、“减小”或“不变”)。
(4) 用亚硫酸钠溶液吸收二氧化硫得到亚硫酸氢钠溶液,然后电解该溶液可制得硫酸,电解原理示意图如图所示。请写出开始时阳极的电极反应式______________。

(5)常温下,Ksp(BaCO3) =2.5×10-9,Ksp(BaSO4) =1.0×10-10,控制条件可实现如下沉淀转换:
BaSO4(s)+CO32-(aq)=BaCO3(s)+SO42-(aq) ,该反应平衡常数K的表达式为:K=_______,欲用1LNa2CO3 溶液将0.01molBaSO4 全部转化为BaCO3,则Na2CO3 溶液的最初浓度应不低于_________。
-
研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:
已知:NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ/mol
2NO(g)+O2(g)=2NO(g) △H=-116.2kJ/mol
则反应I的热化学方程式为________________。
(2)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g) △H>0,请你分析该设想能否实现?______(填“是”或“否”) ,依据是_____________。
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。已知常温时,甲酸的电离平衡常数Ka=1.70×10-4。
① 甲酸钠的水溶液呈碱性,请用离子反应方程式表示其原因___________。
② 向20mL 0.1mol/L的甲酸钠溶液中滴加10ml 0.1mol/L的盐酸,混合液呈______性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为______________。
(4)活性炭也可用于处理汽车尾气中的NO。在2L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如下表:

①该反应的正反应为________(填”吸热”或“放热”)反应。
② 200℃时,平衡后向恒容容器中再充入0.1molNO,再次平衡后,NO的百分含量将_____。(填“增大”、“减小”或“不变”)。
③计算反应体系在335℃ 时的平衡常数_______。
-
(M分)研究碳、氮及其化合物的转化对于环境的改善有重大意义。氧化还原法消除NOx的转化如下:NO NO2
NO2 N2
N2
已知:NO(g)+O3(g)==NO2(g)+O2(g) △H=-200.9kJ·mol-1
2NO(g)+O2(g)==2NO2(g) △H=-2116.2kJ·mol-1
(1)则反应I的热化学方程式为_________________。
(2)有人设想将CO按下列反应除去:2CO(g)==2C(s)+O2(g) △H >0,你认为该设想能
否实现并说明理由:_____________________。
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。己知常温时,甲酸的电离平衡常数Ka= l.70×10-4。向20 mL 0.1 mol/L的甲酸钠溶液中滴加10mL 0.1 mol/L的盐酸,混合液呈_____(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序
为_____________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.1000 mol NO和2.030 mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如下表:
| 固体活性炭/mol | NO/mol | A/mol | B/mol |
| 200℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
| 335℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为_________(填“吸热”或“放热”)反应。
②200℃时,平衡后向恒容容器中再充入0.100 0 mol NO,再次平衡后,NO的百分含量将__________(填“增大”“减小”或“不变”)。
③计算反应体系在335℃时的平衡常数_______________。
(5)CO2的处理方法有多种,将少量CO2气体通入石灰乳中充分反应,达到平衡后,测得溶液中c(OH-)=c mol/L,则c(CO32-)=_____ mol·L-1(用含a、b、c的代数式表示)。(已知Kap(CaCO3)=a,Kap[Ca(OH)2]=b)
-
良好生态环境是最普惠的民生福祉。治理大气污染物CO、NOX、SO2具有十分重要的意义。
(1)氧化还原法消除NOX的转化如下所示: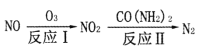 。反应I为NO+O3===NO2+O2,其还原产物是_________。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________。
。反应I为NO+O3===NO2+O2,其还原产物是_________。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________。
(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。
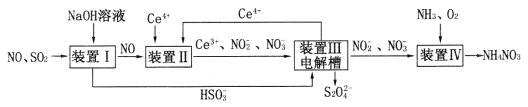
装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式_______________。装置III中发生反应的离子方程式为_________________。
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气____L(用含a代数式表示)。
-
汽车尾气中 CO、NOx 以及燃煤废气中的 SO2 都是大气污染物, 对它们的治理具有重要意义。
(1)氧化还原法消除 NOx 的转化如下: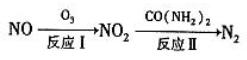
①反应 I 为 NO +O3=NO2+O2,生成标准状况下 11.2 L O2 时,转移电子的物质的量是_______mol。
②反应Ⅱ中, 当 n( NO2): n[CO(NH2)2]=3: 2 时, 氧化产物与还原产物的质量比为_________。
(2)使用“催化转化器”可以减少尾气中的 CO 和 NOx,转化过程中发生反应的化学方程式为 CO+ NOx →N2+CO2(未配平),若 x=1.5,则化学方程式中 CO2 和 N2 的化学计量数比为_________。
(3)吸收 SO2和 NO, 获得 Na2S2O4和 NH4NO3产品的流程图如下(Ce为铈元素)。
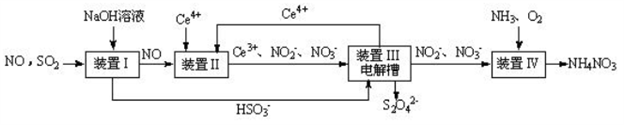
装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-、 NO2-请写出生成等物质的量的NO3-和NO2-时的离子方程式______________________。
(4)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得 Ce4+再生,再生时生成的Ce4+在电解槽的______(填“阳极”或“阴极”),同时在另一极生成S2O42一的电极反应式为_____________。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为 ag.L-1, 要使 1m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气_______L(用含 a 代数式表示,结果保留整数)。
-
近几年我国大面积发生雾霾天气,其主要原因是SO2、NOx,挥发性有机物等发生二次转化,研究碳、氮、硫及其化合物的转化对于环境的改善有重大意义。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g)  CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
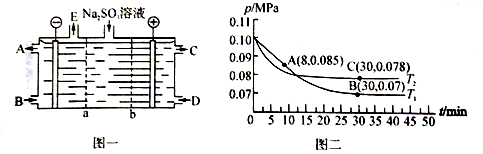
(2)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图一所示,电极材料为石墨。
① a表示_____离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品。其中C为硫酸,则A表示_______。
②阳极的电极反应式为____________________。
(3)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)  2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强与反应时间如图二所示。
2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强与反应时间如图二所示。
①图中A点时,SO2的转化率为________。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v0(正)与A点的逆反应速率vA(逆)的大小关系为v0(正)_____vA(逆) (填“>"、“<”或“ = ”)。
③图中B点的压强平衡常数Kp=______。(Kp=压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)为了清除NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理。现有由a mol NO、b molNO2、c molN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为______________。
-
近几年我国大面积发生雾霾天气,其主要原因是SO2、NOx,挥发性有机物等发生二次转化,研究碳、氮、硫及其化合物的转化对于环境的改善有重大意义。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g)  CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
(2)在3.0 L密闭容器中,通入0.10 mol CH4和0.20 mol NO2,在一定温度进行反应,反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强p/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
由表中数据计算0~4min内v(NO2)=_________,该温度下的平衡常数K=________。
(3)在一恒容装置中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率如图(横坐标为反应温度,纵坐标为NO2转化率/%):
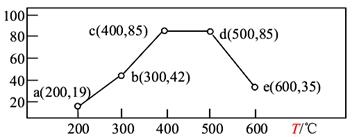
则下列叙述正确的是____________。
A.若温度维持在200℃更长时间,NO2的转化率将大于19%
B.反应速率:b点的v(逆)>e点的v(逆)
C.平衡常数:c点=d点
D.提高c点时NO2的转化率和反应速率,可适当升温或增大c(CH4)
(4)用0.05 mol·L-1Na2S溶液吸收上述甲烷中含有的H2S气体,当吸收的H2S的物质的量与原Na2S的物质的量相等时溶液显碱性,此时溶液中有关粒子的表达式正确的是( )
A.n(Na+)=0.1 mol B.c(Na+)-c(OH-)>c(S2-)+c(HS-)-c(H+)
C.c(H2S)+c(H+)<c(S2-)+c(OH-) D.c(Na+)-c(H2S)=2c(S2-)+c(HS-)
测得25℃时溶液中的c(H2S)=1.0×10-4mol·L-1,则溶液的pH=________。
(5)将(1)中CH4+2NO2 CO2+2H2O+N2的反应设计为原电池,电池内部是掺杂氧化钇的氧化锆晶体,可以传导O2-;则电池的正极电极反应式为______________。
CO2+2H2O+N2的反应设计为原电池,电池内部是掺杂氧化钇的氧化锆晶体,可以传导O2-;则电池的正极电极反应式为______________。
-
研究氮、硫、碳及其化合物的转化对于环境的改善有重大意义,可减少如雾霾天气、酸雨、酸雾等环境污染问题。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2 (g) △H=____kJ·mol-1;
CO2(g)+2H2O(g)+N2 (g) △H=____kJ·mol-1;
(2)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g) 2SO3(g)。在一定温度和压强下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强在不同温度下与反应时间如图1所示。
2SO3(g)。在一定温度和压强下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强在不同温度下与反应时间如图1所示。
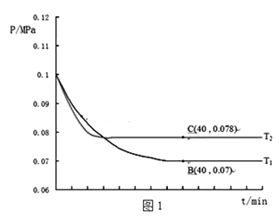
① 图1中C点时,SO2的转化率为_______。
② 图1中B点的压强平衡常数Kp=_______。(Kp=压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)已知4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH1=-1800 kJ·mol-1,将2 mol NH3、3 mol NO的混合气体分别置于a、b、c三个10 L恒容密闭容器中,使反应在不同条件下进行,反应过程中c(N2)随时间的变化如图2所示。
5N2(g)+6H2O(g) ΔH1=-1800 kJ·mol-1,将2 mol NH3、3 mol NO的混合气体分别置于a、b、c三个10 L恒容密闭容器中,使反应在不同条件下进行,反应过程中c(N2)随时间的变化如图2所示。
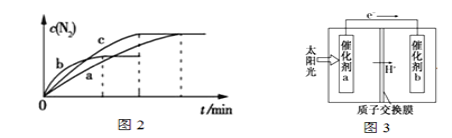
①与容器a中的反应相比,容器b中的反应改变的实验条件可能是_______,判断的依据是______________________________________。
②一定温度下,下列能说明反应已达到平衡状态的是____
A.H2O(g)与NO的生成速率相等 B.混合气体的密度保持不变
C.ΔH保持不变 D.容器的总压强保持不变
(4)利用人工光合作用,借助太阳能使CO2和H2O转化为HCOOH,如图3所示,在催化剂b表面发生的电极反应为:_____________________________________。
-
近几年我国大面积发生雾霾天气,其主要原因是SO2、NOx等挥发性有机物等发生二次转化,研究碳、氮、硫及其化合物的转化对于环境的改善有重大意义。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g)  CO2(g)+2H2O(g)+N2 (g) △H=____kJ·mol-1;该反应在____(高温,低温,任何温度)下可自发进行
CO2(g)+2H2O(g)+N2 (g) △H=____kJ·mol-1;该反应在____(高温,低温,任何温度)下可自发进行
(2)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)  2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:_____________。
2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:_____________。
A. 混合气体的密度不再发生变化 B.混合气体的平均摩尔质量不再发生变化
C.  (SO2):
(SO2): (O2):
(O2): (SO3)=2:1:2 D.混合气体的总物质的量不再发生变化
(SO3)=2:1:2 D.混合气体的总物质的量不再发生变化
(3)若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强与反应时间如下图所示。
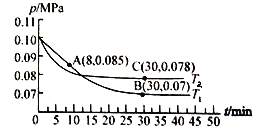
①图中A点时,SO2的转化率为________。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率 0(正)与A点的逆反应速率
0(正)与A点的逆反应速率 A(逆)的大小关系为
A(逆)的大小关系为 0(正)_____
0(正)_____ A(逆) (填“>"、“<”或“ = ”)。
A(逆) (填“>"、“<”或“ = ”)。
③图中B点的平衡常数Kp=______。(Kp=压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)为了清除NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理。现有由a mol NO、b molNO2、c molN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为____________。
NO2
N2




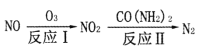 。反应I为NO+O3===NO2+O2,其还原产物是_________。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________。
。反应I为NO+O3===NO2+O2,其还原产物是_________。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________。