-
IBr、ICl等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应_______
,该反应_______ 填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。
 溴化碘
溴化碘 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为___。
溶液发生反应,发生反应的离子方程式为___。
 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________。
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________。
 下列物质中,也可以使该溶液红色褪去的是 _________。
下列物质中,也可以使该溶液红色褪去的是 _________。
A.新制氯水  碘水
碘水 
 盐酸
盐酸
 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为_______________。
和一种单质气体,该反应的离子方程式为_______________。
-
IBr、ICl等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应_______
,该反应_______ 填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。
 溴化碘
溴化碘 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为___。
溶液发生反应,发生反应的离子方程式为___。
 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________。
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________。
 下列物质中,也可以使该溶液红色褪去的是 _________。
下列物质中,也可以使该溶液红色褪去的是 _________。
A.新制氯水  碘水
碘水 
 盐酸
盐酸
 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为_______________。
和一种单质气体,该反应的离子方程式为_______________。
-
IBr、ICl、BrF3等称之为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似,请回答下列问题。
(1)氯化碘(ICl)中碘元素的化合价为_______,它与水反应的化学方程式为ICl+ H2O HIO +HCl,该反应的反应类型为___________(填中学常见的无机反应类型);
HIO +HCl,该反应的反应类型为___________(填中学常见的无机反应类型);
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液发生反应,发生反应的离子方程式为:
____________________________________________________________________________________;
(3)①已知某些离子的还原性强弱顺序为I−>SCN−>CN−>Br−>Cl−。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象____________________________________________________________;
②下列物质中,也可以使该溶液红色褪去的是_________;
A.新制氯水 B.NaBr溶液 C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将CN−氧化为 和一种参与大气循环的单质气体,该反应的离子方程式为________________________;
和一种参与大气循环的单质气体,该反应的离子方程式为________________________;
(5)已知HCN的电离平衡常数K=6.2×10−10,H2CO3的 电离平衡常数K1=4.5×10−7,K2=4.7×10−11,则下列离子方程式能发生的是_________。
A.CN−+CO2+H2O HCN+
HCN+ B.2HCN+
B.2HCN+
 2CN−+CO2↑+H2O
2CN−+CO2↑+H2O
C.2CN−+CO2+H2O HCN+
HCN+ D.HCN+
D.HCN+
 CN−+
CN−+
-
IBr、ICl、BrF3等称之为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似,请回答下列问题。
(1)氯化碘(ICl)中碘元素的化合价为_______,它与水反应的化学方程式为ICl+ H2O HIO +HCl,该反应的反应类型为___________(填中学常见的无机反应类型);
HIO +HCl,该反应的反应类型为___________(填中学常见的无机反应类型);
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液发生反应,发生反应的离子方程式为:_______;
(3)①已知某些离子的还原性强弱顺序为I−>SCN−>CN−>Br−>Cl−。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________;
②下列物质中,也可以使该溶液红色褪去的是_________;
A.新制氯水 B.碘水 C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将CN−氧化为 和一种单质气体,该反应的离子方程式为__________________;
和一种单质气体,该反应的离子方程式为__________________;
(5)已知HCN的电离平衡常数K=6.2×10−10,H2CO3的 电离平衡常数K1=4.5×10−7,K2=4.7×10−11,则下列离子方程式能发生的是_________。
A.CN−+CO2+H2O HCN+
HCN+ B.2HCN+
B.2HCN+
 2CN−+CO2↑+H2O
2CN−+CO2↑+H2O
C.2CN−+CO2+H2O HCN+
HCN+ D.HCN+
D.HCN+
 CN−+
CN−+
-
IBr、ICl、BrF3等称之为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似,请回答下列问题。
(1)氯化碘(ICl)中碘元素的化合价为____________,它与水反应的化学方程式为ICl+ H2O= HIO +HCl,该反应的反应类型为___________(填中学常见的无机反应类型);
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液反应,发生反应的离子方程式为:_______;
(3)①已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________;
② 下列物质中,也可以使该溶液红色褪去的是_________;
A.新制氯水 B.碘水 C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将CN-氧化为CO32-和一种单质气体,该反应的离子方程式为__________________;
(5)已知HCN的电离平衡常数K=6.2×10-10,H2CO3的 电离平衡常数K1=4.5×10-7,K2=4.7×10-11,则下列离子方程式能发生的是_________。
A.CN-+CO2+H2O=HCN+HCO3- B.2HCN+CO32-=2CN-+CO2↑+H2O
C.2CN-+CO2+H2O=HCN+CO32- D.HCN+CO32-=CN-+HCO3-
-
IBr、ICl、BrF3等称之为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是____________________ 。
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液发生反应,发生反应的离子方程式为______________________________________________________________;
(3)①已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象____________________________;
② 下列物质中,也可以使该溶液红色褪去的是_________;
A.新制氯水 B.碘水 C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将CN-氧化为CO32-和一种单质气体,该反应的离子方程式为________________;
(5)已知HCN的电离平衡常数K=6.2×10-10,H2CO3的 电离平衡常数K1=4.5×10-7,K2=4.7×10-11,则下列离子方程式能发生的是_________。
A.CN-+CO2+H2O═HCN+HCO3- B.2HCN+CO32-=2CN-+CO2↑+H2O
C.2CN-+CO2+H2O═HCN+CO32- D.HCN+CO32-=CN-+HCO3-
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为__。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为__。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于__。
(4)互为等电子体的微粒相互之间结构相似。I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为___,中心原子杂化类型为__。
(5)铁在元素周期表中的位置___(用“周期”和“族”来描述)。
(6)简述三价铁比二价铁稳定的原因___。
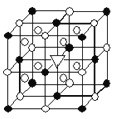
(7)如图所示为卤化物冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子__、__;大立方体的体心处▽所代表的是__。
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)卤素互化物如IBr ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸点由髙到低的顺序为
_____,I和Cl相比,电负性较大的是_____。
(2)基态溴原子的电子排布式为_____,碘原子价电子的电子排布图为_____。
(3)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为______,中心I原子的杂化轨道类型为
__________。
(4)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为_______(填序号)。
(5) 离子化合物RbICl2存在复合阴离子,且晶体结构与NaCl相似,晶胞边长为685.5pm( pm=10-12m), RbICl2晶胞中含有______个氯原子,RbICl2晶体的密度是_____g•cm3(只要求列箅式,不必计算出数值。阿伏伽德罗常数为NA)。
-
氯化碘(ICl)与Cl2性质相似,可发生下列反应,①2ICl+2Mg═MgI2+MgCl2②ICl+H2O═HCl+HIO.对上述两个反应的有关说法正确的是( )
A.ICl是一种新的卤素单质
B.反应①中MgI2既是氧化产物,又是还原产物
C.反应②中ICl既是氧化剂,又是还原剂
D.固态ICl是一种离子晶体
-
粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )。
A.H2O B.Zn C.KI D.KCl
、
、
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
氯化碘
能与水发生反应:
,该反应_______
填“是”或“不是”
氧化还原反应。
溴化碘
具有强氧化性,能与
溶液发生反应,发生反应的离子方程式为___。
已知某些离子的还原性强弱顺序为
。现将几滴KSCN溶液滴入到含少量
的溶液中,溶液立即变红,向其中逐滴滴入酸性
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________。
下列物质中,也可以使该溶液红色褪去的是 _________。
碘水
盐酸
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
氧化为
和一种单质气体,该反应的离子方程式为_______________。
